
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
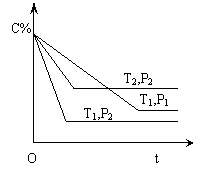
8.”””””””” ŗ²ĮÖ»ćĻĀĮŠæÉÄę·“Ó¦“ļĘ½ŗāדĢ¬ŗ󣬽µĪĀæÉŅŌŹ¹»ģŗĶĘųĢåĘ½¾ł·Ö×ÓĮæ¼õŠ”µÄŹĒ
””””
A£®H2(Ęų)+Br2(Ęų) 2HBr(Ęų)+Q
2HBr(Ęų)+Q
””””
B£®N2(Ęų)+3H2(Ęų) 2NH3(Ęų)+Q
2NH3(Ęų)+Q
””””
C£®2SO3(Ęų) 2SO2(Ęų)+O2(Ęų)£Q
2SO2(Ęų)+O2(Ęų)£Q
 D£®4NH3(Ęų)+5O2(Ęų)
D£®4NH3(Ęų)+5O2(Ęų) 4NO(Ęų)+6H2O(Ęų)+Qŗ²ĮÖ»ć
4NO(Ęų)+6H2O(Ęų)+Qŗ²ĮÖ»ć
7.””””””””
ŌŚÄ³Ņ»ĆܱÕČŻĘ÷ÖŠ£¬³äČėŅ»¶ØĮæµÄHIĘųĢ壬·¢Éś·“Ó¦2HI(Ęų) 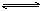 H2(Ęų)+I2(Ęų)£Q£¬ŌŚt1Ź±“ļµ½Ę½ŗā£¬t2Ź±¼ÓČČÉżĪĀ²¢±£ĪĀ£¬µ½t3Ź±ÓÖ“ļµ½ŠĀĘ½ŗā£¬·ūŗĻÕāŅ»±ä»ÆµÄĶ¼ĻńŹĒ
H2(Ęų)+I2(Ęų)£Q£¬ŌŚt1Ź±“ļµ½Ę½ŗā£¬t2Ź±¼ÓČČÉżĪĀ²¢±£ĪĀ£¬µ½t3Ź±ÓÖ“ļµ½ŠĀĘ½ŗā£¬·ūŗĻÕāŅ»±ä»ÆµÄĶ¼ĻńŹĒ
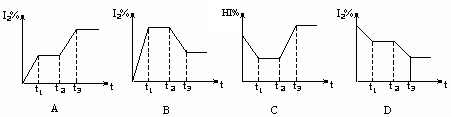 ””
””
6.””””””””
Ņ»¶ØĪĀ¶ČŹ±ÓŚĆÜ·āČŻĘ÷ÖŠ·¢Éś·“Ó¦£ŗmA(g)+nB(g) 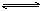 ””pC(g)£¬“ļĘ½ŗāŗó£¬Čō½«ĘųĢåĢå»żŃ¹Ėõµ½ŌĄ“µÄ1/2”£µ±ŌŁ“ļĘ½ŗāŹ±CµÄÅØ¶ČŹĒŌĄ“µÄ1.9±¶£¬ŌņĻĀĮŠŠšŹöÕżČ·µÄ
””pC(g)£¬“ļĘ½ŗāŗó£¬Čō½«ĘųĢåĢå»żŃ¹Ėõµ½ŌĄ“µÄ1/2”£µ±ŌŁ“ļĘ½ŗāŹ±CµÄÅØ¶ČŹĒŌĄ“µÄ1.9±¶£¬ŌņĻĀĮŠŠšŹöÕżČ·µÄ
A£®Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ”””” ”””””” ”””””””””””””” B£®CĘųĢåµÄÖŹĮæ·ÖŹżŌö“ó
C£®ĘųĢåAµÄ×Ŗ»ÆĀŹ½µµĶ”””””””” ”””””” ”””” ”””””” D£®m+n£¾p
5.””””””””
½«2 mol SO2ŗĶ2 mol SO3ĘųĢ壬³äČė¹Ģ¶ØĢå»żµÄĆܱÕČŻĘ÷£¬ŌŚŅ»¶ØĢõ¼žĻĀ·¢ÉśĻĀĮŠ·“Ó¦£ŗ2SO2+O2
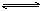 ””2SO3£¬Ę½ŗāŹ±SO3ĪŖn mol£¬ĻąĶ¬ĪĀ¶ČĻĀ£¬·Ö±š°“ĻĀĮŠÅä±ČŌŚĻąĶ¬Ģå»żµÄĆܱÕČŻĘ÷ÖŠ¼ÓČėĘšŹ¼ĪļÖŹ£¬µ½“ļĘ½ŗāŹ±SO3µÄĪļÖŹµÄĮæ“óÓŚn molµÄŹĒ
””2SO3£¬Ę½ŗāŹ±SO3ĪŖn mol£¬ĻąĶ¬ĪĀ¶ČĻĀ£¬·Ö±š°“ĻĀĮŠÅä±ČŌŚĻąĶ¬Ģå»żµÄĆܱÕČŻĘ÷ÖŠ¼ÓČėĘšŹ¼ĪļÖŹ£¬µ½“ļĘ½ŗāŹ±SO3µÄĪļÖŹµÄĮæ“óÓŚn molµÄŹĒ
A£®2 mol SO2+1mol O2”””””””””””””””””””””””””””””””” ”””” B£®4 mol SO2+1mol O2
C£®2 mol SO2+1mol O2 +2 mol SO3”””””””””””” D£®3 mol SO2+1 mol SO3
4.”””””””” “ÓĻĀĮŠŹĀŹµ£¬²»ÄÜÓĆĄÕɳĢŲĮŠŌĄķ½āŹĶµÄŹĒ
A£®äåĖ®ÖŠÓŠĻĀĮŠĘ½ŗāBr2+H2O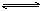 HBr + HBrO,µ±¼ÓČėAgNO3ČÜŅŗŗó£¬ČÜŅŗŃÕÉ«±äĒ³
HBr + HBrO,µ±¼ÓČėAgNO3ČÜŅŗŗó£¬ČÜŅŗŃÕÉ«±äĒ³
B£®¶Ō2HI(g)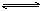 H2(g)+I2(g),Ę½ŗāĢåĻµŌö“óŃ¹ĒææÉŹ¹ŃÕÉ«±äÉī
H2(g)+I2(g),Ę½ŗāĢåĻµŌö“óŃ¹ĒææÉŹ¹ŃÕÉ«±äÉī
C£®·“Ó¦CO+NO2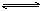 CO2+NO+Q,ÉżøßĪĀ¶ČæÉŹ¹Ę½ŗāĻņÄę·“Ó¦·½ĻņŅʶÆ
CO2+NO+Q,ÉżøßĪĀ¶ČæÉŹ¹Ę½ŗāĻņÄę·“Ó¦·½ĻņŅʶÆ
D£®ŗĻ³ÉNH3·“Ó¦£¬ĪŖĢįøßNH3µÄ²śĀŹ£¬ĄķĀŪÉĻÓ¦²ÉČ”µĶĪĀ¶ČµÄ“ėŹ©
3.””””””””
ŌŚ3NO2+H2O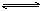 2HNO3+NO+Q·“Ó¦“ļµ½Ę½ŗāŗó£¬øıäĻĀĮŠĢõ¼ž£¬æÉŹ¹HNO3ÅضČŌö“óµÄŹĒ
2HNO3+NO+Q·“Ó¦“ļµ½Ę½ŗāŗó£¬øıäĻĀĮŠĢõ¼ž£¬æÉŹ¹HNO3ÅضČŌö“óµÄŹĒ
A£®ÉżĪĀ”” ”””””””””” B£®¼õŃ¹”” ”””””””””””””””””” C£®¼ÓĖ®”” ”””””””””””””””””” D£®ĶØČėO2
2.”””””””” Ņ»¶ØĪĀ¶ČĻĀ£¬ŌŚ¹Ģ¶ØČŻ»żµÄĆܱÕČŻĘ÷ÖŠ£¬æÉÄę·“Ó¦£ŗ
””mA(Ęų)+nB(Ęų)”” 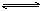 ””pC(Ęų)+qD(Ęų)£¬µ±m”¢n”¢p”¢qĪŖČĪŅāÕżÕūŹżŹ±£¬ĻĀĮŠ×“Ģ¬£ŗ¢ŁĢåĻµµÄŃ¹Ēæ²»ŌŁ·¢Éś±ä»Æ£¬¢ŚĢåĻµµÄĆÜ¶Č²»ŌŁ·¢Éś±ä»Æ£¬¢Ūø÷×é·ÖµÄĪļÖŹµÄĮæÅØ¶Č²»ŌŁøı䣬¢Üø÷×é·ÖµÄÖŹĮæ·ÖŹż²»ŌŁøı䣬¢Ż·“Ó¦ĖŁĀŹVA£ŗVB£ŗVC£ŗVD=m£ŗn£ŗp£ŗq£¬ĘäÖŠ£¬ÄÜĖµĆ÷·“Ó¦ŅŃ“ļµ½Ę½ŗāµÄŹĒ
””pC(Ęų)+qD(Ęų)£¬µ±m”¢n”¢p”¢qĪŖČĪŅāÕżÕūŹżŹ±£¬ĻĀĮŠ×“Ģ¬£ŗ¢ŁĢåĻµµÄŃ¹Ēæ²»ŌŁ·¢Éś±ä»Æ£¬¢ŚĢåĻµµÄĆÜ¶Č²»ŌŁ·¢Éś±ä»Æ£¬¢Ūø÷×é·ÖµÄĪļÖŹµÄĮæÅØ¶Č²»ŌŁøı䣬¢Üø÷×é·ÖµÄÖŹĮæ·ÖŹż²»ŌŁøı䣬¢Ż·“Ó¦ĖŁĀŹVA£ŗVB£ŗVC£ŗVD=m£ŗn£ŗp£ŗq£¬ĘäÖŠ£¬ÄÜĖµĆ÷·“Ó¦ŅŃ“ļµ½Ę½ŗāµÄŹĒ
A£®Ö»ÓŠ¢Ū¢Ü”” ”” B£®¢Ś¢Ū¢Ü”””””””””””””””””” C£®¢Ł¢Ę¢Ē¢Ü”” ”””””””””” D£®¢Ł¢Ś¢Ū¢Ü¢Ż
1.””””””””
·“Ó¦4NH3+5O2 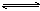 4NO+6H2OŌŚ5LµÄĆܱÕČŻĘ÷ÖŠ½ųŠŠ£¬°ė·ÖÖÓŗó£¬NOµÄĪļÖŹµÄĮæŌö¼ÓĮĖ0.3mol£¬ŌņĻĀĮŠ·“Ó¦ĖŁĀŹÕżČ·µÄŹĒ
4NO+6H2OŌŚ5LµÄĆܱÕČŻĘ÷ÖŠ½ųŠŠ£¬°ė·ÖÖÓŗó£¬NOµÄĪļÖŹµÄĮæŌö¼ÓĮĖ0.3mol£¬ŌņĻĀĮŠ·“Ó¦ĖŁĀŹÕżČ·µÄŹĒ
A£®V(O2)=0.01mol”¤L-1 ”¤s-1”” ”””””””””””””” ””””B£®V(NO)=0.008mol L-1 ”¤s-1
C£®V(H2O)=0.015mol L-1 ”¤s-1”””””””””””” ”””” D£®V(NH3)=0.002mol L-1 ”¤s-1
20£®Č”µČĪļÖŹµÄĮæÅØ¶ČµÄNaOHČÜŅŗĮ½·Ż£¬Ćæ·ŻĪŖ50mL”£ĻņĘäÖŠø÷ĶØČėŅ»¶ØĮæµÄCO2£¬Ėęŗó·Ö±šø÷Č”ČÜŅŗ10mL£¬½«ĘäĻ”ŹĶ³É100mL£»²¢·Ö±šĻņĻ”ŹĶŗóµÄČÜŅŗÖŠÖšµĪ¼ÓČė0.1mol”¤L-1µÄHClČÜŅŗ£¬²śÉśµÄCO2ĘųĢåĢå»ż(±ź×¼×“æö)ÓėĖł¼ÓČėŃĪĖįµÄĢå»żÖ®¼äµÄ¹ŲĻµČēĻĀĶ¼ĖłŹ¾£ŗ(Éč·Ö±šĪŖA”¢BĮ½ÖÖĒéæö)”£
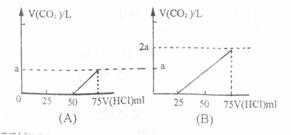
»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)ŌŚ(A)ĒéæöĻĀ£¬ČÜÖŹĪŖ(Š“»ÆѧŹ½)__________£¬ĘäĪļÖŹµÄĮæÖ®±ČĪŖ__________£¬ŌŚ±ź×¼×“æöĻĀCO2ĘųĢåµÄĢå»żĪŖ____________”£
”””””” (2)ŌŚ(B)ĒéæöĻĀ£¬ČÜÖŹĪŖ(Š“»ÆѧŹ½)________________£¬ĘäĪļÖŹµÄĮæÖ®±ČĪŖ______£¬ŌŚ±ź×¼×“æöĻĀCO2ĘųĢåµÄĢå»żĪŖ____________”£
”””””” (3)ŌNaOHČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ____________”£
19£®½«mgĢś·ŪŌŚ500mL pH=1µÄŃĪĖįÖŠĶźČ«Čܽā£¬ĻņČÜŅŗÖŠĶØČėŹŹĮæµÄĀČĘų£¬Ē”ŗĆĶźČ«·“Ó¦ŗó£¬ŌŁ¼ÓČė0.02mol/LµÄNiIxČÜŅŗ500mLŹ±£¬øÕŗĆŹ¹I-×Ŗ±äĪŖI2Īö³ö£¬“ĖŹ±ČÜŅŗµÄpH=2”£ŅŃÖŖ·“Ó¦Ē°ŗóNix+µÄ»ÆŗĻ¼Ūƻӊ±ä»Æ£¬·“Ó¦¹ż³ĢÖŠČÜŅŗĢå»żµÄ±ä»ÆæÉŅŌŗöĀŌ”£ŹŌĶعż¼ĘĖćĒó(1)mÖµ”£(2)xÖµ”£
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com