
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
20°¢“™«Û…˺∆ µ—È÷§√˜£¨ƒ≥÷÷—ŒµƒÀÆΩ‚ «Œ¸»»µƒ£¨œ¬¡–ªÿ¥’˝»∑µƒ «
A. Ω´œıÀ·ÔßæßûД⁄ÀÆ£¨»ÙÀÆŒ¬œ¬Ωµ£¨Àµ√˜œıÀ·ÔßÀÆΩ‚ «Œ¸»»µƒ
B. ‘⁄—ŒÀ·÷–º”»ÎœýÕ¨≈®∂»µƒ∞±ÀÆ£¨»ÙªÏ∫œ“∫Œ¬∂»œ¬Ωµ£¨Àµ√˜—Œ¿ýÀÆΩ‚ «Œ¸»»µƒ
C. ‘⁄¥◊À·ƒ∆»Ð“∫÷–º”»Î¥◊À·ƒ∆æß㨻ٻГ∫Œ¬∂»œ¬Ωµ£¨Àµ√˜—Œ¿ýÀÆΩ‚ «Œ¸»»µƒ
D. ‘⁄¥◊À·ƒ∆»Ð“∫÷–µŒ»Î∑”Ù ‘“∫£¨º”»»∫Û»Ù∫Ï…´º”…Ó£¨Àµ√˜—Œ¿ýÀÆΩ‚ «Œ¸»»µƒ
µ⁄IIæÌ(∑«—°‘Ò£¨π≤80∑÷)
19°¢‘⁄»»µƒœ°¡ÚÀ·»Ð“∫÷–»ÐΩ‚¡À11.4gFeSO4°£µ±º”»Î50mL0.5mol•L-1KNO3»Ð“∫∫Û£¨ π∆‰÷–µƒFe2+»´≤ø◊™ªØ≥…Fe3+£¨KNO3»Ð“∫“≤ÕÍ»´∑¥”¶£¨≤¢”–NxOy∆¯Ã“ð≥ˆ£¨‘Ú∏√NxOy «
A°¢N2O°°°°°°°°°°°°°° B°¢NO°°°°°°°°°°°°°°°° C°¢N2O3°°°°°°°°°°°° D°¢NO2
18°¢ƒ≥Œ¬∂»œ¬£¨»ÙΩ´Na2SO4»Ð“∫’Ù∑¢180 gÀÆ£¨ø…±‰≥…±•∫ջГ∫°£»ÙœÚ∏√»Ð“∫÷–º”»Î14.2gŒÞÀÆNa2SO4“≤ø…±‰≥…±•∫ջГ∫°£»Ù‘⁄∏√»Ð“∫÷–º”»ÎNa2SO4°§10H2O–Œ≥…±•∫ջГ∫ ±À˘–ËNa2SO4°§10H2Oµƒ÷ ¡øø…“‘Œ™
A£Æ14.2 g°°°°°°°°°° B£Æ32.2 g°°°°°° °°°°C£Æ35.8 g°°°°°°°°°° D£Æ46.4 g
17°¢ƒ≥—ß…˙…˺∆¡À»ÁÕºµƒ∑Ω∑®∂‘A—ŒΩ¯––º¯∂®£∫°°
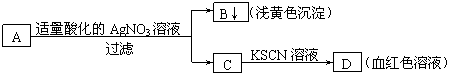 °°
°°
°° °°°° ”…¥À∑÷Œˆ£¨œ¬¡–Ω·¬€÷–£¨’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°°°°
°° A£ÆA÷–“ª∂®”–Fe3+°°°°°°°° B£ÆC÷–“ª∂®”–Fe3+°°
C£ÆBŒ™AgI≥¡µÌ°° °°°°°°°°°° D£ÆA“ª∂®Œ™FeBr2»Ð“∫
16°¢“—÷™µ±ŒÔ÷ µƒ¡ø≈®∂»œýÕ¨ ±£¨ÃºÀ·÷–c(CO32-)±»∆´¬¡À·÷–c(AlO2-)¥Ûµ√∂ý£¨‘Úœ¬¡–Õ∆¬€÷–’˝»∑µƒ «
A. Õ®»Î ¡øCO2”⁄AlO2-»Ð“∫÷–£¨”–CO32-…˙≥…
B. ∫¨CO32-µƒ»Ð“∫»ð“◊ πAl(OH)3»ÐΩ‚±‰≥…AlO2-
C. HCO3-÷ªƒÐ”ÎAl3+∑¥”¶∂¯≤ªƒÐ∫ÕAlO2-∑¥”¶
D. NH4+°¢AlO2-∫ÕHCO3-ƒÐ¥Û¡øπ≤¥Ê”⁄Õ¨“ª»Ð“∫÷–
15°¢‘⁄º◊…’±≠÷–∑≈»Î—ŒÀ·£¨““…’±≠÷–∑≈»Î¥◊À·£¨¡Ω÷÷»Ð“∫µƒÃª˝∫ÕpH∂ºœýµ»£¨œÚ¡Ω…’±≠÷–Õ¨ ±º”»Î÷ ¡ø≤ªµ»µƒ–ø¡££¨∑¥”¶Ω· ¯∫Ûµ√µΩµ»¡øµƒ«‚∆¯°£œ¬¡–Àµ∑®’˝»∑µƒ «
A°¢º◊…’±≠÷–∑≈»Î–øµƒ÷ ¡ø±»““…’±≠÷–∑≈»Î–øµƒ÷ ¡ø¥Û
B°¢º◊…’±≠÷–µƒÀ·π˝¡ø
C°¢¡Ω…’±≠÷–≤Œº”∑¥”¶µƒ–øµ»¡ø
D°¢∑¥”¶ø™ º∫Û““…’±≠÷–µƒc(H+) º÷’±»º◊…’±≠÷–µƒc(H+)–°
14°¢œ¬¡–∏˜»Ð“∫÷–£¨Œ¢¡£µƒŒÔ÷ µƒ¡ø≈®∂»πÿœµ’˝»∑µƒ «£∫
A£Æ10mL 0.5mol/L CH3COONa»Ð“∫”Î6mL 1mol/L—ŒÀ·ªÏ∫œ£∫
c(Cl£≠)£æc(Na+)£æc(H+)£æc(OH£≠)
B£Æ0.1mol/L pHŒ™4µƒNaHB»Ð“∫÷–£∫c(HB£≠)£æc(H2B)£æc(B2-)
C£Æ‘⁄NaHA»Ð“∫÷–“ª∂®”–£∫c(Na+)+c(H+)£Ωc(HA£≠)+c(OH£≠)+c(A2-)
D£Æc(NH4+)œýµ»µƒ(NH4)2SO4»Ð“∫°¢(NH4)2CO3»Ð“∫∫ÕNH4Cl»Ð“∫£∫
c[(NH4)2SO4]£ºc[(NH4)2CO3]£ºc(NH4Cl)
13°¢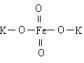 ∏þÃ˙À·ºÿ°° °°°°°°°°°°°°°° «“ª÷÷–¬–Õ°¢∏þ–ß°¢∂ýπ¶ƒÐÀÆ¥¶¿Ìº¡£¨ «±»Cl2°¢O3°¢ClO2°¢
∏þÃ˙À·ºÿ°° °°°°°°°°°°°°°° «“ª÷÷–¬–Õ°¢∏þ–ß°¢∂ýπ¶ƒÐÀÆ¥¶¿Ìº¡£¨ «±»Cl2°¢O3°¢ClO2°¢
KMnO4—ıªØ∏¸«ø£¨ŒÞ∂˛¥ŒŒ€»æµƒ¬Ã…´ÀÆ¥¶¿Ìº¡°£π§“µ «œ»÷∆µ√∏þÃ˙À·ƒ∆£¨»ª∫Û‘⁄µÕŒ¬œ¬£¨‘⁄∏þÃ˙À·ƒ∆»Ð“∫÷–º”»ÎKOH÷¡±•∫ÕæÕø…Œˆ≥ˆ∏þÃ˙À·ºÿ(K2FeO4)°£ ™∑®÷∆±∏µƒ÷˜“™∑¥”¶∑Ω≥ÃŒ™£∫2Fe(OH)3 +3ClO -+4OH- =2FeO42- +2Cl- +5H2O , ∏…∑®÷∆±∏µƒ÷˜“™∑¥”¶∑Ω≥ÃŒ™£∫2FeSO4 +6Na2O2 = 2Na2FeO4 +2Na2O +2Na2SO4 +O2°¸ œ¬¡–”–πÿÀµ∑®≤ª’˝»∑µƒ «£∫ A£Æ∏þÃ˙À·ºÿ÷–Ã˙œ‘+3º€°°°° °°
B£Æ ™∑®÷–√ø…˙≥…1mol Na2FeO4 ◊™“∆3molµÁ◊” C£Æ∏…∑®÷–√ø…˙≥…1mol Na2FeO4 ◊™“∆4molµÁ◊” D£ÆK2FeO4¥¶¿ÌÀÆ ±£¨≤ªΩˆƒÐœ˚∂æ…±æ˙£¨ªπƒÐ≥˝»•ÀÆÃÂ÷–µƒH2S°¢NH3µ»£¨…˙≥…µƒFe(OH)3ªπƒÐŒ¸∏ΩÀÆ÷–µƒ–¸∏°‘”÷
12°¢œ¬¡–¿Î◊”∑Ω≥Ã Ω È–¥’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°°A£ÆNa2HPO4»Ð“∫µƒÀÆΩ‚£∫°° HPO42£≠+H2O H3O++PO43£≠
H3O++PO43£≠
B£Æ¬¡∆¨»Ð”⁄ø¡–‘ƒ∆»Ð“∫£∫°° 2Al+2OH-+2H2O =2AlO2-+3H2°¸
C£Æ¬»ªØ«‚∆¯ÃÂÕ®»ÎœıÀ·“¯»Ð“∫°° C1£≠+ Ag += AgC1°˝
D£Æ∏÷Ã˙∑¢…˙Œ¸—ı∏Ø ¥ ±µƒ∏∫º´∑¥”¶ Ω£∫2H2O + O2 + 4e£≠= 4OH£≠
11°¢”√NA±Ì æ∞¢∑¸º”µ¬¬Þ≥£ ˝£¨œ¬¡–Àµ∑®’˝»∑µƒ «
A£Æ°°°°°°°°°°°° √ø…˝¡ÚÀ·»Ð“∫¿Ô∫¨”–10-2NA∏ˆH+£¨∏√¡ÚÀ·»Ð“∫µƒpHŒ™2
B£Æ°°°°°°°°°°°° ≥ ÷––‘µƒœ°»Ð“∫1L÷–¿Ô∫¨”–10-7NA∏ˆH+
C£Æ°°°°°°°°°°°° NA∏ˆNH4+”–10 mol÷ ◊”°°°°°° °°°°°°
D£Æ≥£Œ¬œ¬pH÷µŒ™2µƒ1L—ŒÀ·»Ð“∫÷–£¨◊È≥…—Ù¿Î◊”µƒ‘≠◊”∫ÀŒ™10-2NA∏ˆ
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com