
题目列表(包括答案和解析)
1. 下列变化过程中无化学键断裂或生成的是
A.石墨转化为金刚石 B.NaCl晶体溶于水 C.干冰升华 D.氮的固定
19、
[答案]A是KAl(SO4)2·12H2O;B为Al(OH)3;C为BaSO4;D为NaAlO2;E为AlCl3。
[解析]分析①可知,A晶体中含有钾离子。分析②可知,A晶体溶于水后显酸性,可判断A溶于水可电离出H+或A中含有易水解的阳离子。分析③、⑤、⑥可知,A晶体中可能含有Al3+。分析④可知,A晶体中含有SO42-。综合以上各个分析结果可得出A可能是明矾等。再根据⑦中的数据进行计算后可确证A是KAl(SO4)2·12H2O。
[方法指点]这类试题中往往有多条信息,需要解题者对每条信息一一进行分析,再把分析所得的结论进行综合,才能得出判断的结论。解题过程中,还常常边分析边综合。有的考生能顺利对单个信息进行分析判断,但对多信息的分析判断能力较差。高考复习训练中要重视培养分析处理多条信息作出判断的能力。
18、.(8分)
|
|
选择保存方法 |
解释 |
|
(1) |
② |
液体药品存放在细口瓶中,便于倾倒液体 |
|
(2) |
③ |
液溴能腐蚀橡皮塞,不能腐蚀玻璃塞 |
|
(3) |
⑤ |
液溴溶解于煤油,在水中的溶解度小,密度大于水,用水封将减少溴的挥发 |
|
(4) |
⑦ |
水封后上层溴水中的HBrO见光分解. |
17.(共11分)(8分)①Cu + 2H2SO4(浓) CuSO4+SO2↑+ 2H2O;(2分)
CuSO4+SO2↑+ 2H2O;(2分)
验证SO2的漂白性(1分); 吸收多余的SO2防止污染大气(1分);
SO2+Na2CO3 = Na2SO3 + CO2 (2分);
②用镊子夹取脱脂棉蘸取KMnO4溶液,然后将棉团代替碳酸钠溶液的棉团(1分),过一段时间观察棉团紫色消失或变浅,则证明SO2具有还原性(1分)。
16.(5分)明矾溶于水电离出来的铝离子水解生成氢氧化铝胶体(1分);吸附水中的悬浮物而使水得到净化(1分);SO42-(1分);取适量净化后的水加入试管中,先向试管中滴加少量盐酸,再加入BaCl2溶液(1分),若产生白色沉淀,则说明净化后的水中含有SO42-(1分);
9、B 10、D 11、D 12、C 13、D 14、D 15、A
19.A是一种无色透明的晶体,进行如下实验:
①取少量A晶体做焰色反应实验,透过蓝色钴玻璃观察,火焰呈紫色。
②取少量A晶体溶于水可以得到无色的溶液,该溶液使石蕊变红。
③取少量A的溶液加过量氨水,有白色沉淀B生成。
④过滤除去③中的B后,再在滤液中滴加氯化钡溶液,有白色沉淀C生成,C不溶于稀硝酸。
⑤取少量B滴加氢氧化钠溶液,得无色溶液D。
⑥取少量B滴加盐酸,得无色溶液E。
⑦将47.4gA晶体在120℃下加热脱水,剩余物的质量为25.8g。
根据上述实验现象和结果确定A、B、C、D、E,写出它们的化学式。
A ______ __;B____ ____;C___ _____;D_____ ___;E_______ _。
答案:1、D 2、A 3、D 4、D 5、B 6、A 7、B 8、C
18.(8分)根据溴的性质,填写下列表格中关于液溴保存方法的选择及有关原因的解释: ①广口瓶②细口瓶③玻璃塞④橡皮塞⑤水封⑥煤油封⑦棕色瓶⑧无色瓶
|
|
选择保存方法 |
解释 |
|
(1) |
|
|
|
(2) |
|
|
|
(3) |
|
|
|
(4) |
|
|
17.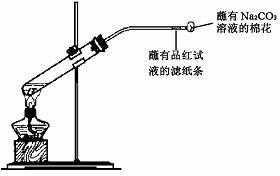 (7分)①某同学用下图所示装置制备SO2
并验证其性质,试管内有一小片铜片和浓硫酸,试管内发生反应的化学方程式为
;导管中品红试纸的作用是
;导管口蘸有碳酸钠溶液的棉花的作用是
;相关的化学方程式是
。
(7分)①某同学用下图所示装置制备SO2
并验证其性质,试管内有一小片铜片和浓硫酸,试管内发生反应的化学方程式为
;导管中品红试纸的作用是
;导管口蘸有碳酸钠溶液的棉花的作用是
;相关的化学方程式是
。
②实验室中现有下列实验用品:氢硫酸、NaOH溶液、KMnO4溶液、脱脂棉、镊子、pH试纸、玻璃棒请设计实验验证SO2的还原性,简述实验操作步骤和现象
。
16. (5分)铝及其化合物在生活中有着广泛应用。在我国南方某些地区,当地居民常采用往水中加明矾的方法来处理水中的悬浮杂质。其原理为
。明矾处理后的水中含有较多的阴离子为 ;写出用化学方法验证水中含有这种阴离子的操作和现象:
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com