
题目列表(包括答案和解析)
19.(12分)已知X、Y、Z都是短周期的元素,它们的原子序数依次递增。X原子的电子层数与它的核外电子总数相同,而Z原子的最外层电子数是次外层电子数的三倍,Y和Z可以形成两种以上气态化合物,则
(1)X是 、Y是 、Z是 。(写名称)
(2)由Y和Z组成,且Y和Z质量比为7∶20的化合物的化学式(分子式)是
。
(3)由X、Y、Z中的两种元素组成,且与X2Z分子具有相同电子数的两种离子是 和 。
(4)X、Y、Z可以形成一种盐,此盐中X、Y、Z元素的原子的个数比为4∶2∶3,该盐的化学式(分子式)是 。
18.(12分)用18.4 mol·L-1的浓H2SO4配制100 mL浓度为1 mol·L-1的稀H2SO4,其操作可分为以下各步:
A.用量筒取 mL浓H2SO4缓缓注入装有约50 mL蒸馏水的烧杯中,并用玻璃棒不断搅拌
B.用约30 mL蒸馏水,分成三次洗涤烧杯和玻璃棒,将每次洗液都倒入容量瓶里
C.将稀释后的H2SO4小心倒人容量瓶里
D.检查100 mL容量瓶口部是否会发生漏液
E.将蒸馏水直接加入容量瓶至液面接近环形刻度线1~2 cm处
F.盖紧瓶塞,反复颠倒,摇匀溶液
G.用 向容量瓶里逐滴滴人蒸馏水,至液面最低点恰好与环形刻度线相切
据此填写:
(1)上述各步的空白处。
(2)正确的操作顺序是(字母填写) 。
(3)进行A步操作应选择下列量器:①10 mL量筒;②50 mL量筒;③500 mL量筒;④1000mL量筒中的 (填写序号)。
(4)进行A步操作后,必须 后,才能进行下一步操作。
(5)下列情况对实验结果产生偏低影响的是 。(填入编号)
A.容量瓶中原有少量蒸馏水
B.稀释所用烧杯洗涤2~3次,洗涤液一并注入容量瓶
C.定容时,仰视读刻度线
D.量取浓H2SO4时,仰视读数
17.(6分)由氢气和氧气反应生成1 mol水蒸气放热241.8 kJ,写出该反应的热化学方程式:
。若1g水蒸气转化成液态水放热2.444 kJ,则反应H2(g)+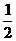 O2(g)=H2O(1)的ΔH=
kJ·mol-1,氢气的燃烧热为
kJ·mol-1。
O2(g)=H2O(1)的ΔH=
kJ·mol-1,氢气的燃烧热为
kJ·mol-1。
16.运用元素周期律分析下面的推断。其中错误的是
A.已知Ra是第七周期、IIA族的元素,故Ra(OH)2的碱性比Mg(OH)2的碱性强
B.已知Cs的原子半径比Na的大,故Cs与水反应比Na与水反应更剧烈
C.已知As是第四周期、VA族的元素,故AsH3的稳定性比NH3的稳定性强
D.已知Cl的核电荷数比Al的核电荷数大,故Cl的原子半径比Al的原子半径小
高三化学复习班下期第一次月考
化 学 试 卷
 高2007届理科复习班 姓名__________ 得分____________
高2007届理科复习班 姓名__________ 得分____________
15.1999年1月,俄美科学家联合小组宣布合成出114号元素的一种同位素,该同位素原子的质量数为298。以下叙述不正确的是
A.该元素属于第七周期
B.该元素位于ⅢA族
C.该元素为金属元素,性质与82Pb相似
D.该同位素原子含有114个电子,184个中子
14.已知1-18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是
A.质子数c>b B.离子的还原性Y2->Z-
C.氢化物的稳定性H2Y>HZ D.原子半径X<W
13.在一定条件下,RO3n-与R2-发生如下反应:RO3n- + 2R2- + 6H+ == 3R + 3H2O,下列关于元素R的叙述中正确的是
A.R原子的最外层上有4个电子 B.RO3n-中的R只能被还原
C.HnRO3一定是强酸 D.R的单质既有氧化性又有还原性
12.已知:
①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;
②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;
③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。
下列判断正确的是
A.上述实验证明氧化性:MnO4->Cl2>Fe3+>I2
B.上述实验中,共有两个氧化还原反应
C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝
D.实验②证明Fe2+既有氧化性又有还原性
11.已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化
H2O2 →H2O IO3- →I2 MnO4-→Mn2+ HNO2→NO
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是
A.H2O2 B.IO3- C.MnO4- D.HNO2
10.下图是几种盐的溶解度曲线下列说法正确是
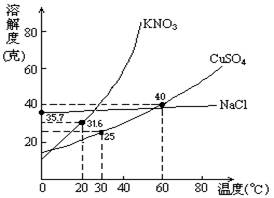
A.40 ℃时,将35 g食盐溶于100 g水中,降温至0 ℃时,可析出氯化钠晶体
B.20 ℃时,硝酸钾饱和溶液中溶质的质量分数为31.6%
C.60 ℃时,200 g水中溶解80 g硫酸铜达饱和,当降温至30 ℃时,可析出30 g硫酸铜晶体
D.30 ℃时,将35 g硝酸钾和35 g食盐同时溶于100 g水中,蒸发时,先析出的是氯化钠
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com