
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
9Θ° 24g ·”ΔΚΆ80g ·Μ“ ·‘ΎΗΏΈ¬œ¬≥δΖ÷Ζ¥”ΠΘ§Ζ≈≥ωΒΡΤχΧε‘Ύ±ξΉΦΉ¥Ωωœ¬ΒΡΧεΜΐ «
ΓΓ ΓΓAΘ°4.48LΓΓΓΓΓΓΓΓ BΘ°8.96LΓΓΓΓΓΓ CΘ°11.2LΓΓΓΓΓΓ DΘ°17.92L
8Θ°”“ΆΦ÷–aΓΔbΓΔcΓΔdΓΔeΓΔfΈΣ‘ΣΥΊ÷ήΤΎ±μ÷–«Α4÷ήΤΎΒΡœύΝΎΒΡ“Μ≤ΩΖ÷‘ΣΥΊΘ§œ¬Ν–”–ΙΊ–π ω’ΐ»ΖΒΡ «
AΘ°bΓΔcΓΔe»ΐ÷÷‘ΣΥΊΒΡΒΞΚΥάκΉ”ΑκΨΕ¥σ–ΓΙΊœΒΘΚ e>b>c
BΘ°Νυ÷÷‘ΣΥΊ÷–Θ§d‘ΣΥΊΒΡ–‘÷ ΉνΈ»Ε®
CΘ°cΒΡ«βΜ·ΈοΖ–Βψ±»f«βΜ·ΈοΒΡΖ–ΒψΒΆ
DΘ°b‘ΣΥΊ≥ΐ0ΦέΆβΘ§÷Μ”–“Μ÷÷Μ·ΚœΦέΓΓ
7Θ°Ζ÷άύΖΫΖ®‘ΎΜ·―ß―ßΩΤΒΡΖΔ’Ι÷–ΤπΒΫΝΥΖ«≥Θ÷Ί“ΣΒΡΉς”ΟΓΘœ¬Ν–Ζ÷άύ±ξΉΦΚœάμΒΡ «
ΓΓ ΔΌΓΓΗυΨίΥαΖ÷Ή”÷–Κ§”–ΒΡH‘≠Ή”Ηω ΐΫΪΥαΖ÷ΈΣ“Μ‘ΣΥαΓΔΕΰ‘ΣΥαΒ»
ΔΎΓΓΗυΨίΖ¥”Π÷– «Ζώ”–ΒγΉ”ΒΡΉΣ“ΤΫΪΜ·―ßΖ¥”ΠΖ÷ΈΣ―θΜ·ΜΙ‘≠Ζ¥”ΠΚΆΖ«―θΜ·ΜΙ‘≠Ζ¥”Π
ΔέΓΓΗυΨίΖ÷…ΔœΒ «ΖώΨΏ”–ΕΓ¥οΕϊœ÷œσΫΪΖ÷…ΔœΒΖ÷ΈΣ»ή“ΚΓΔΫΚΧεΚΆΉ«“Κ
ΔήΓΓΗυΨίΖ¥”Π÷–ΒΡ»»–ß”ΠΫΪΜ·―ßΜ·―ßΖ¥”ΠΖ÷ΈΣΖ≈»»Ζ¥”ΠΚΆΈϋ»»Ζ¥”Π
AΘ°ΔΌΔέΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°ΔΎΔήΓΓΓΓΓΓΓΓΓΓΓΓ CΘ°ΔΌΔΎΔήΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°ΔΎΔέΔή
|
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
a |
|
ΓΓ |
ΓΓ |
b |
c |
ΓΓ |
|
d |
e |
ΓΓ |
ΓΓ |
ΓΓ |
|
ΓΓ |
ΓΓ |
ΓΓ |
f |
ΓΓ |
6Θ° 2005Ρξ10‘¬12»’Θ§‘Ί”–ΝΫΟϊΚΫΧλ‘±ΒΡ…ώ÷ίΝυΚ≈‘Ύ
2005Ρξ10‘¬12»’Θ§‘Ί”–ΝΫΟϊΚΫΧλ‘±ΒΡ…ώ÷ίΝυΚ≈‘Ύ
ΨΤ»ΣΖΔ…δ÷––ΡΥ≥άϊ…ΐΩ’≤Δ”Ύ5ΧλΚσΑ≤»ΪΖΒΜΊΘ§’β±μΟς
Έ“ΙζΒΡ‘Ί»ΥΚΫΧλ ¬“Β”÷»ΓΒΟ–¬ΒΡΆΜΤΤΓΘ”“ΆΦ «ΓΑ…ώΝυΓ±
ΖΔ…δ…ΐΩ’ ±ΒΡ’’Τ§ΓΘΓΓΆΤΕ·…œ«ßΕ÷ΒΡΜπΦΐΚΆΖ…¥§ΒΡΨό¥σ
ΡήΝΩ «¥”ΡΡάοά¥ΒΡΘΩΜ·―ßΖ¥”ΠΝΔœ¬…ώΙΠΓΘΜπΦΐ Ι”ΟΒΡ»Φ
Νœ «ΤΪΕΰΦΉκ¬[(CH3)2NNH2]Θ§ΜπΦΐ…ΐΩ’ ±ΖΔ…ζΒΡΜ·―ßΖ¥
”ΠΈΣΘΚC2H8N2+2N2O4ΘΫ2CO2Γϋ+3N2Γϋ+4H2OΓϋΓΘ
œ¬Ν–”–ΙΊΗΟΖ¥”ΠΒΡΥΒΖ®’ΐ»ΖΒΡ «
ΓΓ ΓΓAΘ°ΗΟΖ¥”ΠΒΡ―θΜ·ΦΝ «ΤΪΕΰΦΉκ¬ΓΓΓΓΓΓ ΓΓBΘ°ΗΟΖ¥”ΠΫχ–– ±÷Μ”–Ζ≈»»Ιΐ≥ΧΟΜ”–Έϋ»»Ιΐ≥Χ
CΘ°ΗΟΖ¥”Π÷–ΒΣ‘ΣΥΊΒΡΜ·ΚœΦέ…ΐΗΏΓΓΓΓ ΓΓ ΓΓDΘ°ΗΟΖ¥”Π÷–ΟΩ…ζ≥…1molΓΓCO2ΉΣ“Τ8molΒγΉ”
5Θ°SO2 «≥ΘΦϊΒΡ¥σΤχΈέ»ΨΈο÷°“ΜΘ§Έ“ΙζΙφΕ®Ω’Τχ÷–SO2Κ§ΝΩ≤ΜΒΟ≥§Ιΐ0.02mg/LΘ§œ¬Ν–¥κ ©÷–ΡήΙΜΦθ…ΌSO2≈≈Ζ≈ΝΩΒΡ «
ΔΌ”ΟΧλ»ΜΤχ¥ζΧφΟΚΧΩΉωΟώ”Ο»ΦΝœΔΎ Ι”ΟΥ°ΟΚΤχΜρΗ…ΝσΟΚΤχΉω»ΦΝœΔέΝρΥα≥ß Ι”ΟV2O5Ής¥ΏΜ·ΦΝΘ§Φ”ΩλSO2ΒΡΉΣΜ·ΥΌ¬ ΔήΫΪΩιΉ¥ΟΚΖέΥιΘ§ΧαΗΏΤδ»Φ…’–߬ Δί‘ΎΟΚ÷–Φ”»κ ·Μ“Κσ»Φ”ΟΔό―≠ΜΖ¥ΠάμΈϋ ’ΥΰΖ≈≥ωΒΡΈ≤Τχ
AΘ°ΔΌΔΎΔέΔήΔίΓΓΓΓΓΓΓΓ BΘ°ΔΌΔέΔίΔόΓΓΓΓΓΓΓΓ CΘ°ΔΌΔΎΔίΔόΓΓΓΓΓΓΓΓ DΘ°ΔΎΔέΔήΔό
4Θ°≤ΜΨΏ”–Ζ≈…δ–‘ΒΡΆ§ΈΜΥΊ≥Τ÷°ΈΣΈ»Ε®Ά§ΈΜΥΊΘ§Έ»Ε®Ά§ΈΜΥΊΖ÷ΈωΖ®‘ΎΫϋ20Ρξά¥÷≤Έο…ζάμ―ßΓΔ…ζΧ§―ßΚΆΜΖΨ≥ΩΤ―ß―–ΨΩ÷–ΜώΒΟΙψΖΚ”Π”ΟΓΘ»γ‘Ύ¬ΫΒΊ…ζΧ§œΒΆ≥―–ΨΩ÷–Θ§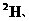
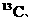
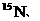
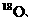
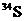 Β»≥Θ”ΟΉςΜΖΨ≥Ζ÷Έω÷Η ΨΈοΓΘœ¬Ν–”–ΙΊΥΒΖ®’ΐ»ΖΒΡ «
Β»≥Θ”ΟΉςΜΖΨ≥Ζ÷Έω÷Η ΨΈοΓΘœ¬Ν–”–ΙΊΥΒΖ®’ΐ»ΖΒΡ «
AΘ°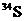 ‘≠Ή”ΚΥΡΎ÷–Ή” ΐΈΣ16
‘≠Ή”ΚΥΡΎ÷–Ή” ΐΈΣ16
BΘ°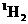
 ΚΆ
ΚΆ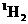
 ΒΡœύΕ‘Ζ÷Ή”÷ ΝΩ≤ΜΆ§
ΒΡœύΕ‘Ζ÷Ή”÷ ΝΩ≤ΜΆ§
CΘ°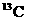 ΚΆ
ΚΆ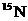 ‘≠Ή”ΚΥΡΎΒΡ÷ Ή” ΐœύ≤ν2
‘≠Ή”ΚΥΡΎΒΡ÷ Ή” ΐœύ≤ν2
DΘ°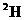 +ΒΡΫαΚœOHΘ≠ΒΡΡήΝΠ±»
+ΒΡΫαΚœOHΘ≠ΒΡΡήΝΠ±» +ΒΡΗϋ«Ω
+ΒΡΗϋ«Ω
3Θ°ΗυΨίœ¬±μ÷–Ν–≥ωΒΡ ΐΨίΘ§≈–Εœœ¬Ν–»»Μ·―ßΖΫ≥Χ Ϋ ι–¥≤Μ’ΐ»ΖΒΡ «
|
Μ·ΓΓ
―ßΓΓ
Φϋ |
HΘ≠H |
ClΘ≠Cl |
HΘ≠Cl |
|
…ζ≥…1molΜ·―ßΦϋ ±Ζ≈≥ωΒΡΡήΝΩ |
436kJΓΛmolΘ≠1 |
243kJΓΛmolΘ≠1 |
431kJΓΛmolΘ≠1 |
AΘ°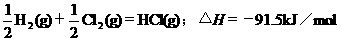
BΘ°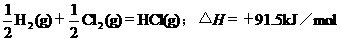
CΘ°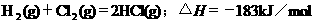
DΘ°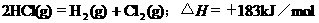
2Θ°…ηNA±μ ΨΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ÷ΒΘ§œ¬Ν––π ω÷–’ΐ»ΖΒΡ «
AΘ°100g98%ΒΡ≈®ΝρΥα÷–Κ§―θ‘≠Ή”Ηω ΐΈΣ4NA
BΘ°1mol ±ΫΖ÷Ή”÷–Κ§”–ΧΦΧΦΥΪΦϋ ΐ‘ΦΈΣ3ΓΝ6.20ΓΝ1023
CΘ°±ξΉΦΉ¥Ωωœ¬Θ§22.4LCH4ΚΆCH3ClΒΡΜλΚœΈοΥυΚ§”–ΒΡΖ÷Ή” ΐΡΩΈΣNA
DΘ°60gSiO2ΨßΧε÷–Κ§SiO2Ζ÷Ή” ΐ‘ΦΈΣ6.02ΓΝ1023
1Θ°Ζ¥”ΠE+F===G‘ΎΈ¬Ε»T1œ¬Ϋχ––Θ§Ζ¥”ΠM+N===K‘ΎΈ¬Ε»T2œ¬Ϋχ––Θ§“―÷ΣT1>T2Θ§«“EΚΆFΒΡ≈®Ε»Ψυ¥σ”ΎMΚΆNΒΡ≈®Ε»(ΤδΥϊΧθΦΰΨυœύΆ§)Θ§‘ρΝΫ’ΏΒΡΖ¥”ΠΥΌ¬
AΘ°«Α’Ώ¥σΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°Κσ’Ώ¥σΓΓΓΓΓΓΓΓΓΓΓΓ CΘ°“Μ―υ¥σΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°ΈόΖ®≈–Εœ
45ΓΔΆ≠Φ»Ρή”κœΓœθΥαΖ¥”ΠΘ§“≤Ρή”κ≈®œθΥαΖ¥”ΠΘ§Β±Ά≠”κ“ΜΕ®≈®Ε»œθΥαΖ¥”Π ±Θ§Ω…ΫΪΖΫ≥Χ Ϋ±μ ΨΈΣ:Cu+HNO3=Cu(NO3)2+NOΓϋ+NO2Γϋ+H2OΓΘ
(1) œθΥα‘ΎΗΟΖ¥”Π÷–ΒΡΉς”Ο «ΓΓΓΓΓΓΓΓ Θ§ΗΟΖ¥”ΠΒΡΜΙ‘≠≤ζΈο «ΓΓ ΓΓΓΓΓΓΓΓΓΘ
(2) 0.3mol Cu±ΜœθΥαΆξ»Ϊ»ήΫβΚσΘ§Cu ß»ΞΒΡΒγΉ” ΐ «ΓΓΓΓΓΓ Θ§»γΙϊΒΟΒΫΒΡ
NOΚΆNO2Έο÷ ΒΡΝΩœύΆ§Θ§‘ρ≤ΈΦ”Ζ¥”ΠΒΡœθΥαΒΡΈο÷ ΒΡΝΩ «ΓΓΓΓΓΓΓΓ Θ§
»τ”Ο≈≈Υ°Ζ® ’Φ·’β–©ΤχΧεΘ§Ω…ΒΟ±ξΉΦΉ¥Ωωœ¬ΒΡΤχΧεΧεΜΐΓΓΓΓΓΓ ΓΘ
(3) »γΙϊ≤ΈΦ”Ζ¥”ΠΒΡCuΚΆHNO3ΒΡΈο÷ ΒΡΝΩ÷°±» «3:10Θ§–¥≥ω≤Δ≈δΤΫΗΟΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ Ϋ_______________________________________________ΓΘ
(4) »γΙϊΟΜ”–Ε‘ΗΟΖ¥”Π÷–ΒΡΡ≥–©Έο÷ ΒΡ±»άΐΉςœόΕ®Θ§‘ρΖΫ≥Χ ΫΩ…ΡήΒΡ≈δΤΫœΒ ΐ”––μΕύΉιΓΘ‘≠“ρ «_____________________________________ΓΘ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com