
题目列表(包括答案和解析)
6.亚硝酸盐中毒,又名乌嘴病、紫绀病、肠源性青紫病。亚硝酸盐可将正常的血红蛋白氧化成高铁血红蛋白,血红蛋白中的铁元素由二价变为三价,失去携氧能力,使组织出现缺氧现象。美蓝是亚硝酸盐中毒的有效解毒剂。下列说法不正确的是
A.在中毒过程中血红蛋白被氧化 B.中毒时亚硝酸盐发生氧化反应
C.药品美蓝应具有还原性 D.解毒时血红蛋白被还原
5.把10mL淀粉胶体和5mLNaCl溶液的混合液体,加入用半透膜制成的袋内,将此袋浸入盛蒸馏水的烧杯中(如右图)。2min后,分别取袋内和烧杯中的液体进行实验。
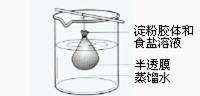 下列有关说法正确的是
下列有关说法正确的是
A.如果将AgNO3 溶液加入袋内液体中,产生白色沉淀,
则说明Cl-不能通过半透膜
B.如果Cl-能通过半透膜,则AgNO3 溶液加入袋内液体
中,将不产生白色沉淀
C.如果将少量碘水加入袋内液体中,溶液变蓝色,则说明淀粉分子不能通过半透膜
D.如果将少量碘水加入烧杯中液体,溶液不变蓝色,则说明淀粉分子不能通过半透膜
4.我国稀土矿资源丰富,品位甚高。提取稀土元素可以向含RE(RE表示稀土元素)的硫酸盐溶液中加入粉状Na2SO4,使稀土元素转入沉淀。有关的反应为:
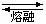 RE2(SO4)3+Na2SO4+xH2O RE2(SO4)3·Na2SO4·xH2O↓。下列叙述不正确的是
RE2(SO4)3+Na2SO4+xH2O RE2(SO4)3·Na2SO4·xH2O↓。下列叙述不正确的是
A.该反应属于化合反应 B.该反应属于可逆反应
C.生成的产物在分类上属于复盐 D.RE在化合物中的化合价为+3
3.下列各项中表达正确的是
A.F原子结构示意图: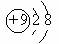 B.CO2的分子模型:
B.CO2的分子模型:
C.HCl的电子式为: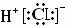 D.NH3的结构式:
D.NH3的结构式: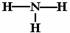
2.教材是学习的重要材料,但不能迷信教材。下列是中学化学教材中摘录的部分表述内容,根据你所学的化学知识判断,其中不够科学严密的是
A.第三册教材P20:除了加入电解质可使某些胶体聚沉外,将两种带相反电荷的胶体混合,也能发生聚沉。
B.第一册教材P17:离子方程式不仅可以表示一定物质间的某个反应,而且可以表示所有同一类型的离子反应。
C.第一册教材P101:元素性质的周期性变化是元素原子的核外电子排布的周期性变化的必然结果。
D.第二册教材P34:不同的化学反应,具有不同的反应速率,这说明,参加反应的物质的性质是决定化学反应速率的重要因素。
1.1934年居里夫妇用α粒子(4He)轰击27Al得到一种自然界不存在的核素-30P,开创了人造核素的先河。其发生的变化可表示如下:27Al+4He→30P+1n。下列有关说法不正确的是
A.30P和 31P 两种核素互为同位素
B.该变化同样遵循质量守恒定律
C.该变化说明原子核在化学反应中也能发生变化
D.在30P中存在:质子数=中子数=核外电子数
25.下图为某市售盐酸试剂瓶标签上的部分数据。
(1)配制200mL0.100 m01.L-1盐酸需该浓盐酸多少毫升?(保留两位
小数)
(2)取等物质的量浓度NaOH溶液两份A和B各10 mL,分别向其
通入不等量的C02,再继续向两溶液中逐滴加入上述配好的0.100
m01.L-1的盐酸,标准状况下产生C02气体体积与所加的盐酸关系如
图所示,,求:
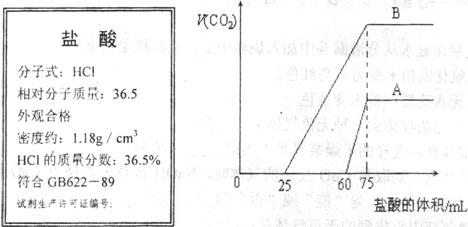
① 原NaOH溶液的物质的量浓度?
② B溶液中通入C02后所含溶质的物质的量之比?
24.(16分)已知碳碳双键的碳原子上连有羟基的结构是不稳定的结构。A是一种直链一溴代物,1mol A与2mol H2反应生成1mol G,F是环状化合物,环上有5个原子,其化学式为C4H6O2。请根据下面的反应路线回答问题:
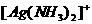 、
、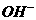 NaOH溶液、
NaOH溶液、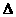
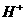 H2、Ni、
H2、Ni、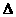 浓H2SO4、
浓H2SO4、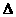
 F
F
① ② ③ ④ ⑤
(1)化合物F的结构简式是____________,化合物C的结构简式是____________。
(2)化合物A含有的官能团是________________________。
(3)G的结构简式是____________________________________。
(4)写出D在一定条件下发生加聚反应的化学方程式是________________________
________________________________________________。
23.(12分)某化学实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
(I)制取氧化铜
(1)称取2gCuSO4 5H2O在 (填仪器)中研细后倒入烧杯,加10mL蒸馏水溶解。
(2)向上述CuSO4溶液中逐滴加入NaOH溶液,立即产生蓝色沉淀,继续滴加,直到不再产生沉淀。然后将所得混合物转移到 (填仪器)中,加热至沉淀全部变为黑色,停止加热。
(3)将步骤(2)所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题: ‘
①完成上面的空白。
②上述实验步骤中需要使用玻璃棒的是 (填实验序号)。
③步骤(3)中洗涤沉淀的操作是
.
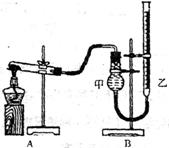
(Ⅱ)该小组同学从资料中得知氧化铜也能催化分解氯酸钾。他们为了比较氧化铜和氧化锰的催化效果,设计用右图装置进行实验,实验时均以生成25mL气体为准。其它可能影响实验的因素均已控制,相关数据见下表:
|
实验序号 |
KCl03质量 |
其它物质质量 |
待测数据 |
|
(4) |
I,2g |
无其他物质 |
|
|
(5) |
1.2g |
CuO 0.5g |
|
|
(6) |
1.2g |
Mn02 O.5g |
|
回答下列问题.
④上述实验中的待测数据指
⑤若(5)(6)中待测数据分别为10和7(单位相同),则 (填写化学式)催化效果好。
⑥为探究CuO在实验(5)中是否起催化作用,需补做如下实验(无需写出具体操作):
a ,b验证CuO的化学性质没有改变。
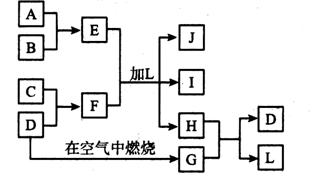
22.如图所示,图每一方框中的字母代表一种反应物或生成物,产物J是含A元素的白色胶状沉淀,I为NaCl溶液,D是淡黄色固体单质。试填写下列空白:
(1)L的化学式为 F的化学式为
(2)写出A+B→E反应的化学方程式
(3) H和G之间反应的化学方程式
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com