
题目列表(包括答案和解析)
7.设NA表示阿伏加德罗常数的值,下列说法中不正确的是
A.如果5.6L N2含有n个氮分子,则阿伏加德罗常数一定约为4n
B.15.6g Na2O2与过量CO2反应时,转移的电子数为0.2 NA
C.在一定条件下,6.4g SO2与足量O2反应生成SO3的分子数为0.1NA
D.T℃时,1 L pH=6纯水中,含10-6NA个OH-
6.2004年,美国科学家通过"勇气"号太空车探测出火星大气中含有一种称为硫化羰(化学式为COS)的物质。已知硫化羰分子中所有原子最外层均满足8电子结构。下列说法正确的是
A.硫化羰是酸性氧化物 B.硫化羰结构式为S=C=O
C.硫化羰属于非极性分子 D.硫化羰为分子晶体,沸点比CO2低
27.(8分)已知在25℃的水溶液中,AgX、AgY、AgZ均难溶于水,且Ksp(AgX)== 1.8×10-10,Ksp(AgY)== 1.0×10-12,Ksp(AgZ)== 8.7×10-17;
(1)根据以上信息,判断AgX、AgY、AgZ三者的溶解度(已被溶解的溶质的物质的量/1L溶液 表示)S(AgX)、S(AgY)、S(AgZ)的大小顺序为:
(2)若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-)
(填“增大”、“减小”或“不变”)。
(3)在25℃时,若取0.188g的AgY(相对分子质量188)固体放入100mL水中(忽略溶液体积的变化),则溶液中Y-的物质的量浓度为
(4)由上述Ksp判断,在上述(3)的体系中,能否实现AgY向AgZ的转化,并简述理由:
26.(10分)
恒温下,将amolN2与bmolH2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g) 2NH3(g)
2NH3(g)
⑴若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则a的值为 。
⑵反应达平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的含量(体积分数)为25%。则平衡时NH3的物质的量为 。
⑶原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),
n(始):n(平)= 。
⑷原混合气体中,a:b= 。
⑸达到平衡时,N2和H2的转化率之比,α(N2):α(H2)= 。
25.(14分)已知: CH3-CH=CH2 + HBr → CH3-CHBr-CH3
1mol某烃A充分燃烧后可以得到8 mol CO2和4 mol H2O。该烃A 在不同条件下能发生下图所示的一系列变化。
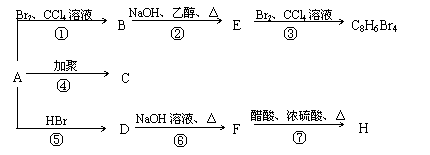
(1)A的化学式: A的结构简式:
(2)上述反应中,①是 反应,⑦是 反应。(填反应类别)
(3)写出C、D、E、H物质的结构简式:
C , D ,
E , H 。
(4)写出D → F反应的化学方程式
24、(7分)某有机化合物A含碳77.8%,氢为7.40%,其余为氧,A的相对分子质量为甲烷的6.75倍。
(1)该有机物的分子式为
(2)据此确定该有机物含苯环的所有可能的结构简式。
23.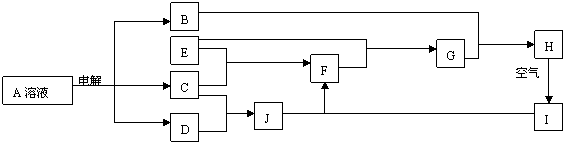 (16分)A、B、C、D、E、F、G、H、I、J均为中学化学中常见物质,其相互转化的关系如下所示:已知,A的焰色反应呈黄色,I是一种红褐色沉淀。
(16分)A、B、C、D、E、F、G、H、I、J均为中学化学中常见物质,其相互转化的关系如下所示:已知,A的焰色反应呈黄色,I是一种红褐色沉淀。
⑴写出下列物质的化学式:B:NaOH ;E:Fe ;D: H ;H: Fe(OH) 。
⑵常温下C是黄绿色气体:
①写出A的电极反应方程式:阴极: 2H++2e-=H↑(或2HO+2e-=H↑+2OH-) ;
阳极: 2Br--2e -=Br ;
②写出H→I的化学方程式:4Fe(OH)+O+2HO=4Fe(OH) ↓;
③G与足量Cl2反应的离子方程式:2Fe2++4Br-+3Cl=2Fe3++2Br+6Cl- 。
22.(8分) A、B、C、D、E都是短周期元素,原子序数依次增大,B、C同周期,A、D同主族。A、B能形成两种常温下为液态化合物甲和乙,原子个数比分别为2∶1和1∶1。E自然界中含量最多的金属元素。
根据以上信息回答下列问题:
(1)甲、乙两分子中含有非极性共价键的物质的结构式是______________________,
C元素在周期表中的位置是__________________。
(2)C和D的离子中,半径较小的是__________(填离子符号)。
 (3)C、D、E可组成离子化合物DxEC6,其晶胞结构如下图所示,阳离子D+位于正方体的棱的中点和正方体内部;阴离子EC6x-位于该正方体的顶点和面心。该化合物的化学式是____________。
(3)C、D、E可组成离子化合物DxEC6,其晶胞结构如下图所示,阳离子D+位于正方体的棱的中点和正方体内部;阴离子EC6x-位于该正方体的顶点和面心。该化合物的化学式是____________。
(六)问题讨论:
(1)滴定时能否剧烈摇动锥形瓶?为什么?
(2)从分析数据看,此软包装橙汁是否是纯天然橙汁?_______(填“是”或“不是”或“可能是”)。制造商最可能采取的做法是__________(填编号):
A.加水稀释天然橙汁 B.橙汁已被浓缩 C.将维生素C作为添加剂
(五)数据记录与处理(请在下面设计并画出数据记录和数据处理的表格,不必填数据)。
若经数据处理,滴定中消耗标准碘溶液的体积是15.00mL,则此橙汁中维生素C的含量是____________mg/L。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com