
题目列表(包括答案和解析)
20.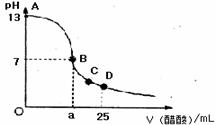 在25mL0.1mol/LNaOH溶液中逐滴加入0.2mol/L醋酸溶液,曲线如下图所示,有关粒子浓度关系比较正确的
在25mL0.1mol/LNaOH溶液中逐滴加入0.2mol/L醋酸溶液,曲线如下图所示,有关粒子浓度关系比较正确的
A.在A、B间任一点,溶液中一定都有
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.在B点,a>12.5,且有
c(Na+)==c(CH3COO-)=c(OH-)==c(H+)
C.在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D.在D点:c(CH3COO-)十c(CH3COOH)==2c(Na+)
19.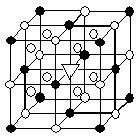 冰晶石(化学式为Na3AlF6)的结构单元如右图所示,已知冰晶石熔融时电离方程式为Na3AlF6
=3Na+ + AlF6-
冰晶石(化学式为Na3AlF6)的结构单元如右图所示,已知冰晶石熔融时电离方程式为Na3AlF6
=3Na+ + AlF6-
●位于大立方体顶点和面心
○位于大立方体的12条棱的中点和8个小立方体的体心
那么大立方体的体心处▽所代表的微粒是
A.Na+ B.Al3+
C.F- D.AlF6-
18、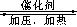
 甲醇是重要的基础化工原料又是一种新型的燃料,制取甲醇传统法是采用CuO-ZnO/γ- Al2O3催化剂,合成反应为:CO+2H2
CH3OH,工艺中一些参数
甲醇是重要的基础化工原料又是一种新型的燃料,制取甲醇传统法是采用CuO-ZnO/γ- Al2O3催化剂,合成反应为:CO+2H2
CH3OH,工艺中一些参数
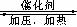 如右图;
如右图;
目前正在开发的新法是:2CH4+ O2 2CH3OH 。
下列关于新法和旧法的说法正确的是
 A.旧法生产中,由图知CO与H2合成甲醇的反应属于放热反应
A.旧法生产中,由图知CO与H2合成甲醇的反应属于放热反应
B.旧法生产中,选择合适催化剂时,可推测高压法合成比低压法合成更有发展优势。
C.新法与旧法相比,原料丰富并可直接从天然气中获得
D.新法生产中,需控制V(CH4)/V(O2)=9∶1,目的是提高空气中氧气的转化率
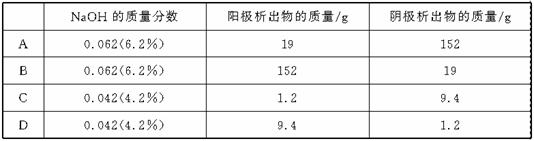
17.将质量分数为0.052(5.2%)的NaOH溶液1 L(密度为1.06 g·cm-3)用铂电极电解,当溶液中NaOH的质量分数改变了0.010(1.0%)时停止电解,则此时溶液中应符合的关系是
16.1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子。如下图分子,因其形状像东方塔式庙宇(pagoda-style temple),所以该分子也就称为pagodane(庙宇烷),有关该分子的说法正确的是
A.一氯代物的同分异构体只有三种
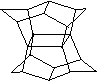 B.分子中含有二个亚甲基(-CH2-)
B.分子中含有二个亚甲基(-CH2-)
C.分子中含有4个五元碳环
D.分子式为C20H20
15.化合物A、B、C、D各由两种元素组成,甲、乙、丙是三种单质。这些常见的化合物与单质之间存在如下关系(已知化合物C是一种有机物),
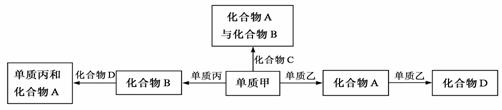
以下结论不正确的是
A.上图所示的五个转化关系中,有三个是化合反应
B.上述转化关系所涉及的化合物中有一种是电解质
C.甲、乙、丙三种单质的晶体均是分子晶体
D.上图所示的五个转化关系中,均为放热反应
14.下表中,对陈述I、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是
|
选项 |
陈述I |
陈述Ⅱ |
判断 |
|
A |
工业生产硫酸用水吸收SO3 |
SO3可与水反应 |
I对;Ⅱ对;有 |
|
B |
Cl2和SO2混合后可用于漂白纸浆 |
Cl2和SO2都有较好的漂白作用 |
I对;Ⅱ错;无 |
|
C |
金属钠具有强还原性 |
高压钠灯发出透雾性强的光 |
I对;Ⅱ对;无 |
|
D |
石墨常用作电解池的电极 |
石墨的化学性质稳定且导电性好 |
I对;Ⅱ对;有 |
13.相互反应时,无论何种试剂过量离子方程式都正确的是
 A.盐酸与NaAlO2溶液:
A.盐酸与NaAlO2溶液: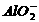 +H++H2O
Al(OH)3↓
+H++H2O
Al(OH)3↓
 B.石灰水与磷酸二氢钠溶液:2H2PO
B.石灰水与磷酸二氢钠溶液:2H2PO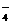 +3Ca2++4OH- Ca3(PO4)2↓+4H2O
+3Ca2++4OH- Ca3(PO4)2↓+4H2O
 C.明矾溶液与小苏打:Al3++3HCO
C.明矾溶液与小苏打:Al3++3HCO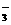 Al(OH)3+3CO2↑
Al(OH)3+3CO2↑
 D.硫酸氢钠溶液和氢氧化钡:SO
D.硫酸氢钠溶液和氢氧化钡:SO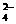 + 2H+ +Ba2+ + 2OH- BaSO4↓
+ 2H2O
+ 2H+ +Ba2+ + 2OH- BaSO4↓
+ 2H2O
12.对于平衡体系mA(g)+nB(g) pC(g)+qD(g);△H<0。下列结论中正确的是
pC(g)+qD(g);△H<0。下列结论中正确的是
A.该反应的化学平衡常数表达式为:K = 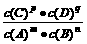
B.若温度不变,将容器的体积增大1倍,此时A的浓度变为原来的0.45倍,则m+n>p+q
C.若m+n=p+q,则往含有a mol气体的平衡体系中再加入b mol B,达到新平衡时,气体的总物质的量等于(a+b)mol
D.若升高温度时,平衡混合气体的平均相对分子质量增大,则m+n>p+q
11.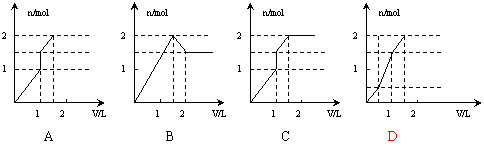 向含1mol HCl和1mol
MgSO4的混合溶液中加入1mol·L-1的Ba(OH)2溶液,产生沉淀的物质的量(n)与加入Ba(OH)2溶液体积(V)间的关系图正确的是
向含1mol HCl和1mol
MgSO4的混合溶液中加入1mol·L-1的Ba(OH)2溶液,产生沉淀的物质的量(n)与加入Ba(OH)2溶液体积(V)间的关系图正确的是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com