
题目列表(包括答案和解析)
17.(11分)(1) 下列有关实验操作或判断不正确的是 _________(填有关序号,选错倒扣分)。
A.用10 mL量筒量取稀硫酸溶液 8.0 mL
B.用干燥的pH试纸测定氯水的pH
C.用碱式滴定管量取KMnO4溶液 19.60 mL
D.使用容量瓶配制溶液时,俯视液面定容后所得溶液的浓度偏大
E.圆底烧瓶、锥形瓶、蒸发皿加热时都应垫在石棉网上
F.测定硫酸铜晶体中结晶水含量时,将加热后的坩埚置于干燥器中冷却后再称量
 G.用冰醋酸,蒸馏水和容量瓶等仪器配制pH为1的醋酸稀溶液
G.用冰醋酸,蒸馏水和容量瓶等仪器配制pH为1的醋酸稀溶液
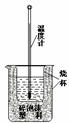
(2)实验室利用如右图装置进行中和热的测定。
回答下列问题:
①该图中有两处未画出,它们是 、 ;
②如果用0.5 mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将 (填“偏大”、“偏小”或“不变”);原因是 。
(3)在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度。在H2SO4溶液中,反应如下:
2MnO4-+5C2O42-+16H+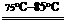 2Mn2++10CO2↑+8H2O
2Mn2++10CO2↑+8H2O
 ①用托盘天平称取W g Na2C2O4晶体。
①用托盘天平称取W g Na2C2O4晶体。
②将W g Na2C2O4配成100 mL标准溶液,移取20.00 mL置于锥形瓶中,则酸性KMnO4溶液应装在________(填“酸式”或“碱式”)滴定管中。
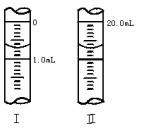
③若滴定管的起始读数和终点读数如右图所示,则酸性KMnO4的物质的量浓度为________ (填表达式)。
④若滴定完毕立即读数,测定的KMnO4溶液的浓度________(填“偏高”“偏低”或“不变”)。
16.经测定某溶液中只含NH4+、Cl-、H+、OH-四种离子,下列说法错误的是
A.溶液中四种粒子之间不可能满足:c(Cl-)>c(H+)>c(NH4+)>c(OH-)
B.若溶液呈酸性,则一定满足:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
C.若溶液呈碱性,则一定满足:c(NH4+)>c(Cl-)
D.若溶液呈中性,则一定满足:c(NH4+)= c(Cl-)
第二卷 (共86分)
15.在pH为4-5的环境中,Cu2+、Fe2+不生成沉淀,而Fe3+几乎完全沉淀。工业上制CuCl2是将浓盐酸用蒸汽加热到80℃左右,再慢慢加入粗氧化铜(含杂质FeO),充分搅拌使之溶解。欲除去溶液中的杂质离子,下述方法正确的是
A.加入纯Cu将Fe2+还原 B.向溶液中加入(NH4)2S使Fe2+沉淀
C.直接加水加热使杂质离子水解除去
D.在溶液中通入Cl2,再加入CuO粉末调节pH为4-5
14.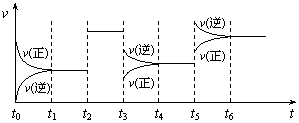 某密闭容器中发生如下反应:X(g)+3Y(g)
某密闭容器中发生如下反应:X(g)+3Y(g) 2Z(g);ΔH<0右图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
2Z(g);ΔH<0右图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
A.t2时加入了催化剂 B.t3时降低了温度
C.t5时增大了压强 D.t4-t5时间内转化率最低
13.对于平衡体系:aA(g)+bB(g)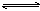 cC(g)+dD(g);正反应放热,有下列判断,其中正确的是:
cC(g)+dD(g);正反应放热,有下列判断,其中正确的是:
A.若温度不变,容器体积扩大一倍,此时A的浓度是原来的0.48倍,则a+b大于c+d
B.若从正反应开始,平衡时,A、B的转化率相等,则A、B的物质的量之比为a:b
C.若平衡体系中共有气体M mol,再向其中充入bmolB,达到平衡时气体总物质的量为M+bmol,则a+b=c+d
D.若a+b=c+d ,则当容器内温度上升时,平衡向左移动,容器中气体的压强不变。
12.X、Y、Z、W为四种短周期主族元素。其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6。下列说法正确的是
A.Y元素最高价氧化物对应水化物的化学式为H2YO4
B.原子半径由小到大的顺序为:W<X<Y<Z
C.X与W可以形成W2X、W2X2两种氧化物
D.Y、Z两元素的气态氢化物中,Z的气态氢化物最稳定
11.在一定温度下,向饱和的氢氧化钠溶液中加入少量的过氧化钠,充分反应后,恢复到原来温度,下列说法正确的是
A.溶液中Na+浓度增大,有O2放出 B.溶液pH不变,有O2放出
C.溶液中Na+数目减少,有O2放出 D.溶液中Na+数目不变,有O2放出
10.下列反应的离子方程式正确的是
A.苯酚钠溶液中通入少量CO2:2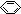 -O-+CO2+H2O→2
-O-+CO2+H2O→2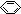 -OH+CO32-
-OH+CO32-
B.FeSO4的酸性溶液中加H2O2:2Fe2++H2O2+2H+=2Fe3++2H2O
C.用氨水吸收少量的SO2:NH3·H2O+SO2=NH4++HSO3-
D.碳酸氢钠溶液中加入过量石灰水HCO3-+OH-=CO32-+H2O
9.常温下,下列各组离子在指定环境下能大量共存的是
A.pH=l的溶液中:Na+、K+、SO32-、MnO4-
B.pH=7的溶液中:Na+、A13+、Cl-、SO42-
C.pH>12的溶液中:Na+、K+、SO42-、AlO2-
D.pH=0的溶液中:Na+、K+、NO3-、ClO-
8.常温下单质硫主要以S8形式存在。加热时,S8会转化为S6、S4、S2等。当温度达到750℃时,硫蒸汽主要以S2形式存在(占92%)。下列说法正确的是
A.S8转化为S6、S4、S2属于物理变化 B.不论哪种硫分子,完全燃烧都生成SO2
C.常温条件下单质硫为原子晶体 D.把硫单质在空气种加热到750℃即得S2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com