
题目列表(包括答案和解析)
5.下列实验能达到预期目的的是
.... ①用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸
.... ②将Cl2的制备和性质实验联合进行以减少实验中的空气污染
.... ③用食醋和澄清石灰水验证蛋壳中含有碳酸盐
.... ④用硝酸钡溶液鉴别硫酸根离子与亚硫酸根离子
.... ⑤用溴水检验汽油中是否含有不饱和脂肪烃
A.①②③ B.①③④ C.②③⑤ D.②④⑤
4.下列说法正确的是
A.用乙醇或CCl4可提取碘水中的碘单质
B.NaCl和SiC晶体熔化时,克服粒子间作用力的类型相同
C.24Mg32S晶体中电子总数与中子总数之比为1∶1
D.H2S和SiF4分子中各原子最外层都满足8电子结构
3.已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化:
H2O2 → H2O IO3- → I2 MnO4- → Mn2+ HNO3 → NO
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是
A.H2O2 B.IO3- C.MnO4- D.HNO3
2.根据相关化学原理,下列判断正确的是
A.若X是原子晶体,Y是分子晶体,则熔点:X < Y
B.若A2 + 2D- → 2A- + D2,则氧化性:D2 > A2
C.若R2-和M+的电子层结构相同,则原子序数:R > M
D.若弱酸HA的酸性强于弱酸HB,则同浓度钠盐溶液的pH:NaA < NaB
1.2006年9月28日,中国科学家研制的“人造太阳”成功地进行了一次放电。所谓“人造太阳”是指受控核聚变。从1 L海水中提取出来的氘(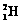 )受控核聚变成氦(
)受控核聚变成氦(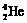 )时产生的能量相当于300 L汽油燃烧放出的能量。因此这种技术对解决能源问题有着十分广阔的发展前景。下列有关说法正确的是
)时产生的能量相当于300 L汽油燃烧放出的能量。因此这种技术对解决能源问题有着十分广阔的发展前景。下列有关说法正确的是
A.氘(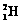 )受控核聚变成氦(
)受控核聚变成氦(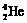 )是一种化学变化
)是一种化学变化
B.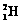 和
和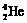 互为同位素
互为同位素
C.符号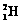 中的“2”与符号
中的“2”与符号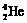 中的“2”意义不同
中的“2”意义不同
D.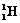 2和
2和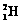 2的物理性质、化学性质都存在着很大的差异
2的物理性质、化学性质都存在着很大的差异
26.(12分)在一定温度下将2molA和2molB两种气体混合于2L密闭容器中,发生如下反应:
3A(g)+B(g)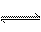 2C(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8mol D,请填写下面空白。
2C(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8mol D,请填写下面空白。
(1)B的平衡浓度为 。
(2)A的转化率为 。
(3)用D表示的平均反应速率为 。
(4)如果缩小容器容积(温度不变),则平衡体系中混合气体的密度、平均相对分子质量__________、__________。(两空均填“增大、“减少”或“不变” )
(5)如果上述反应在相同条件下从逆反应开始进行,开始加C和D各4/3 mol,要使平衡时各物质的质量分数与原平衡相等,则还应加入 mol B物质。
25、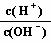 (4分)
(4分)
(1)常温下,将1mL pH = 1的H2SO4溶液加水稀释至100mL ,稀释后的溶液中 =
;
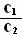 (2)常温下,pH=5的H2SO4溶液中由水电离出的H+浓度为c1;pH=5 的Al2(SO4)3溶液中由水电离出的H+ 浓度为c2,则 = ;
(2)常温下,pH=5的H2SO4溶液中由水电离出的H+浓度为c1;pH=5 的Al2(SO4)3溶液中由水电离出的H+ 浓度为c2,则 = ;
24.(12分)某校化学小组学生利用图12装置进行“氨的催化氧化及其产物验证”实验。(图中夹持装置已略去)
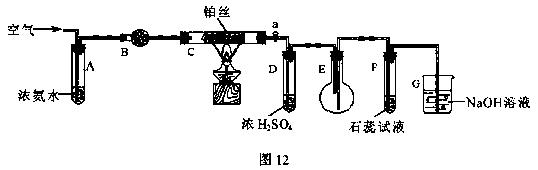 (1)装置B中盛放的试剂是__________(填名称),用来吸收混合气体中的水汽。
(1)装置B中盛放的试剂是__________(填名称),用来吸收混合气体中的水汽。
(2)反应开始时,将装置C中铂丝加热到红热,撤去酒精灯,铂丝变暗。此时鼓入空气,铂丝又变红热。这是因为氨的催化氧化是_________反应。
(3)实验过程中,装置D中的导管容易生成无色晶体而堵塞。为了解决该问题,可以在活塞a后增加______(选填序号)。
①盛有蒸馏水的洗气瓶 ②盛有浓盐酸的洗气瓶 ③盛有碱石灰的U形管
(4)反应一段时间后,装置E中的气体颜色应为 色。此时,装置E中的含氮化合物有NH3、NO、NO2、___________(填化学式)。
(5)反应一段时间后,装置F中的紫色石蕊试液变红,其原因是(写出化学方程式)__________________________________________________。
(6)实验结束时,应__________________________,并停止鼓入空气。
(7)工业上合成氨的反应是:N2(g)+3H2(g)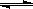 2NH3(g);△H= -92.2kJ·mol-1。
2NH3(g);△H= -92.2kJ·mol-1。
①下列做法能够提高工业合成氨转化率的是_________(选填字母)
a.增大压强 b.升高温度
c.使用铁触媒 d.将生成的NH3及时从混合气体中分离出去
②工业合成氨时采用500℃左右的温度,主要是因为:
____________________________________________________________ 。
23.(8分)如下图所示的装置,C、D、E、F、X、Y都是惰性电极。
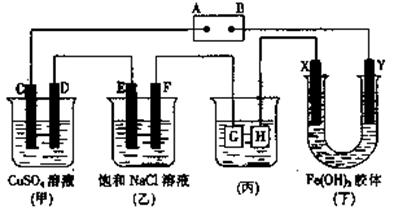
将电源接通后,向乙中滴入酚酞液,在F极附近显红色。试回答以下问题:
(1)电源A极的名称是_______。
(2)甲装置中电解反应的总反应离子方程式是:____________________________________ 。
(3)如果收集乙装置中产生的气体,两种气体的体积比是______________。
(4)欲用丙装置给铜镀一层银,G应该是_______(填“铜”或“银”),电镀液的主要成分是________________(填化学式)。
(5)装置丁中的现象是_________________________________ _____,
说明___________________________________ 。
22.(12分)甲、乙、丙、丁、戊分别是Na2SO4、Ba(NO3)2、HNO3、BaCl2、NaOH五种溶液中的一种,现利用X溶液鉴别它们,已知气体B的密度在同温同压下是氢气密度的22倍。试根据下图中的转化关系回答问题:

(1)下列物质的化学式分别为:
甲 、 乙 、丙 、丁 、X ;
(2)白色沉淀A与乙反应的离子方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com