
题目列表(包括答案和解析)
24.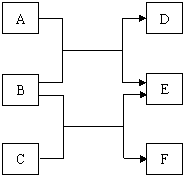 (9分)A、B、C、D、E、F六种中学化学中常
(9分)A、B、C、D、E、F六种中学化学中常
见的物质,有如下转化关系。
(1)若A、C、E皆为氧化物,且E为有毒气体,
B、D、F皆为非金属单质,且D为气体。则:A的结
构式为___________,单质F的晶体类型为________。
1molC中含有___________个共价键。
(2)若A、C、E皆为氢化物,三者皆为极性分子,其中C的相对分子质量最小;D、E、F皆为氧化物,其中D、F为有毒气体。则:
①A、C、E沸点从高到低的顺序为_______________________(填化学式);A、C、E三种气态氢化物稳定性最强的是__________ (填化学式)。
②B跟C反应生成E和F的化学方程式为______________________________________。
③A跟D常温下反应可生成一种单质,化学方程式为____________________________。
23.(14分)A、B、C、D、E分别为周期表中前20号的五种元素。已知它们都不是稀有气体元素,且原子半径依次减小,其中A、E同族,A与C、B与E原子的电子层数都相差2,A、B原子最外层电子数之比为1∶4。
(1)写出元素名称:B_________;D_________;E_________。
(2)A与C、C与E均能以原子数1∶1形成化合物,其中A、C形成化合物的化学式为______________,C与E形成的化合物电子式为________________。
(3)写出二个由上述元素组成的单质及化合物间能发生置换反应的化学方程式。
_________________________________________________________________;
_________________________________________________________________。
22.(9分)下表由元素周期表的前三周期去掉副族上方空区域后组合而成,表中虚线处为ⅡA、ⅢA族的连接处。请用相应的化学用语回答下列问题:
|
a |
|
|
|
|
|
|
|
|
b |
 |
 |
c |
d |
e |
f |
|
|
g |
|
h |
|
|
|
|
|
 (1)h的单质能与g元素的最高价氧化物对应的水化物的溶液反应,请写出该反应的离子方程式
。
(1)h的单质能与g元素的最高价氧化物对应的水化物的溶液反应,请写出该反应的离子方程式
。
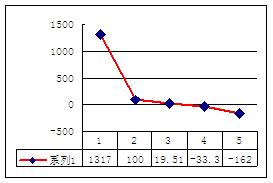
(2)第三周期8种元素按单质熔点(℃)大小顺序的柱形图(上左图,已知 柱形“1”代表Ar),则其中序列“2”代表 ,“8”代表 。(均填化学式)
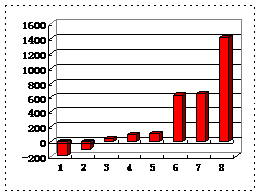
(3)b、c、d、e、f的氢化物的沸点直角坐标图(上右图),序列“5”氢化物的化学式为 ,序列“1”的氢化物的电子式: 。
(4)单质a和单质e可以设计为新型燃料电池,电解质为KOH溶液,则单质a在该燃料电池的______极发生电极反应,电极反应式为____________________________。
21.(10分)有3种可溶性离子化合物A、B、C,它们分别由阳离子NH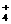 、Na+、Cu2+ 和阴离子OH-、S2-、SO
、Na+、Cu2+ 和阴离子OH-、S2-、SO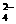 两两结合而成,取质量相等的A、B、C分别溶解于水,配成等体积的溶液,这3种溶液物质的量浓度大小的顺序是B>A>C根据题意回答下列问题:
两两结合而成,取质量相等的A、B、C分别溶解于水,配成等体积的溶液,这3种溶液物质的量浓度大小的顺序是B>A>C根据题意回答下列问题:
(1)推断出A是___________,B是___________,C是___________。
(2)室温时C溶液的pH___________7(填>、=、<=)。
(3)写出A与B溶液混合发生反应的离子方程式___________________________;
20.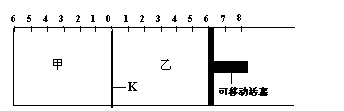 如图所示,甲、乙之间的隔板K可以左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处。在一定条件下发生可逆反应:2A(g)+B(g)
如图所示,甲、乙之间的隔板K可以左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处。在一定条件下发生可逆反应:2A(g)+B(g)
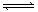 2C(g),反应达到平衡后,恢复到反应发生前时的温度。下列有关说法不正确的是……………( )
2C(g),反应达到平衡后,恢复到反应发生前时的温度。下列有关说法不正确的是……………( )
A.根据隔板K滑动与否可判断左右两边的反应是否达到平衡
B.达到平衡后,隔板K最终停留在左侧刻度0~2之间
C.到达平衡时,甲容器中C的物质的量大于乙容器中C的物质的量
D.若平衡时K停留在左侧1处,则活塞仍停留在右侧6处
第II卷(非选择题 共60分)
19.某浓度的硝酸与过量铁粉反应时生成了4.48LN2O气体(标准状况下),若改与铝反应(生成NO气体),则最后可溶解的铝的质量是……………………………………………( )
A.13.5g B.9g C.27g D.8.9g
18.某离子化合物DxEC6,晶体结构如下图所示,阳离子D+位于正方体的棱的中点和正方体内部;阴离子EC6x-位于该正方体的顶点和面心。该化合物中x 值为…………………( )

A.1 B.2 C.3 D.4
17.将0.4mol/L的盐酸与0.2mol/L的NaAlO2溶液等体积混合,其溶液中离子浓度由小到大的排列顺序正确的是………………………………………………………………………( )
A.c(OH-)<c(H+)<c(Na+)<c(Al3+)<c(Cl-)
B.c(OH-)<c(H+)<c(Al3+)<c(Na+)<c(Cl-)
C.c(H+)<c(OH-)<c(Na+)<c(Al3+)<c(Cl-)
D.c(H+)<c(OH-) <c(Al3+)<c(Cl-)<c(Na+)
16.下列离子方程式正确的是………………………………………………………………( )
A.澄清石灰水中滴加稀硝酸:Ca(OH)2+2H+ == Ca2++2H2O
B.向Ca(HCO3)2溶液中滴加同浓度的少量NaOH溶液:
OH-+Ca2++HCO3-==CaCO3↓+H2O
C.氢氧化铁溶于氢碘酸中:Fe(OH)3 + 3H+ == Fe3+ + 3H2O
D.在标准状况下,向10mL 0.1moL/LFeI2溶液中通入22.4mL氯气:
2Fe2++2I-+2C12 ==2Fe3++ I2+ 4C1-
15.最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳效率104倍的“超级温室气体”--全氟丙烷(C3F8),并提出用其“温室化火星”使其成为第二个地球的计划。有关全氟丙烷的说法正确的是………………………………………………………………( )
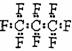 A.分子中三个碳原子可能处于同一直线上
A.分子中三个碳原子可能处于同一直线上
B.全氟冰烷的电子式为:
C.相同压强下全氟丙烷的沸点比丙烷低
D.全氟丙烷分子中既有极性键又有非极性键
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com