
题目列表(包括答案和解析)
6.如图示的装置中,把X溶液逐滴滴下与Y物质反应,若X
为浓硫酸,Y为第三周期金属元素中常温下与水难反应的单
质。Z为品红溶液。实验中观察到Z褪色。则Y为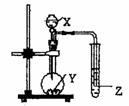
A.Na B.Mg C.Al D.Mg或Al
5.对下列反应①KHCO3溶液与石灰水反应、②明矾溶液与Ba(OH)2溶液、③Na2SO3溶液与稀盐酸反应、④Si与烧碱溶液反应,⑤Fe与稀硝酸反应,改变反应物用量,都只能能用同一个离子方程式表示的是
A.①②⑤ B.③④ C.④⑤ D ④
4.现有碳酸钠、碳酸氢钠、氢氧化钠、氯化铁和苯酚五种物质的溶液,它们之间有如图所示转化关系,图中每条线两端的物质可以发生反应,下列判断不合理的是
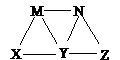 A.X一定是碳酸钠溶液
B.Y一定是氯化铁溶液
A.X一定是碳酸钠溶液
B.Y一定是氯化铁溶液
C.Z可能为碳酸氢钠溶液
D.M、N必定各为苯酚、氢氧化钠溶液中的某一种
3.美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是
A.原子半径:Na>Al B.铝钠合金若投入一定的水中可得无色溶液,则n(Al) ≤ n(Na)
C.m g不同组成的铝钠合金投入足量盐酸中,若放出H2越多,则铝的质量分数越小
D.铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀也可能有铜析出
2.用一定量的铁与足量的CuO制单质铜,有人设计了以下两种方案:
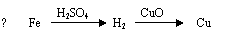
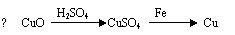
若按实验原则进行操作,则两者制得单质铜的量为A.一样多 B.①多 C.②多 D.无法判断
1.下列金属冶炼的反应原理,错误的是
|
A.2NaCl(熔融) === 2Na + Cl2↑
|
|
C.Fe3O4 + 4CO === 3Fe + 4CO2 D.2CuO === 2Cu + O2↑
7.下图表示各物质之间的相互转化关系(部分反应物或生成物未列出)。其中A、D为常见金属,J为红褐色沉淀。
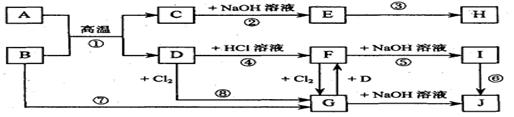
(1)A的原子结构示意图为_____________,B的化学式为_______________。
(2)反应②的离子方程式________________________________________,反应⑥的化学
方程式___________________________________________________________。
(3)在反应③中,要使E中的一种金属元素全部以沉淀的形式析出,最适宜加入的反应物
是________;若将E溶于过量盐酸,反应的离子方程式为___________________。
(4)在实验室进行反应⑧时,观察到的现象是__________________________________,
在所得产物中加入水,得浑浊液,要使其变澄清,可加入少量的_______________。
6.为测定某一铁矿石样品中的铁元素的质量分数, 取3.702g该铁矿石(铁以Fe2O3形式存在,其余物质不含铁)溶于浓热盐酸中,稀释至250mL,从中取出25mL溶液,作如下处理:加入过量的氨水,使铁以氢氧化铁的形式沉淀,将沉淀过滤,洗净并灼烧,使之完全转化为氧化铁。有关实验数据:坩埚质量:15.2861g,第一次灼烧后坩埚和固体的质量:15.6209g 第二次灼烧后坩埚和固体的质量:15.6205g,第三次灼烧后坩埚和固体的质量:15.6205g 则铁矿石中的铁元素的质量分数为
A.63.2% B.90.3% C.6.32% D.34.4%
4.将一定质量的镁、铜合金加入到稀硝酸溶液中,两者恰好完全反应,假设反应过程中还原产生全是NO,向所得溶液中加入物质的量浓度为3mol/LNaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述中正确的是
A.开始加入合金的质量不可能为6.4g
B.生成沉淀完全时消耗NaOH溶液的体积为100mL
C. 参加反应的硝酸的物质的量为0.1mol
D.溶解合金时收集到NO气体的体积为2.24L
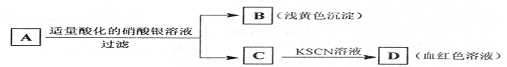 5.某学生设计了如下图中的方法对A盐进行鉴定:
5.某学生设计了如下图中的方法对A盐进行鉴定:
由此分析,下列结论中,正确的是
A.A中一定有Fe3+ B.C中一定有Fe3+
C.B为AgI沉淀 D.A一定为FeBr2溶液
3.下列各组物质相互混合反应,既有气体生成,最终又有沉淀生成的是①金属钠投入到FeCl3溶液②过量NaOH溶液和明矾溶液③少量电石投入过量NaHCO3溶液 ④Na2O2投入FeCl2溶液
A.① B.③ C.②③ D.①③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com