
题目列表(包括答案和解析)
5.下列实验装置、试剂选用或操作正确的是
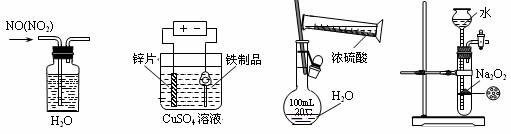
A.除去NO中的NO2 B.铁制品表面镀锌 C.稀释浓硫酸 D.制备少量O2
4.用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.常温常压下,3.6g D2O中含有的电子总数为2.0NA
B.标准状况下,11.2LC2H2和N2的混合气分子中叁键数目为0.5NA
C.常温常压下,4.6g Na在O2中燃烧消耗O2的分子数为0.05NA
D.25℃时, pH=1的CH3COOH溶液中的H+数为0.1 NA
3.在下列各组离子在一定条件下能够大量共存的是
 A.无色溶液:Cu2+、K+、MnO4-、SO42-
A.无色溶液:Cu2+、K+、MnO4-、SO42-
B.能溶解Al2O3的溶液:Na+、Ca2+、HCO3-、NO3-
C.c(OH-)=1×10-13mol·L-1的溶液:NH4+、Al3+、SO42-、Cl-
D.含0.1 mol·L-1 NO3-的溶液:H+、Fe2+、Mg2+、Br-
2.下列描述错误的是
 A.单质硅可用于制造光纤和太阳能电池
A.单质硅可用于制造光纤和太阳能电池
B.将氯气通入冷的消石灰可制得漂白粉
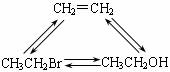
C.右图所示的三种物质间的相互转化均可一步实现
D.Na2CO3饱和溶液中持续通入CO2气体有固体析出
29. (共14分)在一容积为4 L的密闭容器中,加入0.4mol的N2和1.2mol的H2,在一定条件下,发生如下反应:
(共14分)在一容积为4 L的密闭容器中,加入0.4mol的N2和1.2mol的H2,在一定条件下,发生如下反应:
N2(g)+3H2(g) 2NH3(g )
△H<0 ,
2NH3(g )
△H<0 ,
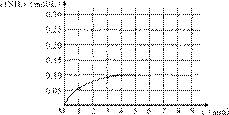
反应中NH3的物质的量浓度变化情况如右图:
(1)根据上图,计算从反应开始到平衡时,平
均反应速率v(NH3)为______mol/(L·min)。
(2)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为___________。
a. 0.20 mol/L b. 0.12 mol/L c. 0.10 mol/L d. 0.08 mol/L
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡___________________移动(填“向逆反应方向”、“向正反应方向”或“不”)。
(4)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol/L),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。
(5)在三个相同容器中各充入1 molN2和3molH2,在某一不同条件下反应并达到平衡,氨的体积分数随时间变化曲线如下图。下列说法正确的是 (填序号) 。
(A)图Ⅰ可能是不同压强对反应的影响,且P2>P1
(B)图Ⅱ可能是不同压强对反应的影响,且P1>P2
(C)图Ⅲ可能是不同温度对反应的影响,且T1>T2
(D)图Ⅱ可能是同温同压下,催化剂性能对反应的影响,且1>2
28.(共14分)某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到沉淀。
甲同学认为两者反应生成只有CuCO3一种沉淀;
乙同学认为这两者相互促进水解反应,生成Cu(OH)2一种沉淀;
丙同学认为生成CuCO3和Cu(OH)2两种沉淀。(已知:CuCO3和Cu(OH)2均不带结晶水)
Ⅰ.(1)写出Na2CO3溶液水解的离子方程式 ;
(2)在探究沉淀物成分前,须将沉淀从溶液中分离并净化。具体操作为: (填操作名称)、干燥。
Ⅱ.请用下图所示装置,选择必要的试剂,定性探究生成物的成分。
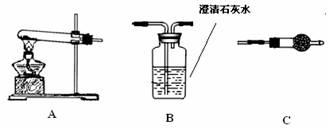

 (1)各装置连接顺序为
。
(1)各装置连接顺序为
。
(2)装置C中装有试剂的名称是 。
(3)能证明生成物中有CuCO3的实验现象是 。
Ⅲ.若CuCO3和Cu(OH)2两者都有,可通过下列所示装置的连接,进行定量分析来测定其组成。
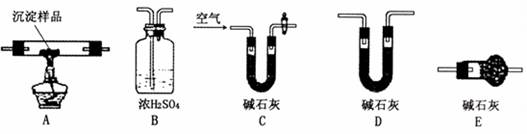
(1)装置C中碱石灰的作用是 ,实验开始时和实验结束时都要通入处理过的过量的空气,其作用分别是: 、 。
(2)若沉淀样品的质量为m g,装置B质量增加了n g,则沉淀中CuCO3的质量分数为:
×100%
27.(共16分)已知有机物A分子由C、H、O三种元素组成,其相对分子质量为120,0.1molA在足量的氧气中充分燃烧后生成0.8mol CO2 和7.2g H2O;A可以发生银镜反应,其苯环上的一卤代物有三种。
 (1)A的分子式是
,A中含氧官能团的名称是
,A的结构简式为
。
(1)A的分子式是
,A中含氧官能团的名称是
,A的结构简式为
。
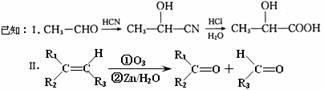
现有如下转化关系:
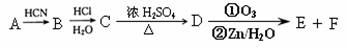
其中D能使溴的四氯化碳溶液褪色,F继续被氧化生成G,G的相对分子质量为90。
(2)C可能具有的化学性质有 (填序号)。
① 能与H2发生加成反应;② 能在碱性溶液中发生水解反应;③ 能与甲酸发生酯化反应;④ 能与Ag(NH3) 2OH溶液发生银镜反应;⑤能与氢氧化钠溶液反应
(A)①②③ (B)①③⑤ (C)①②③⑤ (D)②③④⑤
(3)① 写出C→D的化学反应方程式 ;反应类型为 ;
②在催化剂条件下,C生成高聚物的化学方程式 ;
③ G与足量NaHCO3溶液反应的化学方程式 。
(4)C的同分异构体有多种,其中符合下列要求的有机物有两种:
①属于酯类化合物;②遇三氯化铁溶液显紫色;③与新制氢氧化铜悬浊液共热可生成红色沉淀;④苯环上的一卤代物只有一种
写出其中一种有机物的结构简式 。
26.(共16分)A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件及部分产物均未列出)。
(1)若A、D、F都是短周期的非金属单质,且A、D所含元素同主族,A、F所含元素同周期,已知D单质在电子工业中有重要作用,则D的原子结构示意图为 ;物质E的结构式为 ;反应①的化学方程式为__________________。
(2)若A是常见金属单质,D是气态非金属单质,F是液态非金属单质,反应①、②都在溶液中进行,写出A在周期表中的位置 ;用电子式表示B的形成过程 ;物质C与等物质的量的Cl2在溶液中反应的离子反应方程式为 。
(3)若A、D为常见金属单质,A、D分别与F的浓溶液在加热条件下才能发生反应, 写出反应④的化学方程式 ;足量的A与溶液B充分反应后,生成物C中金属阳离子的检验方法为 ;若以惰性电极电解B的水溶液,当阴极增重3.2g时,阳极生成气体的体积在标准状况下为 L。
13.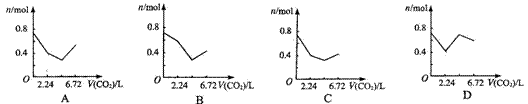 向含有0.2 mol氢氧化钠和0.1 mol氢氧化钙的溶液中,持续稳定地通入二氧化碳气体,通入气体为6.72 L(标准状况)时,立即停止,则这一过程中,溶液中离子数目与通入二氧化碳气体体积的关系正确的是( )(不考虑气体的溶解
向含有0.2 mol氢氧化钠和0.1 mol氢氧化钙的溶液中,持续稳定地通入二氧化碳气体,通入气体为6.72 L(标准状况)时,立即停止,则这一过程中,溶液中离子数目与通入二氧化碳气体体积的关系正确的是( )(不考虑气体的溶解
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com