
题目列表(包括答案和解析)
8.下列说法不正确的是
A.NaCl和SiO2晶体熔化时,克服粒子间作用力的类型不相同
B.将烧黑的铜丝伸入酒精灯火焰的焰心又变红色光亮
C.氯化亚铁溶液长期敞放于空气中会因被氧化而呈黄色
D.室温下,某溶液中由水电离出的c(H+)=10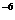 mol·L
mol·L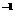 ,则此溶液可能是稀硫酸
,则此溶液可能是稀硫酸
7.下列各选项所述的两个量,前者一定大于后者的是
A.同温下分别在100g水中最多能溶解的无水CuSO4和CuSO5·5H2O的质量
B.纯水在25℃和90℃时的pH值
C.25℃时,等体积的pH都等于3的盐酸和AlCl3溶液中,已电离的水分子数
D.在反应NH3+NO→N2+H2O中,被氧化和被还原的N原子数
本部分包括21个小题.每小题6分,共126分.每小题只有一个选项符合题意.
6.2010年我国“两会”“一号提案”锁定“低碳经济”.下列做法不符合“低碳经济”的是
①禁止电动自行车上路; ②以煤等燃料作为主要生活燃料; ③鼓励私人购买和使用小汽车以代替公交车; ④利用太阳能、风能和氢能等新能源代替化石燃料.
A.①②③ B.②④ C.①④ D.②③④
28.(16分)肉桂醛在食品、医药化工等方面都有应用。
(1)质谱分析肉桂醛分子的相对分子质量为132。其分子中碳元素的质量分数为81.8%,其余为氢和氧。分子中的碳原子数等于氢、氧原子数之和。肉桂醛的分子式是
。
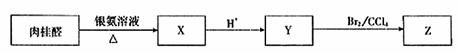 (2)肉桂醛具有下列性质:
(2)肉桂醛具有下列性质:
请回答:
①肉桂醛是苯的一取代物,核磁共振氢谱显示,苯环侧链上有三种不同化学环境的氢原
子,其结构简式是 。(本题均不考虑顺反异构与手性异构)
②Z不能发生的反应类型是 。
A.取代反应 B.消去反应 C.加成反应 D.加聚反应
③Y与乙醇在一定条件下作用得到肉桂酸乙酯,该反应的化学方程式是 。
④Y的同分异构体中,属于酯类目苯环上只有一个取代基的同分异构体有 种。
其中任意一种的结构简式是 。
(3)已知
I.醛与醛能发生反应,原理如下:
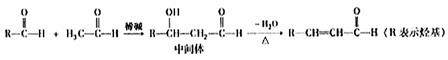
II.合成肉桂酸醛的工业流程如下图所示,其中甲烷。
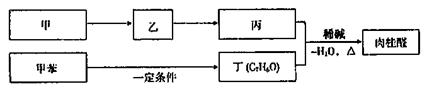
请回答:
①甲的结构简式是 。
②丙和丁生成肉桂的化学方程式是 。
③醛和酯也可以发生如“I”的反应。食用香料肉桂酸乙酯通过如下反应合成:
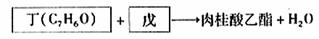
戊的名称是 。
27.(14分)铜及其化合物在生产、生活中有广泛的应用。
(1)铜可采用如下方法制备:
火法炼铜:Cu2S+O2 2Cu+SO2
湿法炼铜:CuSO4+Fe=====FeSO4+Cu-
上述两种方法中,铜元素均被 (填“氧化”或“还原”)成铜单质。
(2)印刷电路板上使用的铜需要回收利用。
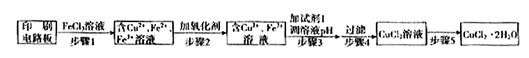 方法一:用FeCl3溶液浸泡印刷电路板制备CuCl2·2H2O,实验室模拟回收过程如下:
方法一:用FeCl3溶液浸泡印刷电路板制备CuCl2·2H2O,实验室模拟回收过程如下:
①证明步骤I所加FeCl3溶液过量的方法是 。
②步骤2中所加的氧化剂最适宜的是 。
A.HNO3 B.H2O2 C.KMnO4
③步骤3的目的是使溶液的pH升高到4.2,此时Fe3+完全沉淀,可选用的“试剂1”是 。(写出一种即可)
④蒸发农缩CuCl2溶液时,要滴加浓盐酸,目的是 (用化学方程式并结合简要的文字说明),再经冷却、结晶、过滤,得到CuCl2·2H2O。
方法二:用H2O2和稀硫酸共同浸泡印刷电路板制备硫酸铜时,其热化学方程式是:
Cu(s)+H2O2(l)+H2SO4(nq)=====CuSO4(aq)+2H2O(l)△H1=-320kJ/mol
又知:2H2O(l)====2H2O(l)+O2(g) △H2=-196kJ/mol
H2(g)+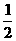 O2(g)====H2O(l)
△H3=-286kJ/mol
O2(g)====H2O(l)
△H3=-286kJ/mol
则反应Cu(s)+H2SO4(aq)====CuSO4(aq)+H2(g)的△H= 。
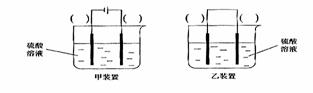
(3)欲实现反应Cu+H2SO2====CuSO4+H2,在你认为能实现该转化的装置中的括号内,标出电极材料(填“Cu”或“C”)
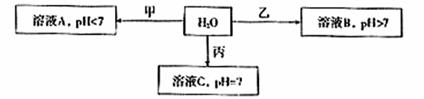
25.(14分)已知X+、Y3+、Z-、W2-是短周期元素X、Y、Z、W形成的离子,下图中的甲、乙、丙均是由上述四种离子中的两种组成的化合物。
回答下列问题:
(1)通常状况下,Z的单质是一种黄绿色气体,工业上常用电解溶液C的方法制备该单质,制备反应的化学方程式是 。
(2)①甲的化学式是 ,乙的化学式可能是 (写一种即可)
②若将溶液A与溶液B混合,产生白色沉淀,则该反应的离子方程式是 。
若W2和Z-具有相同电子层结构,则乙的电子式是 。
(3)Y单质可用来制造Y-空气燃料电池,该电池通常以溶液C或氢氧化钾溶液为电解质溶液,通入空气的电极为正极。
①若以溶液C为电解质溶液时,正极的反应式为 。
②若以氢氧化钾溶液为电解质溶液时,电池的总反应式为 。
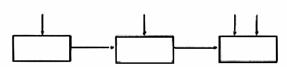
O2 O2 O2 H2O
NH3 NO 吸收塔
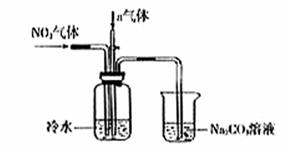 某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)
某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)
(1)工业上用氨气制取NO的化学方程式是 。
(2)连接好装置后,首先进行的操作是 。
(3)通入a气体的目的是 .
(4)盛有Na2CO3溶液的烧杯为尾气处理装置,该装置中发生反应的化学方程式是
2NO2+Na2CO3=====NaNO2+ +
(5)已知:温度低于21.15°C时,NO2几乎全部转变为N2O2。工业上可用N2O4与水反应来提高硝酸产率。N2O4与a气体在冷水中生成硝酸的化学方程式是 。
 (6)一定条件下,某密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.500mol/L,c(N2O4)=0.125mol/L。则2NO2(g) N2O4(g)的平衡常数K= 。若NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为
。
(6)一定条件下,某密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.500mol/L,c(N2O4)=0.125mol/L。则2NO2(g) N2O4(g)的平衡常数K= 。若NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为
。
12.下列叙述正确的是 ( )
①3Li+中含有的中子数与电子数之比为2:1
②在C2H6分子中极性共价键与非极性共价键数之比为3:1
③常温下,11.2L的甲烷气体中含有的氢、碳原子数之比为4:1
④5.6g铁与足量的氯气反应失去的电子与参与反应的铁的物质的量之比为2:1
A.①② B.②③ C.①③ D.③④
11.室温下,下列关于pH均为9、体积均为10m的NaOH溶液和CH3COONa溶液比较的说法,正确的是 ( )
A.两种溶液中的c(Na+)相等
B.分别加热到相同温度时,CH3COONa溶液的pH小
C.分别加水稀释到100mL时,两种溶液的pH依然相等
D.两溶液中由水电离出的c(OH-)之比为10-9/10-5
10.右表是元素周期表的一部分。X、Y、Z、W均为短周期元素,X、W的质子数之和为23。下列说法正确的是 ( )
|
B.氢化物的稳定性:Y<Z
C.最高价氧化物对应水化物的酸性:W>Z
D.Z的氧化物不能溶于Y的氢化物的水溶液
8.下列各组离子一定能大量共存的是 ( )
A.在含有0.1mol/LCa2+的溶液中:Na+、K+、ClO-、Cl-
B.在pH=12的溶液中:NH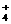 、Na+、SO
、Na+、SO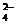 、Cl-
、Cl-
C.在c(H+)=0.1mol/L的溶液中:K+、I-、Cl-、NO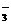
D.在澄清透明的无色溶液中:Na+、Cu2+、Cr2O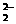 、NO
、NO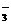
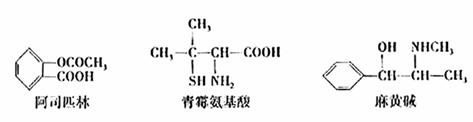 9.下列对三种有机物的叙述不正确的是(-SH的性质类似于-OH) ( )
9.下列对三种有机物的叙述不正确的是(-SH的性质类似于-OH) ( )
A.三种有机物都能发生醋化反应
 B.青霉氨基酸不能与盐酸反应,但能与NaOH反应
B.青霉氨基酸不能与盐酸反应,但能与NaOH反应
C.麻黄碱的分子式为C10H15ON,苯环的一氯代物有3种
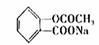
D.阿司匹林能与适量NaOH反应生成可溶性阿司匹林( )
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com