
题目列表(包括答案和解析)
4.最近,长沙晚报报道:今年九月,我省将首次启用飞机人工降雨,即利用飞机向云雾中播撒碘化银以人工降雨。当光束通过下列分散系:①有尘埃的空气 ②稀硫酸 ③水 ④墨水 ⑤淀粉溶液 ⑥鸡蛋白溶液 ⑦云雾,能观察到丁达尔效应的是
A. ①④⑤⑥⑦ B. ①②③④⑦ C. ②③④⑤⑥ D. ③④⑤⑥⑦
3、有些科学家提出硅是“21世纪的能源”,下列有关硅的说法中,不正确的是:
A.高纯度的硅广泛用于制作计算机 B.硅可以通过还原二氧化硅制得
C.常温下,硅与水和硫酸不反应,但能与氢氟酸反应
D.自然界中硅储量丰富,存在大量的单质硅.
2.随着从们生活节奏的加快,方便的小装食品已被广泛接受。为了延长食品的保质期,防止食品受潮及富脂食品氧化变质,在包装袋中应放入的化学物质是:
A.无水硫酸铜、蔗糖 B.硅胶、硫酸亚铁 C.食盐、硫酸亚铁 D.生石灰、食盐
1.2010年9月25日世界运河名城博览会在扬州举行,本届运博会的论坛主题是:运河城市发展低碳经济的重大意义及其途径。下列做法不能体现低碳生活的是
A.减少食物加工过程 B.大量使用薪柴为燃料
C.提倡使用太阳能热水器 D.注意节约用电
21.铁是人体不可缺少的微量元素,摄入含铁的化合物可补充铁。 “速力菲”是市场上一种常见的补铁药物,下表格是它的说明书。
|
[规格] 每片含琥珀酸亚铁0.1g [适应症] 用于缺铁性贫血症,预防及治疗用。 [用量用法] 成人预防量0.1g/日,成人治疗量0.2g-0.4g/日, 小儿用量预防量30-60mg/日,治疗量0.1g-0.3g/日。 [儲藏] 避光、密封、在干燥处保存 |
该药品中Fe2+ 会缓慢氧化,国家规定该药物中Fe2+ 的氧化率超过10%即不能再服用。
①(2分)为了检验某药店出售的“速力菲”是否氧化,实验室可选用最常用最灵敏的检验试剂为 ___________ ( 填试剂的名称 )
②(3分)实验室采用H2SO4酸化的KMnO4溶液,对“速力菲”中的Fe2+ 进行滴定(假设药品中,其它成分不与KMnO4反应)。请配平下列离子方程式
______MnO4- + ______Fe2+ + ______H+ == ______Mn2+ + ______Fe3+ + ______H2O
③(5分) 称量上述含铁元素质量分数为20.00% 的“速力菲”10.00 g,将其全部溶于稀硫酸中,配制成1000.00 mL溶液,取出20.00 mL,用0.01 mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00 mL。该药品可以服用吗?______________(填“可以”或“不可以”),请通过计算简述理由(写出主要计算过程)
临湘一中2011届高三第三次阶段性质量检测
20.二氧化锰(MnO2)与浓盐酸混合加热可得到氯气,下图是制取并探究Cl2化学性质的装置图。
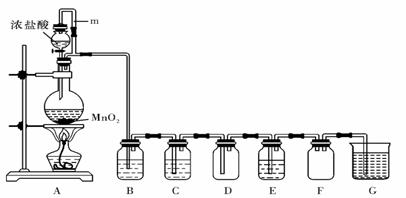
(1)圆底烧瓶中发生反应的化学方程式为 。
(2)E中若装有FeCl2 溶液,反应的离子方程式为 ;
F的作用是 。
(3)若要得到干燥纯净的气体,则B中应盛放的试剂是 。
(4) 能使湿润的淀粉-KI试纸变蓝的气体是 。
(a) Cl2 (b) N2O4 (c) I2蒸气 (d) SO2 (e) O3 (f) CO2
(5)实验中发现:浓盐酸与MnO2混合加热生成氯气,稀盐酸与MnO2混合加热不生成氯气。针对上述现象,临湘一中高三化学兴趣小组对“影响氯气生成的原因”进行了讨论,并设计了以下实验方案:
a.稀盐酸滴入MnO2中,然后通入HCl气体,加热
b.稀盐酸滴入MnO2中,然后加入NaCl固体,加热
c.稀盐酸滴入MnO2 中,然后加入浓硫酸,加热
d.MnO2与NaCl的浓溶液混合,加热
e.浓硫酸与NaCl固体、MnO2固体共热
①实验b的目的是 ;
②实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成。由此得出影响氯气生成的原因是 。
19.双氧水(H2O2)是一种极弱电解质,也是一种“绿色氧化剂”。为了贮存、运输的方便,工业上将其转化为固态过碳酸钠(2Na2CO4·3H2O2),该物质具有Na2CO3与H2O2的双重性质。请回答下列问题:
(1)写出H2O2的电子式: ,并写出它与SO2反应的化学方程式 。
(2)若把H2O2看成二元弱酸,写出它在水中第一步电离的方程式 。
(3)下列物质不会使过碳酸钠失效的是
A.MnO2 B.NaHCO3 C.H2S D.CH3COOH
(4)H2O2成为“绿色氧化剂”的理由是
18. A、B、D、E 四种短周期元素,其原子序数逐渐增大。A 元素原子的核外电子数、电子层数和最外层电子数均相等,B、D、E 三种元素在周期表中相对位置如图①所示,E 的单质能与水反应生成两种酸。甲、乙、M、W、X、Y、Z 七种物质均由A、B、D 三种元素中的一种或几种组成,其中只有M 分子同时含有三种元素;W 为A、B 两元素组成的18 电子分子,可做火箭燃料;甲、乙为非金属单质;X 分子含有10个电子。它们之间的转化关系如图②。
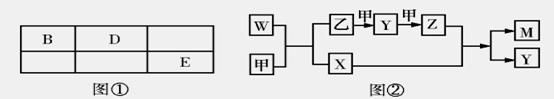
回答下列问题:
(1)Z的化学式为 。
(2)E 的单质与水反应的离子方程式为 。
(3)W与甲反应生成乙和X的化学方程式为: 。
(4)由A、B、D 三种元素组成的某种盐中阳离子的鉴定方法与现象为:
。
17.A、B、C、D四种可溶性的盐,它们的阳离子分别可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别可能是NO3-、SO42-、Cl-、、CO32-中的一种。
⑴若把四种盐分别溶解于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色。
⑵若向⑴的四支试管中分别加入盐酸,B盐溶液有沉淀生成,D盐溶液有五色无味的气体逸出。根据⑴、⑵实验事实可推断它们的化学式为:
A B C D 。
写出盐酸与D反应的离子反应方程式: 。
16、在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关
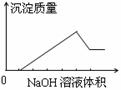 系如右图所示,由此确定,原溶液中含有的阳离子是( )
系如右图所示,由此确定,原溶液中含有的阳离子是( )
A.Mg2+、Al3+、Fe2+ B.H+、Mg2+、Al3+
C.H+、Ba2+、Al3+ D.只有Mg2+、Al3+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com