
题目列表(包括答案和解析)
8.在常温下,发生下列反应:①16H++10Z-+2XO4-→2X2++5Z2+8H2O;②2A2++B2→2A3++2B-;③2B-+Z2→B2+2Z-。根据上述反应,判断下列结论中错误的是 ( )
A.溶液中可发生:Z2+2A2+→2A3++2Z-
B.Z2在①、③反应中为还原剂
C.氧化性强弱的顺序为:XO4->Z2>B2>A3+
D.X2+是XO4-的还原产物
7.某中性含Na+的溶液中,可能还存在NH4+ 、Fe2+ 、Br- 、CO32- 、I- 、SO32-六种离子中的一种或几种。进行以下实验:①在原溶液中滴加足量氯水后,有气泡产生,溶液呈橙黄色;②向橙黄色溶液中加入BaCl2溶液时,无沉淀生成;③橙黄色溶液不能使淀粉变蓝。由此可以推知该溶液中肯定不存在的离子是 ( )
A.NH4+ 、Br- 、CO32- B.NH4+ 、I- 、SO32-
C.Fe2+ 、I- 、SO32- D.Fe2+ 、CO32- 、I-
6.NA表示阿伏加德罗常数,下列说法中正确的是 ( )
A.由2H和18O所组成的水11g,其中所含的中子数为4NA
B.1 mol FeCl3跟水完全反应转化为氢氧化铁胶体后,其中胶体粒子的数目为NA
C.2.3 g Na和足量的O2完全反应,在常温和燃烧时,转移电子数均为0.1NA
D.500mL0.1mol•L-1盐酸溶液中,含有HCl分子数目为0.25 NA
5.下列实验方法不能达到目的的是 ( )
A.用加热的方法分离氯化钠和氯化铵的固体混和物
B.用水鉴别乙醛、苯、硝基苯
C.用核磁共振氢谱鉴定未知物C2H6O的分子结构
D.用10mL量筒量取5.00mL1.00 mol·L-1盐酸配制0.100mol·L-1盐酸
4.下列说法正确的是 ( )
A.根据是否有丁达尔现象将分散系分为:溶液、胶体、浊液。
B.双氧水、水玻璃、氯水都是混合物
C.强电解质的导电能力一定比弱电解质强
D.酸性氧化物一定是非金属氧化物
3.用示意图或图示的方法能够直观形象地将化学知识传授给学生,下列示意图或图示正确的是 ( )
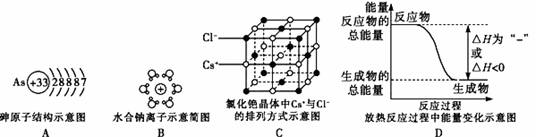
2.Na2O、NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为同一类物质,下列分类标准正确的是 ( )
①钠的化合物 ②能与硝酸反应的物质
③可溶于水的物质 ④电解质
⑤钠盐 ⑥钠的含氧化合物
A.①③④⑤ B.①②⑤⑥ C.①③④ D.②⑤⑥
1.下列分离物质的方法中,根据微粒大小进行分离的是 ( )
①分液 ②过滤 ③分馏 ④重结晶 ⑤渗析
A.②⑤ B.②④ C.①② D. ①③⑤
22.
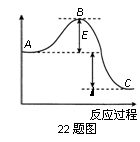
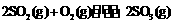 反应过程的能量变化如图所示。已知
反应过程的能量变化如图所示。已知 氧化为
氧化为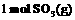 的
的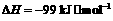 。请回答问题:
。请回答问题:
(1)图中A、C分别表示 、 ,E的大小对该反应的
反应热有无影响? 。该反应通常用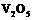 作催化剂,加
作催化剂,加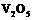 会使图中
会使图中
B点升高还是降低? ,理由是 。
(2)图中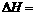
 。
。
(3)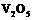 的催化循环机理可能为:
的催化循环机理可能为: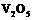 氧化
氧化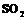 时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式
。
时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式
。
(4)如果反应速率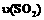 为
为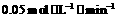 ,则
,则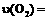
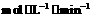 、
、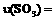
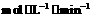 。
。
(5)已知单质硫的燃烧热为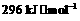 ,计算由
,计算由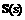 生成
生成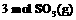 的
的 。
。
21.某厂的酸性工业废水中含有一定量的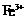 、
、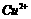 、
、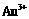 等离子。有人设计了如图所示的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。
等离子。有人设计了如图所示的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。
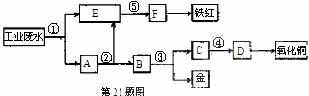
填写下面空白。
(1)图中标号处需加入的相应物质分别是① 、② 、③ 、④ 、⑤ 。
(2)写出①处发生反应的离子方程式 ;
写出③处发生反应的化学方程 。
(3)铁红的化学式为 ;分别写出铁红和氧化铜在工业上的一种主要用途:铁红 ;氧化铜 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com