
题目列表(包括答案和解析)
(12分)碱式碳酸铝镁[MgaAlb(OH)c(CO3)d·x H2O]常用作塑料阻燃剂。
(1)碱式碳酸铝镁具有阻燃作用,是由于其受热分解需吸收大量热量和 。
(2)MgaAlb(OH)c(CO3)d·x H2O中a、b、c、d的代数关系式为 。
(3)为确定碱式碳酸铝镁的组成,进行如下实验:
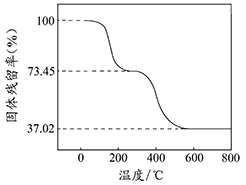
①准确称取3.390g样品与足量稀盐酸充分反应,生成CO20.560L(已换算成标准状况下)。②另取一定量样品在空气中加热,样品的固体残留率(固体样品的剩余质量/固体样品的起始质量×100%)随温度的变化如右图所示(样品在2700C时已完全失去结晶水,6000C以上残留固体为金属氧化物的混合物)。
根据以上实验数据计算碱式碳酸铝镁样品中的n(OH-): n(CO32-)(写出计算过程)。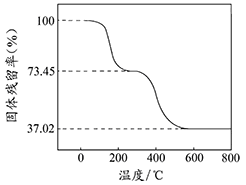
(8分)水煤气不仅是合成氨的原料气也是合成烃及其化工产品的原料。
(1)直接水煤气燃料电池中,通CO、H2的极为电池的 极(选填:“正”,“负”)。
(2)水煤气变换反应:CO(g) + H2O(g)  CO2(g) + H2(g) △H < 0,下列措施能提高反应速率的有 (不定项选择)。
CO2(g) + H2(g) △H < 0,下列措施能提高反应速率的有 (不定项选择)。
a.升高温度 b.加入催化剂 c.增大压强 d.降低浓度
(3)H2和N2在催化剂、高温高压条件下合成氨的化学方程式为 。
(4)氨气的水溶液可用于吸收烟道气中的二氧化硫,该反应的化学方程式为 。
(5)将标准状况下582.4L合成气(已知:n(CO)∶n(H2)=4∶9)通入合成塔,一定条件下可发生2CO(g)+ 4H2(g) → CH2=CH2(g)+2H2O(g);CO(g)+3H2→CH4(g)+H2O(g),充分反应后,经测定产品中只有甲烷、乙烯和水蒸气(假定CO和H2均无剩余),试计算逸出的气体中乙烯的物质的量(列出计算过程)。
 CO2(g) + H2(g) △H < 0,下列措施能提高反应速率的有 (不定项选择)。
CO2(g) + H2(g) △H < 0,下列措施能提高反应速率的有 (不定项选择)。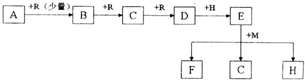
 g
g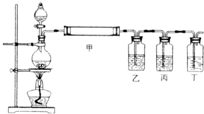
一、选择题(126分、每题6分)
1、B 2、B 3、A 4、A 5、B
6、D 7、A 8、C 9、B 10、C 11、C 12、D 13、B
14、B 15、D 16、B 17、CD 18、B 19、D 20、AC 21、BCD
二、非选择题(174分)
22、I(1)圆形亮斑的直径理科综合.files/image333.gif) (或半径
(或半径理科综合.files/image335.gif) )半球形玻璃砖的直径
)半球形玻璃砖的直径理科综合.files/image337.gif) (或半径
(或半径理科综合.files/image339.gif) )(每空1分)
)(每空1分)
(2) 理科综合.files/image341.gif) 或
或理科综合.files/image343.gif) (2分)
(2分)
(3)理科综合.files/image345.gif) 或
或理科综合.files/image347.gif) (2分)
(2分)
Ⅱ(1) 11.675 (2分) 3.695(3.694~3.696正确)(2分)
理科综合.files/image349.gif) (2)①如图所示(3分)
(2)①如图所示(3分)
②理科综合.files/image179.gif) (2分)
(2分)
③理科综合.files/image352.gif) (2分)
(2分)
23、(1)设纸带的加速度为理科综合.files/image354.gif) ,铁块的加速度为
,铁块的加速度为理科综合.files/image356.gif) ,则
,则理科综合.files/image354.gif) =
=理科综合.files/image358.gif) m/s2 (2分)
m/s2 (2分)
理科综合.files/image360.gif) (2分) 得: t=1s(2分)
(2分) 得: t=1s(2分)
(2)由理科综合.files/image362.gif) (2分) 得
(2分) 得 理科综合.files/image364.gif) (3分)
(3分)
又:理科综合.files/image366.gif) m/s(2分) 所以:
m/s(2分) 所以:理科综合.files/image368.gif) J(3分)
J(3分)
24、(1)带电粒子在磁场运动由轨迹可知:理科综合.files/image370.gif) (2分)
(2分)
又 理科综合.files/image372.gif) (2分) 解得:
(2分) 解得:理科综合.files/image374.gif) (2分)
(2分)
(2)带电粒子在电场中运动时,沿理科综合.files/image052.gif) 轴有:
轴有:理科综合.files/image377.gif) (1分)
(1分)
沿y轴有:理科综合.files/image379.gif) (2分)
(2分)
又 理科综合.files/image381.gif) (2分) 解得:
(2分) 解得:理科综合.files/image383.gif) (2分)
(2分)
(3)带电粒子在磁场中运动时间为: 理科综合.files/image385.gif) (2分)
(2分)
带电粒子在电场中运动时间为:理科综合.files/image387.gif) (2分)
(2分)
所以带电粒子在磁场和电场中运动时间之比为:理科综合.files/image389.gif) (2分)
(2分)
25、(1)对整体由动量守恒定律得 理科综合.files/image391.gif) 解得
解得 理科综合.files/image393.gif) ,方向向右(5分)
,方向向右(5分)
(2)由功能关系得理科综合.files/image395.gif) 解得
解得 理科综合.files/image397.gif) (5分)
(5分)
(3)①物体理科综合.files/image399.gif) 未碰撞,
未碰撞,理科综合.files/image113.gif) 停止时,
停止时,理科综合.files/image111.gif) 继续运动,此时小车开始运动。对小车和
继续运动,此时小车开始运动。对小车和理科综合.files/image113.gif) 应用动能定理得
应用动能定理得 理科综合.files/image404.gif) 则
则 理科综合.files/image406.gif) (4分)
(4分)
②物体理科综合.files/image113.gif) 速度为零时正好与
速度为零时正好与理科综合.files/image111.gif) 发生碰撞,碰后小车开始加速,最终达到共同速度
发生碰撞,碰后小车开始加速,最终达到共同速度 理科综合.files/image410.gif)
对小车应用动能定理得
理科综合.files/image412.gif) 则
则理科综合.files/image414.gif) (4分)
(4分)
所以小车位移大小 的取值范围是 理科综合.files/image416.gif) (2分)
(2分)
26、(1)理科综合.files/image418.gif) (3分)
(3分)
理科综合.files/image420.gif) (3分)
(3分)
(2)
理科综合.files/image422.gif)
2 5
0.04mol 理科综合.files/image424.gif)
理科综合.files/image424.gif) =0.1mol
=0.1mol 理科综合.files/image427.gif) =
=
(3)6.32g理科综合.files/image429.gif) 固体加热分解一段时间:根据极限法,可以分解率为0,即生成氯气的体积在标准状况下为
固体加热分解一段时间:根据极限法,可以分解率为0,即生成氯气的体积在标准状况下为
理科综合.files/image431.gif)
2 1 1
0.04mol 0.02mol 0.02mol
理科综合.files/image433.gif)
1 2
0.02mol 0.04mol
理科综合.files/image435.gif)
1 1
0.02mol 0.02mol
产生的氯气共为0.06mol,
理科综合.files/image427.gif) =
=
可以确定氯气体积范围1.344L理科综合.files/image437.gif) L (4分)。
L (4分)。
27、(1)理科综合.files/image439.gif) (2分)
(2分)
理科综合.files/image441.gif)
(2)(3分)
(3)(只写出两种,每个2分)
理科综合.files/image443.gif)
理科综合.files/image445.gif)
(4)(3分)
(5)有利于控温,均匀受热,减少副反应发生(2分)
(6)解析:理科综合.files/image447.gif) ;
;理科综合.files/image449.gif)
理科综合.files/image451.gif)
理科综合.files/image453.gif) [或
[或理科综合.files/image455.gif) ](3分)
](3分)
28、(每空2分)
(1) 理科综合.files/image457.jpg) 极性
极性
(2)20~50MPa,理科综合.files/image459.gif) 左右,催化剂 >
左右,催化剂 > 理科综合.files/image461.gif)
(3)正四面体形 负 理科综合.files/image463.gif)
29、(每空2分)
(1)理科综合.files/image046.gif) 溶液 (2)除去铝镁合金表面的氧化膜
溶液 (2)除去铝镁合金表面的氧化膜
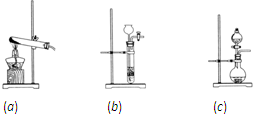
(3)⑤①④③② 使D和C的液面相平
(4)理科综合.files/image466.gif) (5)
(5)理科综合.files/image468.gif) (6)偏小
(6)偏小
解析:(5)反应消耗Al的质量为(理科综合.files/image470.gif) )g,设Al的相对原子质量为
)g,设Al的相对原子质量为理科综合.files/image052.gif) ,则
,则
2Al ~ 3H2
理科综合.files/image473.gif) g 67200
g 67200 理科综合.files/image475.gif)
(理科综合.files/image470.gif) )g b
)g b理科综合.files/image475.gif)
解得:理科综合.files/image468.gif)
(6)若未洗涤过滤所得的不溶物,其表面吸附的物质会导致测得的剩余固体质量变大,使测得的铝的质量分数偏小。
30、(20分,每空2分)
实验组
实验处理方法
预期结果
(下一步)实验处理方法
预期结果
A组(对照组)(2只)
注射等量生理盐水
清醒
不作处理
清醒
B组(2只)
注射一定量胰岛素溶液
休克
注射等量生理盐水
未清醒
C组(2只)
注射一定量胰高血糖素溶液
清醒
D组(2只)
注射一定量葡萄糖溶液
清醒
31、(1)(12分,每空3分)、
吞噬细胞→T细胞→B细胞 ; 造血干细胞; 杂交瘤细胞;
该杂交瘤细胞继承了双亲细胞的遗传物质
(2)(10分)结果及相应的结论:
①若后代中只出现一种性状,,则这些杂交组合中的雌鼠的野生型性状为显性(图一)。
②若后代中雌性个体全为突变型、雄性个体全为野生型,则这些杂交组合中的雄鼠的突变型性状为显性(图二)。
③若后代中雌性和雄性个体中均有突变性,野生型性状出现,则该杂交组合中的雌鼠的野生型性状为显性(图三和图一)。
P XbY(突变型♂)×XBXB(野生型♀)
↓
F XBY(野生型♂)XBXb(野生型♀)
图 一
P XBY(突变型♂)×XbXb(野生型♀)
↓
F XbY(野生型♂)XBXb(突变型♀)
图 二
P XbY(突变型♂)×XBXb(野生型♀)
↓
F XBY(野生型♂) XbY(突变型♂) XBXb(野生型♀) XbXb(突变型♀)
图 三
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com