
30、(15分)TiO2既是制备其他含钛化合物的原料,又是一种性能优异的白色颜料。
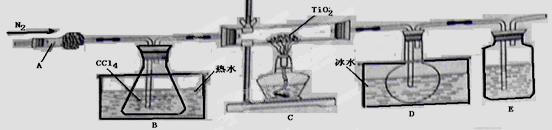
(1)实验室利用反应TiO2(s)+CCl4(g)==TiCl4(g)+CO2(g),在无水无氧条件下,制取TiCl4实验装置示意图如下
有关性质如下表
|
物质 |
熔点/℃ |
沸点/℃ |
其他 |
|
CCl4 |
-23 |
76 |
与TiCl4互溶 |
|
TiCl4 |
-25 |
136 |
遇潮湿空气产生白雾 |
仪器A的名称是 ,装置E中的试剂是 。反应开始前依次进行如下操作:组装仪器、 、加装药品、通N2一段时间后点燃酒精灯。反应结束后的操作包括:①停止通N2②熄灭酒精灯③冷却至室温。正确的顺序为 (填序号)。欲分离D中的液态混合物,所采用操作的名称是 。
(2)工业上由钛铁矿(FeTiO3)(含Fe2O3、SiO2等杂质)制备TiO2的有关反应包括:
|
水解TiOSO4(aq)+ 2H2O(l)== H2TiO3(s)+H2SO4(aq)
简要工艺流程如下:
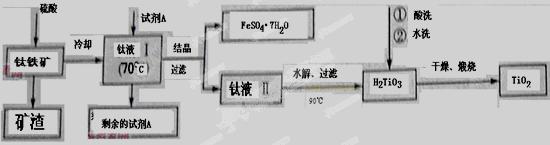
①试剂A为 。钛液Ⅰ需冷却至70℃左右,若温度过高会导致产品TiO2收率降低,原因是
②取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是 。这种H2TiO3即使用水充分洗涤,煅烧后获得的TiO2也会发黄,发黄的杂质是 (填化学式)。
[选做部分24分]
29、(15分)化学反应原理在科研和生产中有广泛应用
(1)利用“化学蒸气转移法”制备TaS2晶体,发生如下反应
TaS2(s)+2I2(g) TaI4(g)+S2(g) △H﹥0 (I)
TaI4(g)+S2(g) △H﹥0 (I)
反应(I)的平衡常数表达式K= ,若K=1,向某恒容密闭容器中加入1mol I2(g)和足量TaS2(s),I2(g)的平衡转化率为
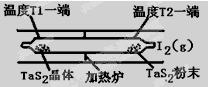 (2)如图所示,反应(I)在石英真空管中进行,先在温度为T2的一端放入未提纯的TaS2粉末和少量I2(g),一段时间后,在温度为T1的一端得到了纯净的TaS2晶体,则温度T1 T2(填“﹥”“﹤”或“=”)。上述反应体系中循环使用的物质是
。
(2)如图所示,反应(I)在石英真空管中进行,先在温度为T2的一端放入未提纯的TaS2粉末和少量I2(g),一段时间后,在温度为T1的一端得到了纯净的TaS2晶体,则温度T1 T2(填“﹥”“﹤”或“=”)。上述反应体系中循环使用的物质是
。
(3)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化为H2SO3,然后用一定浓度的I2溶液进行滴定,所用指示剂为 ,滴定反应的离子方程式为
(4)25℃时,H2SO3  HSO3-+H+的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3的水解反应的平衡常数Kh=
mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中
HSO3-+H+的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3的水解反应的平衡常数Kh=
mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中 将
(填“增大”“减小”或“不变”)。
将
(填“增大”“减小”或“不变”)。
28、(12分)金属冶炼和处理常涉及氧化还原反应。
(1)由下列物质冶炼相应金属时采用电解法的是
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
 (2)辉铜矿(Cu2S)可发生反应2Cu2S+2H2SO4+5O2==4CuSO4+2
H2O,该反应的还原剂是
,当1mol O2发生反应时,还原剂所失电子的物质的量为 mol。向CuSO4溶液中加入镁条时有气体生成,该气体是
(2)辉铜矿(Cu2S)可发生反应2Cu2S+2H2SO4+5O2==4CuSO4+2
H2O,该反应的还原剂是
,当1mol O2发生反应时,还原剂所失电子的物质的量为 mol。向CuSO4溶液中加入镁条时有气体生成,该气体是
(3)右图为电解精炼银的示意图, (填a或b)极为含有杂质的粗银,若b极有少量红棕色气体生成,则生成该气体的电极反应式为
(4)为处理银器表面的黑斑(Ag2S),将银器置于铝制容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为
27、 (14分)某二倍体植物宽叶(M)对窄叶(m)为显性,高茎(H)对矮茎(h)为显性,红花(R)对白花(r)为显性。基因M、m与基因R、r在2号染色体上,基因H、h在4号染色体上。
(14分)某二倍体植物宽叶(M)对窄叶(m)为显性,高茎(H)对矮茎(h)为显性,红花(R)对白花(r)为显性。基因M、m与基因R、r在2号染色体上,基因H、h在4号染色体上。
(1)基因M、R编码各自蛋白质前3个氨基酸的DNA序列如图,起始密码子均为AUG。若基因M的b链中箭头所指碱基C突变为A,其对应的密码子由 变为 。正常情况下,基因R在细胞中最多有 个,其转录时的模板位于 (填“a”或“b”)链中。
(2)用基因型为MMHH和mmhh的植株为亲本杂交获得F1,F1自交获得F2,F2中自交性状不分离植株所占的比例为 ,用隐性亲本与F2中宽叶高茎植株测交,后代中宽叶高茎与窄叶矮茎植株的比例为 。
(3)基因型为Hh的植株减数分裂时,出现了一部分处于减数第二次分裂中期的Hh型细胞,最可能的原因是 。缺失一条4号染色体的高茎植株减数分裂时,偶然出现一个HH型配子,最可能的原因是 。
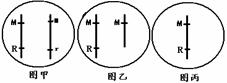 (4)现有一宽叶红花突变体,推测其体细胞内与该表现型相对应的基因组成为图甲、乙、丙中的一种,其他同源染色体数目及结构正常。现只有各种缺失一条染色体的植株可供选择,请设计一步杂交实验,确定该突变体的基因组成是哪一种。(注:各型配子活力相同;控制某一性状的基因都缺失时,幼胚死亡)
(4)现有一宽叶红花突变体,推测其体细胞内与该表现型相对应的基因组成为图甲、乙、丙中的一种,其他同源染色体数目及结构正常。现只有各种缺失一条染色体的植株可供选择,请设计一步杂交实验,确定该突变体的基因组成是哪一种。(注:各型配子活力相同;控制某一性状的基因都缺失时,幼胚死亡)
实验步骤:①
②观察、统计后代表现性及比例
结果预测:Ⅰ若 ,则为图甲所示的基因组成;
Ⅱ若 ,则为图乙所示的基因组成;
Ⅲ若 ,则为图丙所示的基因组成。
26、(8分)稻田中除了水稻外,还有杂草、田螺等生物。
|
样方编号 |
1 |
2 |
3 |
4 |
5 |
6 |
|
样方面积(㎡) |
1 |
1 |
1 |
1 |
1 |
1 |
|
田螺数量(只) |
15 |
18 |
15 |
19 |
15 |
14 |
(1)调查稻田中田螺种群密度时可以采用样方法,选取样方的关键是 。根据右侧的取样调查表可估算出稻田中田螺的种群密度为 。只/m2
 (2)稻田中经控制后的有害生物密度与所需的防治成本有关,并影响作物的价值。图中曲线
(2)稻田中经控制后的有害生物密度与所需的防治成本有关,并影响作物的价值。图中曲线
(填“Ⅰ”或“Ⅱ”)表示将有害生物控制在不同密度时的防治成本。若将有害生物密度分别控制在图中A、B、C三点,则控制在 点时收益最大。
(3)如在适当时间将鸭引入稻田,鸭能以稻田中的杂草、田螺等有害生物为食,从而可以减少 使用,减轻环境污染。稻田生态系统中的 能将鸭的粪便分解成 以促进水稻的生长。
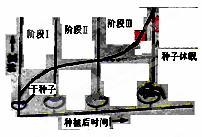
25、(10分)大豆种子萌发过程中鲜重的变化曲线如图
(1)阶段Ⅰ和Ⅲ大豆种子的鲜重增加明显,阶段Ⅰ中,水进入种子胚细胞的穿(跨)膜运输方式为 。阶段Ⅲ中,种子胚细胞内水的主要存在形式是 。
(2)阶段Ⅱ期间,大豆种子胚细胞合成的 解除种子休眠,促进种子萌发。阶段Ⅲ中根向地生长的原因是 分布不均,使根的近地侧生长受到 。
(3)若测得阶段Ⅱ种子吸收O2与释放CO2的体积比为1:3,则此时种子胚细胞的无氧呼吸与有氧呼吸消耗葡萄糖之比为 。
(4)大豆幼苗在适宜条件下进行光合作用时,若突然停止CO2供应,短时间内叶绿体中C5和ATP含量的变化分别为 、 。大田种植大豆时,“正其行,通其风”的主要目的是通过 提高光合作用强度以增加产量。
24、(9分)长跑比赛中,运动员体内多种生理过程发生了改变。
(1)机体产热大量增加,通过神经调节,引起皮肤 和汗腺分泌增强,导致散热加快以维持体温的相对恒定。这一调节过程的中枢位于 。
(2)机体大量出汗导致失水较多,刺激渗透压感受器,引起垂体释放 ,继而促进 ,以维持体内的水盐平衡。
(3)机体血糖大量消耗的主要途径是 ,此时骨骼肌细胞的直接供能物质是 ,血糖含量降低时,胰岛A细胞分泌的胰岛高血糖素增加,肾上腺髓质分泌的 增加,使血糖快速补充。
 (4)比赛结束后,运动员可以适量补充水分以消除由于
中渗透压升高引起的渴感,还可通过积极放松的方式缓解因肌肉细胞中
积累过多造成的肌肉酸痛。
(4)比赛结束后,运动员可以适量补充水分以消除由于
中渗透压升高引起的渴感,还可通过积极放松的方式缓解因肌肉细胞中
积累过多造成的肌肉酸痛。
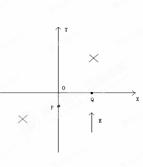
23.(18分)如图所示,在坐标系xoy的第一、第三象限内存在相同的匀强磁场,磁场方向垂直于xoy平面向里;第四象限内有沿y轴正方向的匀强电场,电场强度大小为E。一带电量为 、质量为
、质量为 的粒子,自y轴的P点沿x轴正方向射入第四象限,经x轴上的Q点进入第一象限,随即撤去电场,以后仅保留磁场。已知OP=d,OQ=2d。不计粒子重力。(1)求粒子过Q点时速度的大小和方向。
的粒子,自y轴的P点沿x轴正方向射入第四象限,经x轴上的Q点进入第一象限,随即撤去电场,以后仅保留磁场。已知OP=d,OQ=2d。不计粒子重力。(1)求粒子过Q点时速度的大小和方向。
(2)若磁感应强度的大小为一定值B0,粒子将以垂直y轴的方向进入第二象限,求B0;
(3)若磁感应强度的大小为另一确定值,经过一段时间后粒子将再次经过Q点,且速度与第一次过Q点时相同,求该粒子相邻两次经过Q点所用的时间。
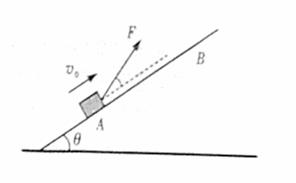
22.(15分)如图所示,一质量m=0.4kg的小物块,以V0=2m/s的初速度,在与斜面成某一夹角的拉力F作用下,沿斜面向上做匀加速运动,经t=2s的时间物块由A点运动到B点,A、B之间的距离L=10m。已知斜面倾角θ=30o,物块与斜面之间的动摩擦因数
 。重力加速度g取10 m/s2.
。重力加速度g取10 m/s2.
 (1)求物块加速度的大小及到达B点时速度的大小。
(1)求物块加速度的大小及到达B点时速度的大小。
(2)拉力F与斜面的夹角多大时,拉力F最小?拉力F的最小值是多少?
21.(13分)
(1)图甲为一游标卡尺的结构示意图,当测量一钢笔帽的内径时,应该用游标卡尺的__________(填“A”“B”或“C”)进行测量;示数如图乙所示,该钢笔帽的内径为________mm。
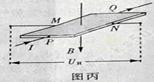

(2)霍尔效应是电磁基本现象之一,近期我国科学家在该领域的实验研究上取得了突破性进展。如图丙所示,在一矩形半导体薄片的P、Q间通入电流I,同时外加与薄片垂直的磁场B,在M、N间出现电压UH,这个现象称为霍尔效应,UH称为霍尔电压,且满足 ,式中d为薄片的厚度,k为霍尔系数。某同学通过实验来测定该半导体薄片的霍尔系数。
,式中d为薄片的厚度,k为霍尔系数。某同学通过实验来测定该半导体薄片的霍尔系数。
①若该半导体材料是空穴(可视为带正电粒子)导电,电流与磁场方向如图丙所示,该同学用电压表测量UH时,应将电压表的“+”接线柱与_________(填“M”或“N”)端通过导线相连。
②已知薄片厚度d=0.40mm,该同学保持磁感应强度B=0.10T不变,改变电流I的大小,测量相应的UH值,记录数据如下表所示。
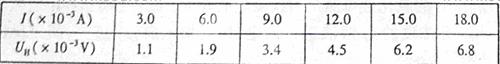
根据表中数据在给定区域内(见答题卡)画出UH—I图线,利用图线求出该材料的霍尔系数为_______________ (保留2位有效数字)。
(保留2位有效数字)。
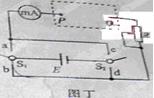
③该同学查阅资料发现,使半导体薄片中的电流反向再次测量,取两个方向测量的平均值,可以减小霍尔系数的测量误差,为此该同学设计了如图丁所示的测量电路,S1、S2均为单刀双掷开关,虚线框内为半导体薄片(未画出)。为使电流自Q端流入,P端流出,应将S1掷向_______(填“a”或“b”), S2掷向_______(填“c”或“d”)。
 为了保证测量安全,该同学改进了测量电路,将一合适的定值电阻串联在电路中。在保持其它连接不变的情况下,该定值电阻应串联在相邻器件____________和__________(填器件代号)之间。
为了保证测量安全,该同学改进了测量电路,将一合适的定值电阻串联在电路中。在保持其它连接不变的情况下,该定值电阻应串联在相邻器件____________和__________(填器件代号)之间。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com