
6、在一个密闭容器内有四种物质,在一定条件下充分反应后,测得反应前后各物质的质量如表所示:已知X的相对分子质量为n,Q的相对分子质量为2n,下列推理正确的是( )
|
物 质 |
X |
Y |
Z |
Q |
|
反应前质量/g |
4 |
10 |
1 |
21 |
|
反应后质量/g |
0 |
12 |
15 |
待测 |
A、反应后Y与Z的质量之比是1:7
B、反应后生成15g Z
C、反应中Y与Q发生改变的质量之比为1:1
D、该反应的化学方程式中X与Q的化学计量数之比为2:3
5、下列各组物质在水中能共存的是( )
A.NaCl、AgNO3、H2SO4 B.BaCl2、Na2CO3、KNO3
C.NaOH、FeCl3、HCI D.NaNO3、KOH、Na2SO4
4、下列关于Fe、Fe2+、Fe3+的说法中,正确的是( )
A.它们结合其他原子的个数相同 B.它们的质子数不同
C.它们的最外层电子数相同 D.它们的核外电子数不同
3.中国科学技术大学钱逸泰教授等以CCl4和金属钠为原料,在700℃时制造出纳米级金刚石粉末。该成果发表在世界权威的《科学》杂志上,立即被科学家们高度评价为“稻草变黄金”。同学们对此的一些“理解”,不正确的是( )
A.金刚石属于金属单质 B.制造过程中元素种类没有变化
C.CCl4是一种化合物 D.这个反应是置换反应
2、下列各组物质中,按单质、化合物、混合物的顺序排列的是( )
A.水银、干冰、尿素 B.蒸馏水、自来水、矿泉水
C.金刚石、生石灰、石油 D.乙醇、乙酸、胆矾
1、下列变化中,属于物理变化,且对其解释正确的是( )
A.二氧化碳气体制成干冰体积变小,是因为二氧化碳分子变小
B.水结成冰体积变大,是因为水的密度比冰的大
C.碳酸钠晶体在干燥空气里变成粉末.是因为此时它易失去结晶水
D.活性炭吸附有毒气体,是因为活性炭与有毒气体发生化学反应
24.有盐酸和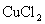 的混合溶液共l00g,向混合溶液中逐滴加入溶质质量分数为l0%的
的混合溶液共l00g,向混合溶液中逐滴加入溶质质量分数为l0%的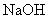 溶液,生成的沉淀与加入的l0%的
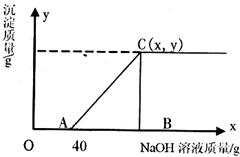
溶液,生成的沉淀与加入的l0%的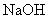 溶液质量关系如图所示。若
溶液质量关系如图所示。若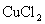 在混合溶液中的质量分数为13.5%。求:
在混合溶液中的质量分数为13.5%。求:
(1)原混合溶液中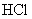 的质量分数;(2)C点的坐标
的质量分数;(2)C点的坐标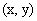 。
。
23.(11分)某校化学研究性学习小组的同学对一包因敞口放置已部分变质的氢氧化钠产生了兴趣,想通过实验测定其中碳酸钠的质量分数,请你参与他们的探究过程。
[提出问题]:样品中碳酸钠的质量分数是多少?
[收集资料]:
(1)判断氢氧化钠是否变质的方法之一是向样品中滴加盐酸,看是否有气泡冒出;
(2)判断氢氧化钠是否变质的另一种方法是将样品溶于水,再向样品中滴加澄清石灰水,看是否变浑浊。
[设计方案]:
(1)甲组同学:称取16.40g样品,放入足量的盐酸中直到反应停止,共收集到4.40g二氧化碳。
则甲组同学设计的思路是根据 ;
(2)乙组同学:称取16.40g样品,加水配成溶液,在溶液中加入过量的澄清石灰水。过滤、洗涤、干燥,共得到白色沉淀l0.00g。
乙组同学设计的思路是根据 ;
[解决问题]:
(1)乙组同学判断石灰水是否过量的方法是: ;
(2)根据两组同学的实验结果,请帮助他们计算出样品中碳酸钠的质量分数:
甲乙两组同学的计算结果分别是 。
[交流与拓展]:
在交流时,老师问同学们“能否用上述实验所得的数据计算出样品中氢氧化钠的质量分数”,甲乙两组的同学都一致认为可以。但小明思考后,觉得甲、乙两种方案都不妥。
小明的理由是: 。
22.(5分)某同学想探究酸碱中和反应是否放热。他进行了下列实验操作:取溶质质量分数为20%的稀硫酸30mL,用温度计测出其温度为13℃。然后向其中加入5.6g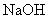 固体,恰好完全反应。再用温度计测出温度为22℃。由此,该同学得出
固体,恰好完全反应。再用温度计测出温度为22℃。由此,该同学得出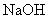 与稀硫酸发生的中和反应是放热反应的结论。请回答下列问题:
与稀硫酸发生的中和反应是放热反应的结论。请回答下列问题:
(1)该同学所得的结论的依据是否科学? (选填“科学”或“不科学),理由是 。
(2)根据本实验的目的,请提出你的做法 。
21.(6分)以下是一些常见物质间互相转化的关系图(有些反应条件未注明)
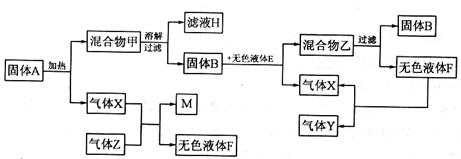
(1)将固体A充分加热至不再产生气体,滤液H中所含有的物质有: (写化学式)。
(2)如果气体Z是最简单的有机物,它在气体X中燃烧,会因X的量的不同而生成不同的物质。试写出X和Z反应生成固体单质M和无色液体F的化学方程式: 。
(3)写出固体B和无色液体E混合后反应的化学方程式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com