
1.下列变化属于化学变化的是
32.在一次课外活动中,先后有三组同学用含有碳酸钠的氯化钠固体进行了如下实验。
(1)为了得到纯净的氯化钠溶液,第一组同学取一定量的上述固体混合物,全部溶解于水,然后加入所选试剂,生成沉淀,恰好完全反应后过滤,所得滤液为氯化钠溶液。则该组同学选择的试剂是 (填写所选试剂编号)。
实验老师提供的试剂有:①盐酸,②氯化钙溶液,③氢氧化钡溶液。
(2)为测定该固体混合物中氯化钠的质量分数,第二组同学取该固体混合物26.5g,全部溶解在水中,然后加入另一种所选试剂,反应至溶液pH等于7,生成气体质量为2.2g。该固体混合物中碳酸钠的质量分数为多少?
(3)第三组同学利用第一组同学除杂提纯氯化钠的方法,配制了600g质量分数为10%的氯化钠溶液,则需要上述固体混合物多少克?
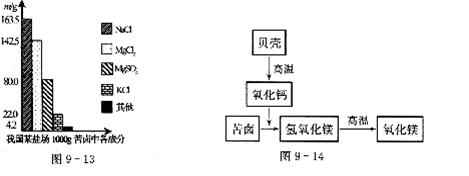
31.苦卤是海水提取食盐后的残液,含有多种成分,在食品、化工等方面有重要应用。如图9-13是我国某盐场苦卤中各成分含量的柱形图。该盐场以苦卤和贝壳为原料按图9-14所示过程生产轻质氧化镁。假设生产过程中镁元素无损失,请计算1000g苦卤可生产氧化镁的质量。
30.中和反应在日常生活和工农业生产中有广泛的应用。某化学兴趣小组的同学在老师的指导下对酸碱中和反应进行了探究。
[提出问题]能否用碳酸钾溶液验证硫酸与氢氧化钠溶液发生中和反应
[实验药品]稀硫酸、稀氢氧化钠溶液、碳酸钾溶液
[实验仪器]试管、滴管、10mL量筒等
[设计方案并实验]小江同学的实验:在试管中加入2 mL稀硫酸,逐滴加入 溶液,振荡后,再滴入V1mL 溶液,实验过程中无气泡逸出。反应的化学方程式为 。
小伟同学的实验:在试管中加入2 mL稀硫酸,逐滴加入氢氧化钠溶液,振荡后,再滴入碳酸钾溶液,有气泡逸出,继续滴加碳酸钾溶液至恰好无气泡时,共消耗碳酸钾溶液V2mL。
小明同学的判断:小江的实验说明能用碳酸钾溶液来验证;小伟的实验还不能,需再做一个实验才能说明。
实验并判断:另取一支试管,加入2 mL稀硫酸,
。(写出实验步骤、现象和判断依据)
[结论]能用碳酸钾溶液验证硫酸与氢氧化钠溶液发生中和反应。
[反思]在小江的实验中,碳酸钾溶液的作用是 (填字母)。
A.仅是反应物 B.相当于指示剂 C.作催化剂
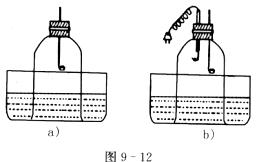
29.小明和小芳在讨论“能否用蜡烛燃烧法来粗略测定空气中氧气的含量”这一问题时,小芳认为:通过图9-12a所示装置,用蜡烛燃烧法测得空气中氧气的含量会 (填“偏高”“偏低”或“不变”)。她根据蜡烛燃烧产物的特点阐述了自己的理由:
,并用图9-12a装置进行实验,证实了自己的结论。(注:本题实验中装置的气密性良好,水槽中的液体是水)
小明认真分析了小芳的实验结果后,进行了如下探究:
[提出问题]导致小芳这一实验结果还有其他原因吗?
[实验探究]小明设计了图9-12b装置,进行以下操作:
(1)取黄豆粒大小的白磷,用滤纸吸去表面的水分,放人捆在电烙铁下面铁片的凹槽内;
(2)将燃烧匙内的蜡烛点燃后迅速插入钟罩内,并立即塞紧橡皮塞;
(3)待蜡烛熄灭后(蜡烛有剩余),接通电烙铁电源,发现白磷先熔成液体,接着燃烧产生大量白烟,说明通电前钟罩内含有 ,产生白烟的化学反应方程式是 。
[得出结论]导致小芳这一实验结果的另一原因是 。
[交流与反思]小明和小芳分析了上述实验后,又提出了一个问题: 。
28.某化学活动小组对实验室制取气体的发生装置进行探究。图9-11是改进后的实验 装置图:
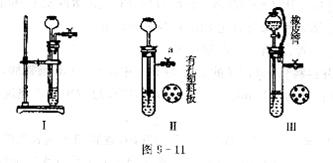
(1)检查装置Ⅱ气密性的方法是 。
(2)小松同学选用装置Ⅱ来制取CO2,现有①Na2CO3固体;②块状大理石;③稀盐酸;④稀硫酸,他应选用的试剂是 。(填序号)
(3)装置Ⅲ中橡皮管的作用是 .
27.某化工厂排出的废水透明、澄清、略显蓝色。一同学取少量废水,加入过量的盐酸,有不溶于稀硝酸的白色沉淀生成。过滤,所得的滤液分成两份,一份滤液中加入稀硫酸,也有不溶于稀硝酸的白色沉淀生成;另一份滤液中加入氢氧化钠溶液,产生蓝色溶液。试回答:
(1)用化学式回答:加入过量的盐酸,生成的白色沉淀是 ;生成的蓝色沉淀是 。
(2)废水中一定含有的物质是 (填编号)
A.氯化物 B.硫酸盐 C.硝酸盐 D.碳酸盐
(3)该同学设计了一个从废水中除去重金属离子的实验方案如图9一10所示[已知白色的Fe(OH)2固体在潮湿的空气中可生成红褐色的Fe(OH)3]。
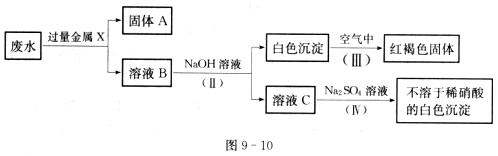
①金属X为 ,固体A中一定含有的物质为(写化学式) 。
②B溶液中的溶质一定含有 和 (填序号字母)。
A.K2CO3 B.Fe(NO3)2 C.MgCl2 D.Ba(NO3)2
③第Ⅳ步反应的化学方程式为 .
26.根据KNO3和NaCl的溶解度曲线(图9-8),回答下列问题:
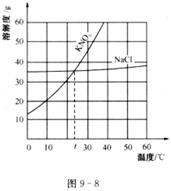
(1)10℃时KNO3的溶解度 (填“>”、“<”或“=”)NaCl的溶解度。
(2)t℃时,将m g KNO3、n g NaCl分别溶解在20 mL水中恰好饱和,则m n(填“>”、“<”或“一”)。
(3)工业上采用如图9-9所示的流程从海水中提取精盐:
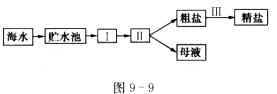
上述流程中I、Ⅱ、Ⅲ分别是 、 、 。
25.利用如图9-7所示装置可进行气体性质的探究实验。甲的玻璃管中盛放黑色粉末(CuO或C),乙的洗气瓶中盛放无色溶液(澄清石灰水或NaOH溶液)。
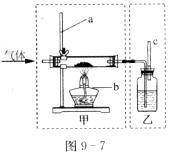
(1)写出仪器的名称:a. ,b. 。
(2)根据要求填表:
|
实 验 |
甲 |
乙 |
|
实验一:探究CO与CuO 的反应。 |
反应的化学方程式: 氧化剂: |
澄清石灰水的作用: |
|
实验二:探究CO2与C的反应。 (b换成酒精喷灯) |
反应的化学方程式: 反应类型: |
NaOH溶液的作用: |
(3)上述两个实验中,在导管c的尖嘴处都用火柴点燃,其目的是否完全相同?简述理由。
24.(1)锂是一种金属单质,化学式为Li,锂原子结构示意图为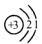 ,易失去最外层一个电子。则锂的氧化物的化学式为
。
,易失去最外层一个电子。则锂的氧化物的化学式为
。
(2)化学反应A B+C,D在反应中作催化剂,12g A与3g D混合后使反应完全生成了8gB,问同时生成
g C。
B+C,D在反应中作催化剂,12g A与3g D混合后使反应完全生成了8gB,问同时生成
g C。
(3)工业酒精中常含有少量甲醇。甲醇有毒,易挥发。请你根据甲醇在氧气中完全燃烧 的产物是CO2和H2O,推断甲醇肯定含有 元素,还可能含有 元素。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com