
(二)岩盐水初步处理后,经净化、精制得到生产碳酸钠所需要的食盐水,同时制取副产品A晶体,其主要流程如下:
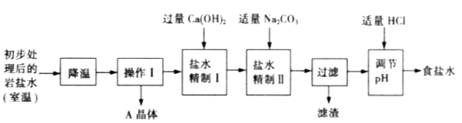
(3)“降温”的目的是析出副产品“A晶体”,A的化学式是________________。
(4)“操作I”中的操作是____________________,若在实验室进行该操作,需要用到的玻璃仪器除烧杯、玻璃棒外,还有______________________________。
(5)“盐水精制I”是除去盐水中的少量氯化镁,反应的化学方程式是________________。
(6)“盐水精制Ⅱ”是除去盐水中的其他杂质,反应的化学方程式是__________________。
(一)原料岩盐水主要含氯化钠,此外还含有较多硫酸钠,以及少量氯化钙和氯化镁。上述几种物质在不同温度时的溶解度数据如下表:
|
温度/℃ |
0 |
10 |
20 |
30 |
40 |
|
|
溶 |
氯化钠 |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
|
解 |
硫酸钠 |
4.5 |
9.6 |
20.2 |
40.8 |
48.4 |
|
度 |
氯化钙 |
59.5 |
65.0 |
74.5 |
100 |
116 |
|
/g |
氯化镁 |
52.9 |
53.8 |
54.8 |
56.0 |
58.0 |
(1)根据所提供的溶解度数据,画出硫酸钠的溶解度曲线。
(2)10℃时由100g水配制得到的饱和硫酸钠溶液中溶质的质量是_________g,溶质的质量分数是____________ (精确到0.1%)。
21.(4分)用化学用语表示下列物质:
(1)氧化钙____________,氯化钡溶于水电离出的离子________________。
(2)1个氮分子__________________________。
(3)某氮的氧化物中氮元素的化合价为+1价,该氧化物是______________________。
22.(4分)现有下列物质:①甲烷 ②氧气 ③硝酸钾 ④碳酸氢钠 ⑤一氧化碳 ⑥二氧化碳 ⑦乙醇 ⑧铁。
(1)属于有机化合物的是(填编号,下同)____________。
(2)属于单质的是____________。
(3)属于氧化物的是____________,属于盐的是____________。
23.(8分)选择“CO”、“CO2”或“稀HCl”填空,并写出有关反应的化学方程式。
(1)能够与氢氧化钠反应的是___________,反应的化学方程式是___________________。
(2)能够把铁从铁矿石(Fe2O3)里还原出来的是___________,反应的化学方程式_______。
(3)能够除去铁制品表面的铁锈(Fe2O3)的是___________,反应的化学方程式是_______。
24.(10分)在当今社会,人类需要的大部分能量都是由化学反应产生的。
(1)下列物质属于化石燃料的是(填写字母编号) ____________。
A.乙醇 B.石油 C.氢气 D.煤
(2)氢气是一种清洁能源,氢气燃烧的化学方程式为__________________,在实验室里可以通过置换反应来制取氢气,写出其中一个化学方程式:________________________。
(3)煤中含有的硫在燃烧时会以二氧化硫的形式排放,污染大气。某工厂有含硫0.8%的煤5000 t,回答下列问题:
①5000 t含硫0.8%的煤中,所含硫的质量为____________;
②二氧化硫的相对分子质量为____________,上述煤如果不经处理直接完全燃烧,产生二氧化硫的质量为____________t;
③二氧化硫可用于生产硫酸,化学方程式为2SO2+O2+2H2O==2H2SO4。参加反应的SO2与生成的H2SO4的质量比是____________,如果将上述SO2全部转化,可得到H2SO4的质量为____________t(精确到0.1)。
25.(10分)某制碱厂以岩盐水为主要原料生产纯碱(碳酸钠)和其他副产品。
20.下列操作可以达到实验目的的是( )
A.用灼烧的方法除去铜粉中混有的木炭粉
B.用测定溶液pH的方法区别食盐水和蒸馏水
C.加入氧化镁除去硫酸镁溶液中含有的少量硫酸
D.通入澄清石灰水除去气体中含有一氧化碳
第Ⅱ卷(非选择题 共60分)
19.氧化镁(MgO)中,镁元素的质量分数是( )
A.30% B.40% C.60% D.70%
18.下列方法能够将石灰水和氢氧化钠溶液区别开的是( )
A.分别滴加紫色石蕊溶液 B.分别通入CO2
C.分别滴加氯化钠溶液 D.分别滴加稀盐酸
17.下列各组溶液,相互能发生反应的是( )
A.碳酸钾和硝酸钡 B.硝酸钡和盐酸
C.氢氧化钠和碳酸钾 D.硫酸钠和碳酸钾
16.下列物质不能导电的是( )
A.澄清石灰水 B.氢氧化钠溶液
C.稀硫酸 D.乙醇
15.下列说法符合事实的是( )
A.铁丝伸入盛有氧气的集气瓶中会剧烈燃烧
B.木炭粉与黑色的氧化铜粉末混合后可看到红色粉末
C.铝放置在空气中不与氧气反应
D.硫燃烧后生成有刺激性气味的气体
14.下列关于金刚石和石墨的说法正确的是( )
A.组成元素都相同 B.原子排列方式都相同
C.都能导电 D.硬度都很大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com