
1£®»¯Ñ§ÒѾÉø͸µ½Éç»á·¢Õ¹µÄ¸÷¸ö·½Ã棬ÔÚ¢Ù»·¾³±£»¤£»¢ÚÄÜÔ´¿ª·¢ÀûÓ㻢ÛвÄÁÏÑÐÖÆ£»¢ÜÉúÃü¹ý³Ì̽Ë÷µÈÁìÓòÖУ¬Ó뻯ѧ¿Æѧ·¢Õ¹ÃÜÇÐÏà¹ØµÄÊÇ(¡¡¡¡ )¡£
¡¡¡¡ A£®Ö»ÓÐ¢Ù¢Ú¢Û ¡¡ B£®Ö»ÓТڢۢܡ¡¡¡ ¡¡¡¡ C£®Ö»ÓТ٢ڢܡ¡¡¡ ¡¡¡¡ D£®¢Ù¢Ú¢Û¢Ü
22£®(7·Ö)ij»¯¹¤³§Óð±¼î·¨Éú²úµÄ´¿¼î²úÆ·Öк¬ÓÐÉÙÁ¿ÂÈ»¯ÄÆÔÓÖÊ£¬Æä²úÆ·°ü×°´üÉÏ×¢Ã÷£ºÌ¼ËáÄÆ¡Ý96%¡£Îª²â¶¨¸Ã²úÆ·Öк¬Ì¼ËáÄƵÄÖÊÁ¿·ÖÊý£¬½øÐÐÁËÒÔÏÂʵÑ飺ȡ11.0g´¿¼îÑùÆ··ÅÈëÉÕ±ÖУ¬³ÆµÃÉÕ±¼°ËùÊ¢´¿¼îÑùÆ·µÄ×ÜÖÊÁ¿Îª158.0g£¬ÔÙ°Ñ100gÏ¡ÑÎËáƽ¾ù·Ö³ÉËÄ·ÝÒÀ´Î¼ÓÈëÑùÆ·ÖУ¬Ã¿´Î¾ù³ä·Ö·´Ó¦¡£ÊµÑéÊý¾Ý¼Ç¼ÈçÏ£º
|
Ëù¼ÓÑÎËáµÄ´ÎÊý |
µÚÒ»´Î |
µÚ¶þ´Î |
µÚÈý´Î |
µÚËÄ´Î |
|
ÉÕ±¼°ËùÊ¢ÎïÖÊ×ÜÖÊÁ¿/g |
181.2 |
204.4 |
228.6 |
253.6 |
ÇëÄã¾Ý´Ë·ÖÎö¼ÆË㣺
(1)µÚÒ»´Î¼ÓÈëÏ¡ÑÎËá³ä·Ö·´Ó¦ºó£¬Éú³É¶þÑõ»¯Ì¼µÄÖÊÁ¿ÊÇ____________g¡£
(2)¸Ã²úÆ·ÖÐ̼ËáÄƵÄÖÊÁ¿·ÖÊýÊÇ·ñºÏ¸ñ?(ÒªÇóд³ö¼ÆËã¹ý³Ì£¬½á¹û¾«È·µ½0.1%)
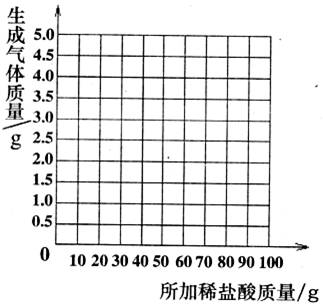
(3)¸ù¾ÝʵÑéÊý¾Ý£¬ÔÚϱߵÄ×ø±êÖ½ÉÏ»æÖƳöËù¼ÓÏ¡ÑÎËáÖÊÁ¿ÓëÉú³ÉÆøÌåÖÊÁ¿¹ØϵµÄÇúÏß¡£(²»ÒªÇóÁмÆËã¹ý³Ì£¬Ö»»³öÇúÏß¼´¿É)
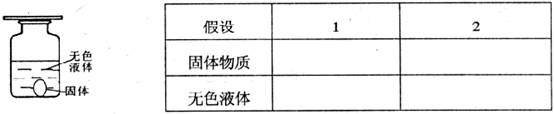
21£®(8·Ö)ijѧУ»¯Ñ§ÐËȤС×éÔÚ»¯Ñ§ÊµÑéÊÒ×öʵÑéʱ£¬¼×°àµÄÍõÃ÷ͬѧ°ÑÒ»ÖÖ°×É«¹ÌÌåºÍÒ»ÖÖÎÞÉ«ÒºÌå»ìºÏ£¬·¢ÏÖ¹ÌÌåÈܽâʱ·Å³öÈÈÁ¿µ«Ã»ÓÐÆøÌå·Å³ö¡£ÒÒ°àµÄÕÅÕýͬѧ°ÑÁ½ÖÖÎÞÉ«ÒºÌå»ìºÏʱ£¬Ò²³öÏÖÁËͬÑùµÄÏÖÏó¡£
¢ÙÇëÄã¸ù¾ÝÍõÃ÷ͬѧµÄʵÑ飬¶ÔÕâÖÖÎÞÉ«ÒºÌåºÍ°×É«¹ÌÌåÌá³öÁ½ÖÖ¼ÙÉè¡£
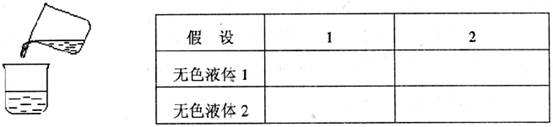
¢ÚÇëÄã¸ù¾ÝÕÅÕýͬѧµÄʵÑ飬ͬÑù¶ÔÕâÁ½ÖÖÎÞÉ«ÒºÌåÌá³öÁ½ÖÖ¼ÙÉè¡£
20£®(14·Ö)ij¹¤³§µÄ·Ïˮֻº¬ÁòËáþºÍÉÙÁ¿ÁòËᣬ¿ÎÍâ»î¶¯Ð¡×éÒÔ´Ë×÷Ϊ¿ÎÌ⣬̽ÌÖÈçºÎ´ÓÖлØÊÕ´¿¾»µÄÁòËáþ¹ÌÌå¡£ËûÃÇÉè¼ÆÁËÁ½ÖÖ²»Í¬µÄ·½°¸£¬ÇëÄã²Î¼ÓÌÖÂÛ£º
(1)·½°¸Ò»£¬Ñ¡ÓÃþ·ÛΪÊÔ¼Á¡£
¢ÙÍù·ÏË®ÖÐÖð´Î¼ÓÈëþ·Û£¬µ±¹Û²ìµ½____________________________________ʱ£¬ËµÃ÷¼ÓÈëþ·ÛµÄÁ¿ÒѾ×ã¹»¡£´Ë¹ý³Ì·¢Éú·´Ó¦µÄ»¯Ñ§·½³ÌʽÊÇ_______________________________£»¢Ú½ÓÏÂÀ´µÄ²Ù×÷·½·¨ÒÀ´ÎÊÇ________________________ºÍ________________________£»
(2)·½°¸¶þ£¬Ñ¡ÓÃÇâÑõ»¯ÄÆÈÜҺΪÊÔ¼Á¡£
¢ÙÏò·ÏË®ÖÐÖðµÎ¼ÓÈëÇâÑõ»¯ÄÆÈÜÒº£¬µ±____________ʱ£¬Í£Ö¹µÎÈëÇâÑõ»¯ÄÆÈÜÒº¡£´Ë¹ý³Ì·¢Éú·´Ó¦µÄ»¯Ñ§·½³ÌʽÊÇ________________________________________________£»
¢ÚΪÁ˵õ½´¿¾»µÄÁòËáþÈÜÒº£¬½Ó×ÅÓ¦½øÐеÄʵÑé²Ù×÷ÊÇ(Çë¼òҪд³ö²Ù×÷¹ý³Ì)
¢Û¡¡£¬µÃµ½ÁòËáþ¹ÌÌå¡£
(3)±È½ÏÁ½¸ö·½°¸£¬¼ÙÉèʵÑéÖж¼Ã»ÓÐËðºÄ£¬ÄÇô£¬×îºóµÃµ½µÄÁòËáþ¹ÌÌåµÄÖÊÁ¿ÊÇ·ñÏàͬ? ____________£¬ÔÒòÊÇ____________________________________¡£
(4)ÇëÄã¼ÌÐø̽¾¿£¬Éè¼Æеķ½°¸(ʹÓõÄÊÔ¼Á±ØÐëÊÇÓëþ·ÛºÍÇâÑõ»¯ÄÆÊô²»Í¬Àà±ð)£ºÄãÑ¡ÓõÄÒ»ÖÖÊÔ¼ÁÊÇ(д»¯Ñ§Ê½) ____________£»¸ÃÊÔ¼Á·¢Éú·´Ó¦µÄ»¯Ñ§·½³ÌʽÊÇ____________¡£
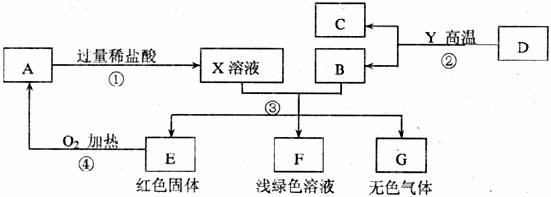
19£®(7·Ö)A¡¢B¡¢C¡¢D¡¢E¡¢F¡¢GΪ³£¼ûµÄÎïÖÊ£¬ÆäÖÐB¡¢E¡¢GÊôÓÚµ¥ÖÊ£¬·´Ó¦¢ÚÊÇÁ¶Ìú¹¤ÒµÖеÄÖ÷Òª·´Ó¦£¬ÏÂͼÊÇËüÃÇÖ®¼äµÄÏ໥ת»¯¹Øϵ¡£Çë»Ø´ð£º
 ¡¡
¡¡
(1)AÎïÖʵĻ¯Ñ§Ê½____________¡£
(2)д³ö·´Ó¦¢ÚµÄ»¯Ñ§·½³Ìʽ____________________________________£»CÎïÖʹÌ̬ʱµÄÃû³Æ____________£¬¸Ã¹ÌÌåÎïÖÊÔÚʵ¼ÊÉú»îÖеÄÒ»ÖÖÓÃ;ÊÇ________________________¡£
(3)д³ö·´Ó¦¢ÛÖÐÉú³ÉºìÉ«¹ÌÌåµÄ»¯Ñ§·½³Ìʽ________________________¡£
(4)ÉÏͼת»¯ÖвúÉúÎÞÉ«ÆøÌåGµÄÔÒòÊÇ____________________________________¡£Ð´³öÎïÖÊGºÍAÔÚ¼ÓÈÈÌõ¼þÏ·´Ó¦µÄ»¯Ñ§·½³Ìʽ____________________________________¡£
18£®(6·Ö)ij¿ÎÍâÐËȤС×飬ȷÁ¢ÁË¡°Ëá¼îÖкÍÉú³ÉµÄÕýÑÎÈÜÒºµÄÐÔÖÊ¡±×÷ΪÑо¿¿ÎÌ⣬ÔÚÑо¿ÖÐËûÃÇ·¢ÏÖ£¬ÕýÑÎËäÈ»²»ÄܵçÀë³öÇâÀë×Ó»òÇâÑõ¸ùÀë×Ó£¬µ«ÊÇÆäÈÜҺȴ²»Ò»¶¨³ÊÖÐÐÔ£¬ÓеijÊËáÐÔ£¬ÓеijʼîÐÔ¡£ÎªÊ²Ã´ÄØ?ÑÎÈÜÒºµÄËá¼îÐÔÓëʲôÓйØÄØ?ÓÉ¡°×é³É¡¢½á¹¹¾ö¶¨ÎïÖÊÐÔÖÊ¡±µÄ¹Ûµã³ö·¢£¬ËûÃÇÓÖ½øÒ»²½´Ó×é³ÉÌØÕ÷ÉÏÈ¥ÕÒÔÒò£¬·¢ÏÖÕýÑÎÈÜÒºµÄËá¼îÐÔÓë¶ÔÓ¦µÄËáºÍ¼îµÄÇ¿ÈõÓйء£ËûÃǽ«ÊµÑé½á¹ûͳ¼ÆÈçÏ£º
|
Ëá |
¼î |
ÏàÓ¦µÄÕýÑÎ |
ÈÜÒºµÄpH |
|
HCl¡¡ (Ç¿Ëá) |
NaOH¡¡ (Ç¿¼î) |
NaCl |
7 |
|
H2SO4¡¡
(Ç¿Ëá) |
KOH¡¡ (Ç¿¼î) |
K2SO4 |
7 |
|
H2CO3¡¡
(ÈõËá) |
NaOH¡¡ (Ç¿¼î) |
Na2CO3 |
>7 |
|
H3PO4¡¡
(ÈõËá) |
KOH¡¡ (Ç¿¼î) |
K3PO4 |
>7 |
|
HNO3 (Ç¿Ëá) |
Cu(OH)2(Èõ¼î) |
Cu(NO3)2 |
<7 |
|
HCl¡¡ (Ç¿Ëá) |
Fe(OH)3 (Èõ¼î) |
FeCl3 |
<7 |
(1)ÇëÄã¸ù¾ÝÉϱí¹éÄɳöÕýÑÎÈÜÒºµÄËá¼îÐÔÓë¶ÔÓ¦Ëá¡¢¼îµÄÇ¿Èõ¹Øϵ£º
(2)¸ù¾ÝËûÃǵķ¢ÏÖ£¬ÇëÄãÅжÏÏõËáÄÆ¡¢ÏõËáÌú¡¢ÁòËáÍ¡¢ÂÈ»¯¼Ø¡¢Á×ËáÄÆ¡¢Ì¼Ëá¼ØÁùÖÖÈÜÒºµÄËá¼îÐÔ£¬ÆäÖÐÈÜÒº³ÊËáÐÔµÄÊÇ____________________________________¡¢³Ê¼îÐÔµÄÊÇ__________________________¡¢³ÊÖÐÐÔµÄÊÇ__________________________¡£
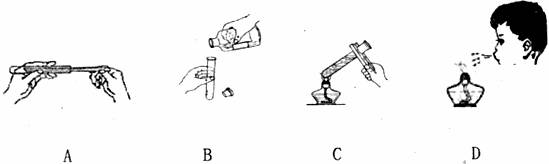
17£®(6·Ö)2007Äê4ÔÂ18ÈÕijÊнøÐоÅÄ꼶»¯Ñ§ÊµÑ鿼²é¡£Ä³Ð¡×éÔÚ¿¼²éʱ³éµ½µÄÌâÄ¿ÊÇ£ºÑõ»¯Í¸úÏ¡ÁòËá·´Ó¦¡£ÒÔÏÂÊǸÃС×éʵÑé²Ù×÷¹ý³ÌµÄʾÒâͼ£º
 ¡¡
¡¡
(1)ÒÔÉÏʵÑé²Ù×÷ÕýÈ·µÄÊÇ(Ìî×Öĸ)__________________¡£
(2)ʵÑéÏÖÏóΪ____________________________________________¡£
(3)ʵÑé½áÂÛ(Óû¯Ñ§·½³Ìʽ±íʾ) ____________________________________________¡£
(4)ÒªÔڹ涨µÄʱ¼äÄÚ˳ÀûµØÍê³ÉʵÑ鿼²é£¬Ð¡×é¸÷³ÉÔ±Ö®¼äÓ¦______________________¡£
16£®(6·Ö)(1)½üÄêÀ´£¬ÈËÃǶ¼ÔÚº°£ºÈÈ¡¢ÈÈ¡¢ÈÈ¡£²»ÉÙ¿Æѧ¼ÒÈÏΪµØÇò±íÃæ±äů¼°Ò»Ð©Òì³£ÆøºòÓë´óÆøÖжþÑõ»¯Ì¼µÄº¬Á¿Ôö¼ÓÓÐÒ»¶¨µÄ¹Øϵ¡£ÏÂÁз´Ó¦¶¼Äܷųö¶þÑõ»¯Ì¼ÆøÌ壬ÊÔ·ÖÎöÅжϣ¬»á¸ø×ÔÈ»½çÔì³É´óÁ¿¡°ÎÂÊÒÆøÌ塱--¶þÑõ»¯Ì¼µÄÖ÷Òª·´Ó¦ÊÇ£º____________(ÌîÐòºÅ)
¢ÙC+O2 ¡¡µãȼ¡¡ ¡¡CO2¡¡ ¢ÚCH4+2CO2 ¡¡µãȼ¡¡ ¡¡CO2+2H2O¡¡
¢ÛCaCO3+2HCl ====CaCl2+CO2¡ü+H2O
¢ÜʯÓÍȼÉÕÖ÷ÒªÉú³ÉË®ºÍ¶þÑõ»¯Ì¼¡¡ ¢Ý2NaHCO3 ¡¡¡÷ ¡¡¡¡Na2CO3+ CO2¡ü+H2O
(2)ÏÂÁз´Ó¦¶¼ÄÜÎüÊÕ¶þÑõ»¯Ì¼ÆøÌ壺
¢ÙCO2+2NaOH==Na2CO3+H2O¡¡ ¢Ú6CO2+6H2O==C6H12O6(ÆÏÌÑÌÇ)+6O2¡ü(¹âºÏ×÷ÓÃ)
¢ÛCO2+H2O== H2CO3
ÊÔÅжϣºÈôÒª¼õÉÙ´óÆøÖеĶþÑõ»¯Ì¼ÆøÌ壬¿ÉÀûÓõķ´Ó¦ÊÇ£º_____________(ÌîÐòºÅ)
(3)¸ù¾Ý¶Ô(1)ºÍ(2)µÄ·ÖÎö£¬ÄãÈÏΪ£¬Îª±£»¤ÈËÀàÀµÒÔÉú´æµÄµØÇò£¬ÎÒÃÇÓ¦²ÉÈ¡ÄÄЩ´ëÊ©¿ÉÒÔ·ÀÖ¹´óÆøÖжþÑõ»¯Ì¼º¬Á¿µÄÔö¼Ó?
15£®(4·Ö)ËÕµ¤ºìÊÇÒ»ÀàȾɫ¼Á¡£ÔÚÎÒÃÇÈÕ³£½Ó´¥µÄÎïÆ·ÖУ¬¼ÒÓõĺìÉ«µØ°åÆá»òºìɫЬÓÍͨ³£º¬ÓÐËÕµ¤ºìµÄ³É·Ö¡£¸ù¾Ý2004Äê4ÔÂMSDSÌṩµÄÊý¾Ý£¬ËÕµ¤ºì´æÔÚÓÐÏÞµÄÖ°©×÷Ó㬲»¿É·þÓá£2005Äê2ÔÂ23ÈÕÖйúÕþ¸®·¢²¼½ô¼±¹«¸æ£¬½ûÖ¹ËÕµ¤ºì×÷ΪʳƷÌí¼Ó¼Á¡£Ï±íÊÇËÕµ¤ºìÒ»ºÅµÄÓйØÐÅÏ¢£º
|
񅧏 |
»¯Ñ§Ê½ |
C16H12N2O |
|
¢Ù |
Íâ¹Û |
°µºìÉ«»òÉî»ÆɫƬ״¾§Ìå |
|
¢Ú |
Èܽâ¶È |
ÔÚË®ÖУº<0.01g/100ml£»ÔÚÆûÓÍÖУºÈÎÒâ±ÈÀý»¥ÈÜ |
|
¢Û |
ÈÛµã |
404-406¡æ |
|
¢Ü |
Éý»ª |
475¡æ |
|
¢Ý |
ÖÂÍ´ÔÒò |
ÔÚÈËÌåÄÚ·Ö½â³öÒ»ÖÖÓж¾µÄÓлúÎï(±½°·) |
ÊԻشðÏÂÁÐÎÊÌ⣺
(1)ËÕµ¤ºìÒ»ºÅÖк¬ÓÐ____________-ÖÖÔªËØ£¬ÆäÏà¶Ô·Ö×ÓÖÊÁ¿Îª____________¡£
(2)ÔÚÉϱí¸ø³öµÄÐÅÏ¢ÖУ¬ÊôÓÚËÕµ¤ºìÒ»ºÅÎïÀíÐÔÖʵÄÓÐ(Ìî±àºÅ) ____________¡£
(3)ËÕµ¤ºìÒ»ºÅ¶Ô¶¯ÎïºÍÈËÌåÓÐÖ°©×÷Óã¬Ö÷ÒªÊÇÒòΪ¸ÃÎïÖÊÔÚÌåÄÚ·¢ÉúÁË__________±ä»¯¡£
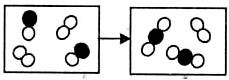
14£®¡¢ÏÂͼΪ¼×(¡ñO)ÓëÒÒ(OO)·´Ó¦Éú³É±û(O¡ñO)µÄ΢Á£Êý±ä»¯Ê¾Òâͼ£¬ÔòÏÂÁÐ˵·¨ÕýÈ·µÄÊÇ
 ¡¡
¡¡
¡¡ A£®¼×Ò»¶¨ÊÇÑõ»¯Îï¡¡¡¡¡¡¡¡ B£®ÓÒ¿òͼµÄÎïÖÊÊÇ´¿¾»Îï
¡¡ C£®¸Ã·´Ó¦ÀàÐÍÊǷֽⷴӦ¡¡¡¡ D£®¼×¡¢ÒÒ¡¢±ûµÄ»¯Ñ§¼ÆÁ¿ÊýÖ®±ÈΪ2:1:2
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com