
 2NaHCO3 Na2CO3+CO2↑+H2O
2NaHCO3 Na2CO3+CO2↑+H2O
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是 (填字母标号)。
a.碳酸氢钠难溶于水 b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验。
① 一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。
22.(12分)我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:NH3+CO2+H2O NH4HCO3 ;
NH4HCO3+NaCl NaHCO3↓+NH4Cl ;
21.(12分)A、B、C是中学化学中常见的三种短周期元素。已知①A元素原子最外层电子数是次外层电子数的2倍。②B元素最高正价与负价的代数和为2。③C元素有多种化合价,且常温下C元素的单质与某种一元碱溶液反应,可得到两种含C元素的化合物。④B、C两种元素质子数之和是A元素质子数的4倍。
( 1 ) 写出A、B、C三种元素的名称:A B C
( 2 ) 写出C的单质和强碱溶液反应的离子方程式 。
(3)由B、C两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X子为三角锥形分子,且分子里B、C两种原子最外层均达到8个电子的稳定结构。X遇水蒸气可形成一种常见的漂白性物质。则X的分子式 。分子中B、C原子间的化学键的类型为 。(填“极性键”或“非极性键”)X与水反应的化学方程式 。
(4)A、B两种元素可形成一种硬度比金刚石还大的化合物Y。在化合物Y中,A、B两原子以单键相结合,且每个原子的最外层均达到8个电子的稳定结构。则Y的化学式为 , Y的硬度比金刚石硬度大的原因是 。
20.硝酸铵(NH4NO3)在不同条件下分解可以得到不同的产物,下列各组物质中肯定不可能是硝酸铵分解产物的是
A.N2O、H2O B.N2、O2、H2O
C.N2、HNO3、H2O D.NH3、NO、H2
2007高三化学周考测试题
第Ⅱ卷(非选择题,共40分)
题号
1
2
3
4
5
6
7
8
9
10
答案
题号
11
12
13
14
15
16
17
18
19
20
答案
A.V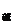 = 102 V
= 102 V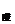 B.V
B.V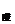 = 102V
= 102V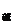 C.V
C.V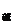 =2V
=2V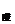 D.V
D.V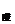 =2 V
=2 V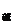
19、室温下,某强酸溶液pH = a,某强碱溶液pH = b,已知a
+ b = 12,且两溶液混合后溶液pH = 7。则该强酸溶液的体积V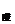 与强碱溶液的体积V
与强碱溶液的体积V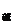 的正确关系为
的正确关系为
D.Ca2+的结构示意图为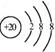 ,NH4Cl的电子式为
,NH4Cl的电子式为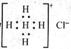
18.正确掌握化学用语和化学基本概念是学好化学的基础。下列有关表述中正确的一组是
A.过氧乙酸(CH3COOOH)与羟基乙酸(HOCH2COOH)所含官能团相同;两者互为同分异构体
B.16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体
C.P4、CH4、NH4+粒子的空间构型均为正四面体型;CO2、C2H2均为直线型分子
17.从海水中提取镁,可按如下步骤进行:
①把贝壳制成石灰乳; ②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物; ③将沉淀物与盐酸反应,结晶过滤、在HCl气体氛围中干燥产物; ④将得到的产物熔融电解得到镁。下列说法不正确的是
A.此法的优点之一是原料来源丰富
B.①②③步骤的目的是从海水中提取MgCl2
C.以上提取镁的过程中涉及化合、分解和复分解反应
D.第④步电解时阴极产生氯气
 Z
Z
例
氧化物
化合物
纯净物
A
苯的同系物
芳香烃
芳香族化合物
B
胶体
分散系
混合物
C
电解质
离子化合物
化合物
D
碱性氧化物
金属氧化物
氧化物
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com