
1£®½šŹōÄĘ²»½öøśŃõĘų”¢Ė®µČĪŽ»śĪļ·“Ó¦£¬»¹ÄÜøś¾Ę¾«”¢“×ĖįµČÓŠ»śĪļ·“Ó¦”£ŅŖŃŠ¾æ½šŹōÄĘøś¾Ę¾«·“Ó¦µÄŠŌÖŹŅŌ¼°ĖüÓėĖ®·“Ó¦µÄŅģĶ¬µć£¬ĻĀĮŠŃŠ¾æ·½·Ø֊ƻӊÓƵ½µÄŹĒ
”””” A£®ŹµŃé·Ø”””””””” B£®¹Ū²ģ·Ø”””””””” C£®·ÖĄą·Ø”””””” D£®±Č½Ļ·Ø
31£®(6·Ö)½šŹōĪż(Sn)µÄ“æ¶ČæÉŅŌĶعżĻĀŹö·½·Ø·ÖĪö£ŗ½«ŹŌŃłČÜÓŚŃĪĖį£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗSn+2HC1=SnC12+H2”ü£¬ŌŁ¼ÓČė¹żĮæFeC13ČÜŅŗ£¬·¢ÉśČēĻĀ·“Ó¦£ŗSnC12+2FeC13=SnC14+2FeC12×īŗóÓĆŅŃÖŖÅضČK2Cr2O7cyČÜŅŗµĪ¶ØÉś³ÉµÄFe2+Ąė×Ó£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ
”” 6FeC12+K2Cr2O7+14HC1=6FeC1+2CrCl32KC13+7H2O
”” ĻÖÓŠ½šŹōĪżŹŌŃł0.613æĖ£¬¾ÉĻŹöø÷²½·“Ó¦ŗ󣬹²ÓĆČ„0.100mol/LK2Cr2O7ČÜŅŗ16.0ŗĮÉż£¬ĒóŹŌŃłÖŠĪżµÄ°Ł·Öŗ¬Įæ(¼Ł¶ØŌÓÖŹ²»²Ī¼Ó·“Ó¦)”£
30£®(6·Ö)400K”¢101.3kPaŹ±,L1.5LijĢžÕōĘųÄÜŌŚaLŃõĘųÖŠĶźČ«Č¼ÉÕ,Ģå»żŌö“óÖĮ(a+3)L (Ķ¬ĪĀĶ¬Ń¹ĻĀ²ā¶Ø)”£
”” (1)øĆĢžŌŚ×é³ÉÉĻ±ŲŠėĀś×ćµÄĢõ¼žŹĒ””””””””””””””””””””””””””””””””””””””””””””””
”” (2)µ±a = 10LŹ±£¬øĆĢžæÉÄܵķÖ×ÓŹ½ĪŖ””””””””””””””””””””””””””””””””””””””””””””
”” (3)µ±øĆĢžµÄČĖ×ÓŹ½ĪŖC7H8Ź±£¬aµÄȔֵ·¶Ī§ĪŖ”””””””””””””””””””””””””””””””” ”£
29£®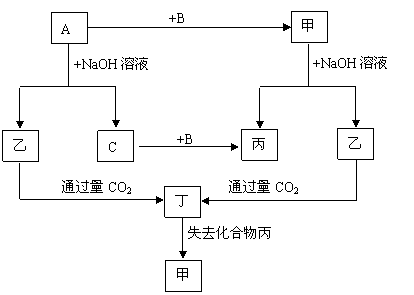 (4·Ö)ĻĀĮŠø÷µ„ÖŹ(A”¢B”¢C)ŗĶ»ÆŗĻĪļ(¼×”¢ŅŅ”¢±ū”¢¶”)
(4·Ö)ĻĀĮŠø÷µ„ÖŹ(A”¢B”¢C)ŗĶ»ÆŗĻĪļ(¼×”¢ŅŅ”¢±ū”¢¶”)
Ö®¼äÓŠŅŌĻĀµÄ×Ŗ»Æ¹ŲĻµ£¬¶ųĒŅø÷µ„ÖŹŗĶ»ÆŗĻĪļµÄ×é³ÉŌŖĖŲ½ŌĪŖ¶ĢÖÜĘŚŌŖĖŲ”£
ŹŌĶʶĻø÷»ÆŗĻĪļµÄ»ÆѧŹ½ĪŖ£ŗ
¼×”””””””” ”¢”¢ŅŅ”””””””” ”¢”¢±ū ”””””””””¢”¢¶””””””””” ”¢”£
28£®(10·Ö)A”¢B”¢C”¢D”¢EĪåÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬ĖüĆĒµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£»AŌŖĖŲµÄŌ×ÓŹĒ°ė¾¶×īŠ”µÄŌ×Ó£»BŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļÓėĘäĒā»ÆĪļ·“Ӧɜ³ÉŅ»ÖÖŃĪX£»DÓėAĶ¬Ö÷×壬ĒŅÓėEĶ¬ÖÜĘŚ£»EŌŖĖŲµÄ×īĶā²ćµē×ÓŹżŹĒĘä“ĪĶā²ćµē×ÓŹżµÄ3/4±¶”£A”¢B”¢D”¢EÕāĖÄÖÖŌŖĖŲ£¬ĆæÖÖÓėCŌŖĖŲ¶¼ÄÜŠĪ³ÉŌŖĖŲµÄŌ×ÓøöŹż±Č²»ĻąĶ¬µÄČōøÉÖÖ»ÆŗĻĪļ”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
”” (1)Š“³öB”¢C”¢D”¢EŌŖĖŲµÄŌŖĖŲ·ūŗÅ£ŗB”””””””” ””C”””””””” ””D”””””””” E”””””””” ””
”” (2)A”¢B”¢C”¢EĖÄÖÖŌŖĖŲæÉŠĪ³ÉĮ½ÖÖĖįŹ½ŃĪ£¬ÕāĮ½ÖÖĖįŹ½ŃĪµÄ»Æ²»Ź½ĪŖ”””””” ”¢”¢”””””” ”¢£»ÕāĮ½ÖÖĖįŹ½ŃĪŌŚČÜŅŗÖŠĻą»„·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ””””””””””””””””””””””””””
”” (3)ÓÉA”¢C”¢DČżÖÖŌŖĖŲŠĪ³É»ÆŗĻĪļµÄµē×ÓŹ½ĪŖ”””””””””””””””” ””£¬ĘäÖŠŗ¬ÓŠµÄ»Æѧ¼üĪŖ”””””””””””””””””””””””””””””””””””””””””””””””””””””””””””” ””
”” (4)ÓƵē×ÓŹ½±ķŹ¾»ÆŗĻĪļA2EµÄŠĪ³É¹ż³Ģ””””””””””””””””””””””””””””””””””””””””””
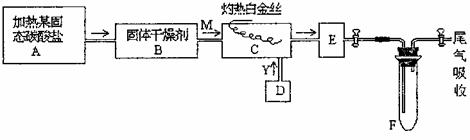
27£®(8·Ö)ij»ÆѧæĪĶāŠ”×éĖł×öŹµŃéµÄŹ¾ŅāĶ¼ČēĻĀ£ŗ
 ””
””
ÉĻĶ¼ÖŠ”°”ś”±±ķŹ¾ĖłĢåĮ÷Ļņ£¬MŹĒŅ»ÖÖ“æ¾»¶ųøÉŌļµÄĘųĢ壬YĪŖĮķŅ»ÖÖĘųĢ壬EÄŚÓŠ×ŲÉ«²śÉś£¬ŹµŃéĖłÓƵÄĪļÖŹ£¬Ö»ÄÜÓÉĻĀĮŠĪļ֏֊єȔ£ŗ
”””” Na2CO3”¢Na2O2”¢NaCl”¢Na2O”¢CaC12”¢(NH4)2CO3”¢¼īŹÆ»Ņ¹ĢĢå¼°ÕōĮóĖ®£¬¾Ż“ĖŹµŃ飬Ķź³ÉĻĀĮŠĢīæÕ£ŗ
(1)AÖŠĖłÓĆ×°ÖƵÄÖ÷ŅŖŅĒĘ÷ÓŠ”””””””””””””””””””””””””””””””””””””””””””””””” ”£
(2)BÖŠĖłŃ”µÄøÉŌļ¼ĮŹĒ”””””””””” Ęä×÷ÓĆŹĒ”””””””””””””””””””””””””””””””””””” ”£
(3)CÖŠ·¢ÉśµÄÖ÷ŅŖ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ”””””””””””””””””””””””””””””””””””””””” ”£
(4)D×°ÖĆÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ”””””””””””””””””””””””””””””””””””””””””” ”£
26£®(6·Ö)ŹµŃéŹŅŠčŅŖÅäÖĘ1.0mol/LĮņĖįČÜŅŗ500mL£¬øł¾ŻČÜŅŗÅäÖĘĒéæö»Ų“šĻĀĮŠĪŹĢā£ŗ
”” (1)ŹµŃéÖŠ³żĮĖÉÕ±”¢ĮæĶ²Ķā»¹ŠčŅŖµÄĘäĖüŅĒĘ÷ÓŠ£ŗ”””””””””””””””””””””””””” ”£
”” (2)øł¾Ż¼ĘĖćµĆÖŖ£¬ĖłŠčÖŹĮæ·ÖŹżĪŖ98%”¢ĆܶČĪŖ1.84g/cm3µÄÅØĮņĖįĢå»żĪŖ”””””” mL”£”””””””””””””””””””””””””””””””””””””””””””””””””” (¼ĘĖć½į¹ū±£ĮōŅ»Ī»Š”Źż)
”” (3)ÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅضČČÜŅŗµÄŹµŃéÖŠ£¬Čē¹ū³öĻÖŅŌĻĀ²Ł×÷£ŗ
”””””””” A£®ĮæČ”ÅØĮņĖįµÄĮæĶ²ÄŚÓŠÉŁĮæÉŁ£»
”””””””” B£®ÅØĮņĖįŌŚÉÕ±ÖŠČܽāŗó£¬Ī“¾ĄäČ“¾ĶĮ¢¼“×ŖŅʵ½ČŻĮæĘæÖŠ£»
”””””””” C£®×”ČŻĮæĘæ×ŖŅĘŹĒ£¬ÓŠÉŁĮæŅŗĢ彦³ö
”””””””” D£®½«ĮæĶ²Ļ“µÓŗóĻ“µÓŅŗŅ»²¢×ŖČėČŻĮæĘæ
”””””””” E£®¶ØČŻŹ±ŃöŹÓæĢ¶ČĻß
”””””””” F£®ČŻĮæĘæĪ“øÉŌļ¼“ÓĆĄ“ÅäÖĘČÜŅŗ
”””””””” G£®¶ØČŻŗóČūÉĻĘæČū·“ø“Ņ”ŌČ£¬¾²ÖĆŗó£¬ŅŗĆę²»µ½æĢ¶ČĻߣ¬ŌŁ¼ÓĖ®ÖĮæĢ¶ČĻß”£
”””””””” ¶ŌÅäÖʵÄČÜŅŗĪļÖŹµÄĮæÅØ¶Č“óŠ”æÉÄÜŌģ³ÉµÄÓ°ĻģŹĒ(ĢīŠ“×ÖÄø)
”””””””” Ę«“óµÄÓŠ”””””””””””””””” £»ĪŽÓ°ĻģÓŠ””””””””””””””””””””””
25£®µČĪļÖŹµÄĮæµÄÖ÷×彚ŹōA”¢B”¢C·Ö±šÓė×ćĮæµÄĻ”ŃĪĖį·“Ó¦£¬ĖłµĆĒāĘųµÄĢå»żŅĄ“ĪĪŖVA”¢VB”¢VC£¬ŅŃÖŖVB=2VC£¬ĒŅVA=VB+VC£¬ŌņŌŚCµÄÉś³ÉĪļÖŠ£¬øĆ½šŹōŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ(”””” )
”” A£®+1”””””””””””””” B£®+2”””””””””””” C£®+3”””””””””””””” D£®+4
µŚ¢ņ¾ķ(·ĒŃ”ŌńĢā”” ¹²40·Ö)
24£®2mol/LµÄŃĪĖįÓė2mol/LµÄĮņĖįø÷100mL£¬·Ö±š¼ÓČėµČÖŹĮæµÄĢś·Ū£¬·“Ó¦½įŹųŗó£¬ĖłµĆĘųĢåÖŹĮæĪŖ2£ŗ3£¬ŌņĶłŃĪĖįÖŠ¼ÓČėĢś·ŪµÄÖŹĮæĪŖ”””””””””””””””””””” (”””” )
”” A£®2.8g”””””””””””” B£®5.6g”””””””””” C£®8.4g”””””””””””” D£®11.2g
23£®ŌŚĶ¬Ņ»Ģõ¼žĻĀ£¬Ģå»żĻąĶ¬µÄČżøöÉÕĘæÖŠ·Ö±šŹ¢ÓŠNH3”¢HC1”¢NO2ĘųĢ壬²¢·Ö±šµ¹Į¢ŌŚĖ®²ŪÖŠ£¬³ä·Ö·“Ó¦ŗó£¬ÉÕĘæÄŚČżÖÖČÜŅŗµÄĪļÖŹµÄĮæÅضČÖ®±ČĪŖ(ÉčÉÕĘæÖŠµÄČÜŅŗĪ“Ą©É¢µ½Ė®²ŪĄļ)”””””””””””””””””””””””” (”””” )
”” A£®1£ŗ1£ŗ1”””””””” B£®2£ŗ2£ŗ3”””””” C£®3£ŗ3£ŗ2”””””””” D£®2£ŗ2£ŗ1
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com