
7.已知0.1mol/L的醋酸溶液中存在电离平衡: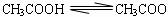 -+H+要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是 ( )
-+H+要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是 ( )
A.加少量烧碱溶液 B.升高温度
C.加少量冰醋酸 D.使用催化剂
6.下列离子方程式书写正确的是 ( )
A.铝与烧碱溶液反应:Al+2OH-=AlO2-+H2↑
B.碳酸钙与醋酸反应:CaCO3+2H+=Ca2++CO2↑+H2O
C.CO2气体通入次氯酸钙溶液中:CO2+2ClO-+H2O=CO32-+2HClO
D.氯化铁溶液呈酸性:
5.下列各条件下可能共存的离子组是 ( )
A.某无色溶液中:NH4+、Na+、Cl-、MnO4-
B.由水电离出的c(H+)=1×10-13mol·L-1的溶液中:Na+、、K+、SO32-、CO32-
C.在c(H+)=11×10-13mol·L-1的溶液中:NH4+、Al3+、SO42-、NO3-
D.在pH=1的溶液中:K+、Fe2+、Cl-、NO3-
4.用NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.0.2mol过氧化氢完全分解转移的电子数目为0.4NA
B.1mol C8H18中含有的共价键为26NA
C.在常温常压下,17g硫化氢所含质子数目为8NA
D.在标准状况下,2.24L二氧化硫与氧气混合气体中所含氧原子数为0.2NA
3.下列事实不能用勒夏特列原理解释的是 ( )
A.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率
B.将FeCl3溶液加热蒸干最终得不到FeCl3固体
C.实验室用排饱和食盐水的方法收集氯气
D.经粉碎的黄铁矿在沸腾炉中燃烧得较快、较完全
2.下列实验方法正确的是 ( )
A.用渗析的方法精制氢氧化铁胶
B.加入适量NaOH溶液后过滤,以除去KCl溶液中少量的MgCl2
C.测定溶液pH,用玻璃棒蘸取原溶液点在润湿的pH试纸上立即与比色卡比较
D.测定硫酸铜晶体中结晶水含量,实验过程中至少需要三次称量
1. 判断下列有关化学基本概念的依据正确的是 ( )
A.氧化还原反应:元素化合价是否变化
B.共价化合物:是否含有共价键
C.强弱电解质:溶液的导电能力大小
D.金属晶体:晶体是否能够导电
24.(16分)电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a:X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
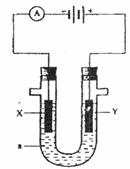
(1)若X、Y都是惰性电极,a是饱和NaC1溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为 。
在X极附近观察到的现象是 。
②Y电极上的电极反应式为 ,
检验该电极反应产物的方法是 。
(2)如用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 ,电极反应式为 。
②Y电极的材料是 ,电极反应式为 。(说明:杂质发生的电极反应不必写出)
23.(8分)实验室常用的几种气发生装置如下图所示:
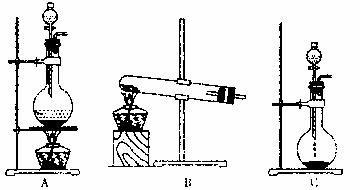
(1)实验室利用氧化钙氨水制取氨气,应选装置 ;控制氨气生成的操作为 。
(2)现有两种方法制取氨气,可供选用的药品有:KC1O3、Na2O2、NaOH、H2O、Na2CO3、MnO2。
第一种方法是选择装置B,则需选用的试剂为 ;
第二种方法是选择装置C,则需选用的试剂为 。
(3)若把A装置与下图装置相连,在实验室可用来制取下列气体中的 (填序号)。
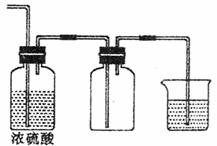
①HC1 ②NO ③C12
制取这种气体时,除选用(2)所供几种药品外,还需要的一种试剂是 。
图4-4小烧杯中盛的试剂是 。其作用是 。
22.(16分)现用U型管(用硬质玻璃管弯制)、干燥管、酒精灯、胶塞和玻璃导管等仪器设计右图装置来证实稀稍酸与铜反应生成NO。
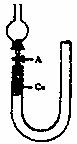
(1)补充完成下列实验步骤:
①检查装置的气密性,方法是 。
②打开活塞A,从U形管长管一端注入稀硝酸,一直注到 为止。
③关闭活塞A,用酒精灯在U型管短管一侧加热,当观察到 现象时,立即停止加热原因: 。
(2)记录描述观察到的实验现象:
①可在U型管短管上方处观察到 色气体产生。若铜丝和稀硝酸均未完全反应,在 时反应也可自行停止。
②反应自行停止后,如果慢慢打开活塞A,可立即观察 ,以上现象说明 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com