
4.当前中央提出“大力抓好节能减排、保护环境”,下列措施与这一主题不吻合的是( )
A.推广燃烧脱硫技术,防止SO2污染
B.推广垃圾的分类存放、回放、处理
C.大量使用农药、化肥提高粮食产量
D.采用“绿色化学”工艺,减少副产物
3.在0.5L某浓度的NaC1溶液中含有0.5mol·Na+,下列对该溶液的说法中,不正确的是
( )
A.该溶液的物质的量浓度为1mol·L-1
B.该溶液中含有58.5g NaC1
C.配制100mL该溶液需用58.5g NaC1
D.量取100mL该溶液倒入烧末中,烧杯中C1的物质的量为0.1mol
2.某同学效游不慎被蜜蜂蛰伤,已知蜜蜂蛰人时分泌的液体是酸性的。该同学随身携带的物品有苹果汁、牛奶、矿泉水和香皂等,其pH分别为a、b、c、d(如图所示,d为香皂水的pH),为了减轻蛰伤处的疼痛,应涂沫 ( )
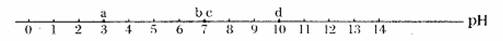
A.苹果汁 B.牛奶 C.矿泉水 D.香皂水
1.诗句“春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别指 ( )
A.纤维素,脂肪 B.蛋白质,烃
C.淀粉,油脂 D.蛋白质,硬化油
26.(6分)
(1)宇宙飞船上的氢氧燃料电池,其电池反应为:2H2+O2=2H2O试写出电解质溶液若为盐酸时的正极反应式:__________________________________________。
(2)已知4g甲烷气体充分燃烧生成CO 2(气体)和H2O(液)时,放出Q kJ的热量。写出甲烷燃烧热的热化学方程式:___________________________________________。
(3)已知下列热化学方程式:
①.Fe2O3(s) + 3CO(g) = 2Fe(s) + 3CO2(g) △H= -Q1kJ/mol
②.3Fe2O3(s) + CO(g) = 2Fe3O4 (s) + CO2(g) △H= -Q2kJ/mol
③. Fe3O4(s) + CO(g) = 3FeO(s) + CO2(g) △H= -Q3kJ/mol
利用盖斯定律计算:FeO(s) + CO (g)= Fe(s) + CO2(g) 的焓变△H=______________。
25.(16分)某化学小组的同学进行研究性学习时,决定自己动手探究NO2能否支持燃烧的问题。
(1)甲组同学设计的方案是:向烧瓶中加入适量的浓硝酸并加热,当烧瓶中有红棕色气体产生之后,将燃着的木条伸入烧瓶中,发现木条火焰熄灭。
①.写出浓硝酸受热分解的化学方程式:__________________________________。
②.根据甲组同学设计的方案,能不能得出NO2不支持燃烧的结论?___________(填能或不能)。推断的理由是:____________________________________________
___________________________________________________________________。
③.当烧瓶中充满红棕色气体时,将带火星的木条伸入烧瓶中,木条复燃了。有同学得出NO2能支持木条燃烧的结论。你认为这一结论是否正确?_____________(填正确或不正确)。理由是:________________________________________________
___________________________________________________________________。
(2)乙组同学通过查资料得知,某些不活泼金属的硝酸盐受热时也能产生NO2气体。
例如:2Cu(NO3) 2 2CuO
+4NO 2↑+O 2↑,2AgNO3
2CuO
+4NO 2↑+O 2↑,2AgNO3 2Ag
+2NO 2↑+O 2↑。他们根据此原理设计如图甲所示的实验装置(加热、夹持仪器未画出),并分别用硝酸铜和硝酸银进行实验,实验中发现当红棕色气体进入集气瓶后,带火星的木炭均能复燃,乙同学由此得出NO2支持燃烧的结论。
2Ag
+2NO 2↑+O 2↑。他们根据此原理设计如图甲所示的实验装置(加热、夹持仪器未画出),并分别用硝酸铜和硝酸银进行实验,实验中发现当红棕色气体进入集气瓶后,带火星的木炭均能复燃,乙同学由此得出NO2支持燃烧的结论。
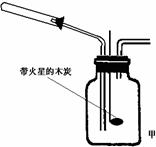
①.乙组同学使用该装置进行实验时,从环保的角度考虑。应采取的措施是:____________________________。
②.指导老师认为乙组同学进行的两个实验中,有一个实验所得结论是不可靠的。你认为不可靠的实验选用的反应物是:____________,该实验所得结论不可靠的原因是:
________________________________________________________________。
24.(14分)根据下列题目要求,回答下列问题:
(1)硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离。事实上,硫酸的第一步电
离是完全的:H2SO4= H++ HSO4-,第二步电离并不完全:HSO4- 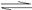 H++ SO42- 。
H++ SO42- 。
①.则Na2SO4溶液呈__________(填弱酸性、中性或弱碱性),其理由是(用离子方程式表示)______________________________________________。
②.写出硫酸与氯化钡溶液反应的离子方程式:______________________________。
(2)在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝,有关反应的离子方程式是:_____________________________________________;
在上述溶液中加入足量的亚硫酸钠溶液,蓝色逐渐消失,有关反应的离子方程式是:___________________________________________________________。
(3)把氯化亚铁水溶液中的Fe2+氧化为Fe3+,而不引进金属阳离子或其它原溶液中不含有的阴离子,所用的两种方法的离子方程式分别为:
①.______________________________________________________;
②.______________________________________________________。
23.(4分)如图所示的装置,实验前a、b、c活塞均关闭。
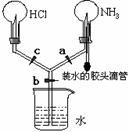
(1)要在该装置中产生喷烟现象,其操作方法是:
。
(2)若要在该装置中产生双喷泉现象,其操作方法是:
。
22.(6分)根据题目要求回答下列问题:
(1)化学实验时,下列处理方法不正确的是__ ______ _(少选得一半的分,错选不得分)
A.金属钠失火,用泡沫灭火器扑灭
B.用瓷坩埚熔融氢氧化钠或碳酸钠固体
C.用滴有酚酞的水做喷泉实验,只验证了氨气的溶解性
D.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼
E.温度计的水银球破裂后,掉在地上的水银应用洒硫粉的方法除去
F.实验桌上的酒精灯失火后,立即用湿抹布盖灭
G.配制FeCl2溶液先将FeCl2溶解在盐酸中,再加入蒸馏水稀释,最后加少量铁粉
(2)就教材中氢氧化铁胶体的制备实验中应该注意的事项,回答:向沸水中滴加饱和氯化铁溶液,稍微加热煮沸,不宜长时间加热。这样操作的原因是:
__________________________________________________________________。
(3)在100ml的混合溶液中硝酸和硫酸的物质的量浓度分别是0.4mol/l和0.1mol/l,向该混合溶液中加入1.92g铜粉,所得溶液中Cu2+的物质的量浓度为:________。
21.(4分)某溶液由Na+、Cu2+、Ba2+ 、Fe3+、 AlO2-、CO32- 、SO42-、Cl-中的若干种离子组成。
取适量该溶液进行如下实验:
①向其中加入过量盐酸,有气体生成,并得到无色透明溶液;
②向①所得的溶液中加入过量氨水,产生白色沉淀,过滤;
③向②所得的溶液中加入过量氢氧化钡溶液,产生白色沉淀,过滤;
④向③所得的滤液中加入过量稀硝酸,再加入硝酸银溶液,产生白色沉淀。
根据上述实验回答下列问题:
(1)原溶液一定不存在的离子是:_____________________________________;
(2)原溶液一定存在的离子是:______________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com