
9.FeS2结构类似于Na2O2,与酸反应时生成H2S2,H2S2类似于H2O2,易分解。实验室用稀盐酸制取H2S时,某学生误将FeS2颗粒当作FeS使用,当FeS2反应完后,不可能生成的物质是:
A.H2S B.S C.FeS D.FeCl2
|
A.无色透明的溶液中: K+、Ba2+ 、I-、 MnO4-
B.含有大量NO3-的溶液中: NH4+ 、Fe2+ 、SO42- 、H+
C.c(HCO3-)=0.1mol/l的溶液中: K+ 、Na+、 Br-、 CO32-
D.强碱性溶液中: ClO- 、 S2- 、 HSO3-、 Na+
8.A、B为短周期元素,二者能组合形成多种我们所熟知的化合物。在这些化合物中,A与B的原子个数比为A:B=1:2。已知A的原子序数为n ,B的原子序数是①n+2 ②n+3 ③n+4④n+5 ⑤n+8 ⑥n-5 ⑦ n-7⑧n-8中的几种,其中不符合题目要求的是 ( )
A.①④ B.②⑧ C.③⑤ D.⑥⑦
7.将1.92g铜粉投入到一定量的浓硝酸中反应,当铜完全作用时,生成的气体颜色越来越浅,共收集到气体672ml(标况下),将盛有此气体的容器倒扣在水槽中,通入标准状况下的一定体积的氧气,恰好使气体完全溶于水,则所通入氧气的体积为 ( )
A.504ml B.336ml C.224ml D.168ml
6.某同学为了探索镁粉与溴水反应的机理,做了如下四组实验:
①将镁粉投入冷水中,未见任何现象;
②将镁粉投入溴水中,观察到只是开始时产生极少量的气泡,但溴水的颜色全逐渐褪色;
③将镁粉投入液溴中,未观察到任何明显现象;
④向含足量镁粉的液溴中滴加几滴水,观察到溴的红棕色很快褪去。关于镁与溴水的反
应机理的论述中正确的是: ( )
A.镁粉只直接与溴水中的溴反应
B.产生极少量的气泡是由于镁粉和水反应得到
C.镁粉只与溴水中的酸反应
D.镁粉在水的催化下与溴反应
5.下列各组混合物的分离或提纯方法不正确的是 ( )
A.渗析法分离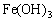 胶体和
胶体和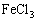 溶液的混合物
溶液的混合物
B.分液法分离CCl4和NaCl溶液的混合物
C.结晶法提纯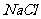 和
和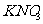 混合物中的
混合物中的
D.加热法分离碘和氯化铵的混合物
4.下列事实与氢键有关的是: ( )
A.水加热到很高的温度都难以分解
B.水结成冰体积膨胀
C.CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高
D.HF、HCl、HBr、HI的热稳定性依次减弱
3.取体积相同的KI、Na2S和FeBr2溶液,分别通入足量氯气当反应恰好完全时,三种溶液消耗氯气的物质的量相同,则KI 、Na2S、FeBr2溶液的物质的量浓度之比为( )
A.2:1:2 B.2:1:3 C.6:3:2 D.3:7:1
2.将质量分数为2w,物质的量浓度为C1的硫酸加水稀释到质量分数为w,物质的量浓度为C2,则C1、C2满足 ( )
A.C1=2C2 B.C1<2C2 C.C1>2C2 D.2C1=C2
1.设NA表示阿伏加德罗常数,下列叙述中,正确的是: ( )
A.假设1mol氯化铁完全转化为氢氧化铁胶体,则分散系中胶体微粒数为NA
B.46g二氧化氮和四氧化二氮的混合气体中含原子数为3NA
C.78g过氧化钠固体中所含阴、阳离子总数为4NA
D.在铜与硫的反应中,1mol铜原子参加反应失去的电子数为2NA
20.(8分)已知某固体混合物A由NaHCO3、KHCO3、MgCO3、CaCO3四种物质中的两种混合而成,通过推理和计算回答下列问题:
(1)取A与足量盐酸反应,若保持总物质的量不变,不论以何种比例混合,生成气体的量均保持不变,则混合物A的组成情况最多有 种(填数字)。
(2)取A与足量盐酸反应,若保持总质量m(A)不变,不论以何种比例混合,生成气体的量均保持不变,则A的可能组成是
和 、 和 、 和 。(可不填满,也可补充)。
(3)若先将A加热,剩余固体再与足量盐酸反应,且将先后两次生成的气体分别通入足量澄清石灰水中,生成的沉淀均为10.0g,则A中各物质的量之和为 mol。
(4)取ag该混合物与足量盐酸反应生成CO2气体的体积V的取值范围是(标准状况) 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com