
13. 某温度下在容积为21的密闭容器中,发生2Y(g)+Y(g) 2W(g)的反应,充入1moLX和1molY,经20s达到平衡时生成了0.4molW。下列说法正确的是( )
某温度下在容积为21的密闭容器中,发生2Y(g)+Y(g) 2W(g)的反应,充入1moLX和1molY,经20s达到平衡时生成了0.4molW。下列说法正确的是( )
A.若升高温度,W的体积分数减小,则该反应△H<0
B.以Y的浓度变化表示的反应速率为0.01mol/(L·s)
C.在其它条件不变的情况下,增加1molX,则X和Y的转化率均提高
D.增大压强正反应速率增大,逆反应速率减小,则平衡向正反应方向移转
12.下列实验能达到预期目的是 ( )
|
序号 |
实验内容 |
实验目的 |
|
A |
向甲酸和甲醛的混合物中加入氢氧化钠溶液,中和甲酸后,加入新制的氢氧化铜加热 |
检验混合物中是否含有甲醛 |
|
B |
向米汤中加入含碘的食盐,观察是滞有颜色的变化 |
检验含碘食盐中是否含碘酸钾 |
|
C |
向红砖粉末中加入盐酸,充分反应后,取上层清液于试管中,滴加硫氰化钾溶液,观察溶液颜色的变化 |
检验红砖中是否含有Fe3+ |
|
D |
向淀粉溶液中加入稀硫酸加热后,再做银镜反应实验 |
检验淀粉是否水解 |
11.短周期元素X、Y、Z和W的原子序数依次递增,且均为同周期,四元素原子的最外层电子数之和为18,X和Y的原子序数比6:7,X的最高正价是W的最低负价绝对值的2倍。下列说法不正确的是 ( )
A.Y的单质可能为原子晶体
B.X和W可组成离子化合物
C.Z和W的单质发生化学反应可生成两种共价化合物
D.Z和W的最高价氧化物对应水化物都是强酸
10.为监测空气中汞蒸气是否超标,通过悬挂涂有Cul(白色)的滤纸,根据滤纸是否变色(亮黄色至暗红色)及变色所需时间来判断空气的汞含量。发生的化学反应为
|
A.上述反应属于置换反应
B.该反应中的氧化剂为Cul
C.Cu2Hg14既是氧化产物又是还原产物
D.当有1molCu1参与反应时,转移电子的物质的量为0.5mol
9.能大量共存于同一溶液中,且当水电离c(H+)=10-13mol/L时,又能发生反应的离子组是 ( )
①Na+、Ba2+、C1-、HCO3- ②K+、NH4+、CH3COO-、SO42-
③Ca2+、NH4+、SO42-、SO32- ④Fe3+、Na+、SCN-、C1-
⑤A13+、Na+、HCO3-、NO3-
A.只有① B.②③ C.①④ D.①②
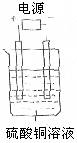
8.如图电解池中装有硫酸铜溶液,选用不同材料的电极进行电解。下列说法正确的是( )
|
序号 |
电极材料 |
通电后的变化 |
|
|
阴极 |
阳极 |
||
|
A |
石墨 |
石墨 |
阴极质量增加,溶液的pH增大 |
|
B |
铜 |
铜 |
阳极质量减小,阴极质量增加 |
|
C |
铁 |
铁 |
两极质量不发生变化 |
|
D |
铂 |
铁 |
阴极质量增加,溶液的pH不变 |
7.下列离子方程式不正确的是 ( )
A.向碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O
B.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:
2Fe2++H2O2+2H+=2Fe3++2H2O
C.铜和稀硝酸反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
D.向次氯酸钙溶液中通入少量二氧化碳:Ca2++2C1O-+CO2+H2O=2HC1O+CaCO3↓
6.下列说法正确的是 ( )
A.浓粉、纤维和葡萄糖均属于多糖
B.苯和甲苯均能使酸性高锰酸钾溶液褪色
C.用溴水能鉴别苯、四氯化碳、乙醇和苯酚
D.溴已烷在氢氧化钠醇溶液共热的条件下生成乙醇
5.下图是制备和收集气体的实验装置,该装置可用于 ( )
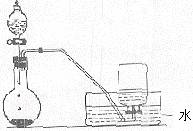
A.浓硝酸与铜反应制取二氧化氮
B.碳化钙与食盐水反应制取乙炔
C.浓氨水与生石灰反应制取氨气
D.浓盐酸与二氧化锰反应制取氯气
4.下列实验操作或安全事故处理中正确的是 ( )
A.用分液漏斗分离甘油和水的混合物
B.用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸杂质
C.不慎将苯酚沾到皮肤上,先用氢氧化钠溶液清洗,再用大量的清水冲洗
D.稀释浓硫酸时,将浓硫酸沿烧杯壁慢慢注入水中并不断搅拦
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com