
11Ł®ÔÚş¬ÓĐFeC13şÍBaC12µÄËáĐÔ»ěşĎŇşÖĐŁ¬Í¨Čë×ăÁżSO2ĆřĚ壬ÓĐ°×É«łÁµíÉúłÉŁ¬ąýÂËşóŁ¬ĎňÂËŇşÖеμÓKSCNČÜŇşŁ¬˛»łöĎÖşěÉ«Ł¬Óɴ˵óöµÄ˝áÂŰĘǡˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ (ˇˇˇˇ )
ˇˇˇˇˇˇ AŁ®°×É«łÁµíĘÇBaSO3ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ BŁ®°×É«łÁµíĘÇFeSO3
ˇˇˇˇˇˇˇˇˇˇˇˇˇˇ CŁ®°×É«łÁµíĘÇBaSO3şÍSˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ DŁ®°×É«łÁµíĘÇBaSO4
9Ł®ĎÂÁĐŔë×Ó·˝łĚĘ˝ĘéĐ´ŐýČ·µÄĘǡˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ (ˇˇˇˇ )
ˇˇˇˇˇˇ AŁ®´×ËáÄƵÄË®˝â·´Ó¦ŁşCH3COO-+H3O+ˇˇˇˇ CH3COOH+H2O
ˇˇˇˇˇˇ BŁ®ĚĽËáÇâÄĆČÜŇşÓëÁňËáÇâÄĆČÜŇş·´Ó¦ŁşHCO3-+H+=CO2ˇü+H2O
ˇˇˇˇˇˇ CŁ®Ďň±˝·ÓÄĆČÜŇşÖĐͨČëÉŮÁżCO2
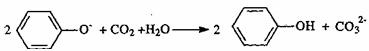
ˇˇˇˇˇˇ DŁ®ĎňFeBr2ČÜŇşÖĐͨČë×ăÁżµÄC12Łş2Fe2++2Br-+2C12=2Fe3++Br2+4C1-
|
ˇˇˇˇˇˇ AŁ®Na2CO3ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ BŁ®Na2CO3şÍNaHCO3
ˇˇˇˇˇˇˇˇˇˇˇˇˇˇ CŁ®Na2CO3şÍNaOHˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ DŁ®NaHCO3şÍNaOH
8Ł®ÉčNAÎŞ°˘·üĽÓµÂÂŢłŁĘýŁ¬ĎÂÁĐĐđĘöŐýČ·µÄĘǡˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ (ˇˇˇˇ )
ˇˇˇˇˇˇ AŁ®ş¬1molĚĽÔ×ӵĽđ¸ŐĘŻľ§ĚĺÖĐC-CĽüµÄĘýÄżÓĐ4NA¸ö
ˇˇˇˇˇˇ BŁ®±ę׼״żöĎÂŁ¬2.24LŇŇČ©ÍęČ«ČĽÉŐËůµĂCO2·Ö×ÓĘýÎŞ0.2NA¸ö
ˇˇˇˇˇˇ CŁ®1mol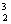 HeËůş¬µÄÖĐ×ÓĘýÎŞ2NA¸ö
HeËůş¬µÄÖĐ×ÓĘýÎŞ2NA¸ö
ˇˇˇˇˇˇ DŁ®ĚúşÍϡÁňËá·´Ó¦Ł¬µ±×ŞŇĆNA¸öµç×ÓʱŁ¬˛úÉúµÄĆřĚĺĚĺ»ý(±ę׼״żö)ÔĽÎŞ11.2L
7Ł®Ň»¶¨ĚőĽţĎÂŁ¬¶ÔÓÚ2SO2+O2
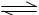 2SO3Ł¬ˇ÷H<0µÄ·´Ó¦Ł¬ĎÂÁĐ˵·¨ÖĐŐýČ·µÄĘÇ (ˇˇˇˇ )
2SO3Ł¬ˇ÷H<0µÄ·´Ó¦Ł¬ĎÂÁĐ˵·¨ÖĐŐýČ·µÄĘÇ (ˇˇˇˇ )
ˇˇˇˇˇˇ AŁ®µ±SO2şÍSO3µÄŨ¶ČĎŕµČʱŁ¬±íĂ÷żÉÄć·´Ó¦´ďµ˝»ŻŃ§Ć˝şâ״̬
ˇˇˇˇˇˇ BŁ®µ±O2µÄÉúłÉËŮÂĘÓëSO3µÄÉúłÉËŮÂĘĎŕµČʱŁ¬±íĂ÷żÉÄć·´Ó¦´ďµ˝»ŻŃ§Ć˝şâ״̬
ˇˇˇˇˇˇ CŁ®Î¶ČŇ»¶¨Ł¬Ôö´óĆ˝şâĚĺϵµÄѹǿŁ¬żÉŇÔĚá¸ßSO2µÄת»ŻÂĘ
ˇˇˇˇˇˇ DŁ®ŃąÇżŇ»¶¨Ł¬Éý¸ßζȣ¬VŐýˇ˘VÄćľůÔö´óŁ¬ÉĎĘö»ŻŃ§Ć˝şâ˛»·˘ÉúŇƶŻ
6Ł®ĎÂÁĐÓйػŻŃ§ĽüÓ뾧Ěĺ˝áąąµÄ˵·¨ŐýČ·µÄĘǡˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ (ˇˇˇˇ )
ˇˇˇˇˇˇ AŁ®Á˝ÖÖÔŞËŘ×éłÉµÄ·Ö×ÓÖĐŇ»¶¨Ö»ÓĐĽ«ĐÔĽü
ˇˇˇˇˇˇ BŁ®Ŕë×Ó»ŻşĎÎďµÄČ۵ăŇ»¶¨±Čą˛ĽŰ»ŻşĎÎďµÄČ۵ă¸ß
ˇˇˇˇˇˇ CŁ®ş¬ÓĐŇőŔë×ӵĻŻşĎÎďŇ»¶¨ş¬ÓĐŃôŔë×Ó
ˇˇˇˇˇˇ DŁ®·Ç˝đĘôÔŞËŘ×éłÉµÄ»ŻşĎÎďŇ»¶¨ĘÇą˛ĽŰ»ŻşĎÎď
23Ł®(6·Ö)ŇřĐżĽîĐÔĐîµçłŘĘÇŇ»ÖÖżÉŇÔ·´¸´łäµçˇ˘·ĹµçµÄ×°ÖᣵçłŘ·´Ó¦ĘÇŁş
ˇˇˇˇˇˇ 2Ag+Zn(OH)2 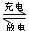 Zn+Ag2O+H2O
Zn+Ag2O+H2O
ˇˇˇˇˇˇ ĽŮČç´ËÖÖĐîµçłŘ·Ö±đÓĂŔ´µç˝âĎÂÁĐÁ˝ÖÖČÜŇşŁ¬ą¤×÷Ň»¶ÎʱĽäşóĐîµçłŘ¶Ľ·Ö±đĎűşÄ0.72gH2O(µç˝âłŘµÄµçĽ«ľůÎŞ¶čĐԵ缫)ˇŁ»Ř´đŁş
ˇˇ (1)µç˝âM(NO3)xČÜҺʱŁ¬ÄłŇ»Ľ«ÔöĽÓÁËagMŁ¬Ôň˝đĘôMµÄĎŕ¶ÔÔ×ÓÖĘÁżÎŞˇˇˇˇˇˇˇˇ
ˇˇˇˇˇˇ (ÓĂaˇ˘x±íĘľ)Ł»
ˇˇ (2)µç˝âş¬ÓĐ0.04mloCuSO4şÍ0.04molNaClµÄ»ěşĎČÜŇş400mlŁ¬ÔňŃôĽ«˛úÉúµÄĆřĚĺĘÇ
ˇˇˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇÉý(±ę׼״żö)Ł»´ËʱČÜŇşµÄpH = ˇˇˇˇˇˇˇˇ(ĽŮÉčµç˝âşóČÜŇşĚĺ»ý˛»±ä)
22Ł®(8·Ö)ÄĚÓÍÖĐÓĐŇ»ÖÖÖ»ş¬Cˇ˘Hˇ˘OµÄ»ŻşĎÎďAˇŁAżÉŇÔÓĂ×÷ĎăÁĎŁ¬ĆäĎŕ¶Ô·Ö×ÓÖĘÁżÎŞ88Ł¬·Ö×ÓÖĐCˇ˘Hˇ˘OÔ×Ó¸öĘý±ČÎŞ2ˇĂ4ˇĂ1Ł¬ÇŇş¬ÓĐĚĽŃőË«ĽüˇŁ
ˇˇˇˇˇˇ ŇŃÖŞŁş˘ŮROH+HBr(ÇâäĺËá RBr+H2Oˇˇ ˘Ú
RBr+H2Oˇˇ ˘Ú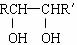
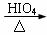 RCHO+RˇäCHOˇˇˇˇˇˇˇˇˇˇˇˇ
RCHO+RˇäCHOˇˇˇˇˇˇˇˇˇˇˇˇ
ˇˇˇˇˇˇ ÓëAĎŕąŘµÄ·´Ó¦ČçĎÂŁş

ˇˇ (1)Đ´łöĎÂÁĐ·´Ó¦»ŻŃ§·˝łĚĘ˝şÍ·´Ó¦ŔŕĐÍŁş
ˇˇˇˇ ˘ŮEˇúF ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇŁ»·´Ó¦ŔŕĐÍÎŞˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ Ł»
ˇˇˇˇ ˘ÚBˇúD ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇŁ»·´Ó¦ŔŕĐÍÎŞˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ Ł»
ˇˇ (2)ÔÚżŐĆřÖĐł¤Ę±Ľä˝Á°čÄĚÓÍŁ¬AżÉŇÔת»ŻÎŞĎŕ¶Ô·Ö×ÓÖĘÁżÎŞ86µÄ»ŻşĎÎďGŁ¬GµÄŇ»ÂČ´úÎďÖ»ÓĐŇ»ÖÖŁ¬Đ´łöGµÄ˝áąąĽňĘ˝ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
21Ł®(8·Ö)ŇŇȲĘÇŇ»ÖÖÖŘŇŞµÄÓĐ»ú»Żą¤ÔÁĎŁ¬ŇÔŇŇȲΪÔÁĎÔÚ˛»Í¬·´Ó¦ĚőĽţĎÂżÉŇÔת»ŻÎŞŁş
ˇˇˇˇ ˘ŮŐýËÄĂćĚĺÍé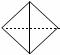 Ł¬ ˘ÚŇŇĎ©»ůŇŇȲCH2=CH-C=CHŁ¬˘Ű±˝
Ł¬ ˘ÚŇŇĎ©»ůŇŇȲCH2=CH-C=CHŁ¬˘Ű±˝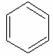
ˇˇ (1)ŐýËÄĂćĚĺÍéµÄ·Ö×ÓʽΪˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ Ł»
ˇˇ (2)ąŘÓÚŇŇĎ©»ůŇŇȲµÄ˵·¨´íÎóµÄĘǡˇˇˇˇˇˇˇˇˇˇˇˇˇ Ł»
ˇˇˇˇˇˇˇˇˇˇˇˇˇˇ AŁ®ÄÜĘąËáĐÔKMnO4ČÜŇşÍĘÉ«
ˇˇˇˇˇˇˇˇ BŁ®µČÖĘÁżµÄŇŇȲşÍŇŇĎ©»ůŇŇȲÍęČ«ČĽÉŐʱµÄşÄŃőÁż˛»Ďŕͬ
ˇˇˇˇˇˇˇˇˇˇˇˇˇˇ CŁ®1mol ŇŇĎ©»ůŇŇȲÄÜÓë3mol Br2 ·˘ÉúĽÓłÉ·´Ó¦
ˇˇˇˇˇˇˇˇˇˇˇˇˇˇ DŁ®ŇŇĎ©»ůŇŇȲ·Ö×ÓÄÚş¬ÓĐÁ˝ÖÖąŮÄÜÍĹ
ˇˇ (3)Đ´łöÓë±˝»ĄÎŞÍ¬ĎµÎďÇŇŇ»ÂČ»ŻÎďÖ»ÓĐÁ˝ÖÖÎďÖʵĽṹĽňĘ˝Łş(Đ´Á˝¸ö)ˇˇˇˇˇˇˇˇˇˇ ˇŁ
20Ł®(9·Ö)ĎÂÍĽÖĐËůÓĐÎďÖĘľůÓɶĚÖÜĆÚÔŞËŘ×éłÉŁ¬AµÄŃćÉ«·´Ó¦ÎŞ»ĆÉ«Ł¬Bˇ˘Cˇ˘Gľůş¬Í¬Ň»ÖÖÔŞËŘŁ¬DłŁÎÂĎÂÎŞŇşĚ壬Bˇ˘CľůČÜÓÚHµÄČÜŇşˇŁ
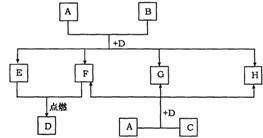
ˇˇˇˇ Çë»Ř´đŁş
ˇˇ (1)ČôBÎŞ˝đĘôŁ¬»ŻŃ§Ę˝ÎŞˇˇˇˇˇˇˇˇˇˇˇˇ Ł¬ą¤ŇµÉĎÓÉCÖĆȡBµÄ»ŻŃ§·˝łĚʽΪˇˇˇˇˇˇ
ˇˇˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇŁ»
ˇˇ (2)ČôBÎŞ·Ç˝đĘôŁ¬»ŻŃ§Ę˝ÎŞˇˇˇˇˇˇˇˇˇˇˇˇ Ł¬ą¤ŇµÉĎÓÉCÖĆȡBµÄ»ŻŃ§·˝łĚʽΪˇˇˇˇ
ˇˇˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇŁ»
ˇˇ (3)ČôBÎŞ·Ç˝đĘôŁ¬Đ´łöA+B+DˇúE+F+G+HµÄŔë×Ó·˝łĚĘ˝(ĆäÖĐEşÍFµÄÎďÖʵÄÁżÖ®±ČÎŞ3ˇĂ1)Łşˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
19Ł®(8·Ö)Wˇ˘Xˇ˘Yˇ˘Zˇ˘Aˇ˘BĘÇÔ×ÓĐňĘýŇŔ´ÎÔö´óµÄÁůÖÖłŁĽűÔŞËءŁAµÄµĄÖĘÔÚY2ÖĐČĽÉյIJúÎďżÉʹƷşěČÜŇşÍĘÉ«ˇŁBşÍYÔŞËŘĐγɵĻŻşĎÎďB3Y4ľßÓĐ´ĹĐÔˇŁWµÄµĄÖĘÔÚY2ÖĐČĽÉŐżÉÉúłÉWYşÍWY2Á˝ÖÖĆřĚ塣ZµÄµĄÖĘĘÇŇ»ÖÖ˝đĘôŁ¬¸Ă˝đĘôÔÚWY2ÖĐľçÁŇČĽÉŐÉúłÉşÚˇ˘°×Á˝ÖÖąĚĚ塣
ˇˇ (1)XµÄµĄÖĘ·Ö×ӵĵç×ÓʽΪˇˇˇˇˇˇˇˇˇˇˇˇ Ł»BÔŞËصÄÔÚÖÜĆÚ±íÖеÄλÖĂĘǡˇˇˇˇˇˇˇ Ł»
ˇˇ (2)ZÔÚWY2ÖĐČĽÉյĻŻŃ§·˝łĚĘ˝ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ Ł¬Wˇ˘Xˇ˘Y·Ö±đÓëÇâĐγɵÄ10µç×ÓÇ⻯şĎÎďÖĐŁ¬·Đµă×îµÍµÄĘÇ(Đ´»ŻŃ§Ę˝)ˇˇˇˇˇˇˇˇˇˇˇˇˇˇ Ł»
ˇˇ (3)AY2ĆřĚĺͨČëBaCl2şÍHNO3µÄ»ěşĎČÜŇşÖĐŁ¬ÉúłÉ°×É«łÁµíşÍÎŢÉ«ĆřĚĺXYÓйصÄŔë×Ó·˝łĚʽΪˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ Ł¬Óд˿ɼűXYşÍAY2Ďŕ±Č»ąÔĐÔ˝ĎÇżµÄĘÇ(Đ´»ŻŃ§Ę˝)ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
ąúĽĘѧУÓĹѡ - Á·Ď°˛áÁбí - ĘÔĚâÁбí
şţ±±Ęˇ»ĄÁŞÍřÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨Ć˝Ě¨ | ÍřÉĎÓĐş¦ĐĹϢľŮ±¨×¨Çř | µçĐĹթƾٱ¨×¨Çř | ÉćŔúĘ·ĐéÎŢÖ÷ŇĺÓĐş¦ĐĹϢľŮ±¨×¨Çř | ÉćĆóÇÖȨľŮ±¨×¨Çř
ÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨µç»°Łş027-86699610 ľŮ±¨ÓĘĎ䣺58377363@163.com