
9.将1mol SO2和1mol O2通入恒容密闭器中,一定条件下达到平衡时,SO3的物质的量为0.3mol,此时若移走0.5mol SO2和0.5mol O2,反应达到新的平衡时,SO3的物质的量是( )
A.0.3mol B.0.5mol
C.小于0.5mol D.大于0.5mol,小于0.3mol
8.在水电离出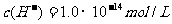 的溶液中,一定能大量共存的离子组是 ( )
的溶液中,一定能大量共存的离子组是 ( )
A.Na*、K*、Br-、NO-3 B.K*、NH+4、CO2-3、Br-
C.Fe2* 、Na*、MnO-4、Cl- D.Cu2*、Na+、Cl-、SO2-4
7.将X溶液滴加到Y溶液中,开始没有明显现象,后来出现白色沉淀的是 ( )
|
选项 |
X溶液 |
Y溶液 |
|
A |
NaOH |
Mg(HCO3)2 |
|
B |
Al2(SO4)3 |
Ba(OH)2 |
|
C |
Na2CO3 |
CaCl2 |
|
D |
NaAlO2 |
HCl |
6.下列说法正确的是 ( )
A.二氧化硅分子中存在极性共价键
B.Na2O2、H2O2、CO2中均含有非极性键
C.水的化学性质较稳定是由于水分子间存在共价键
D.离子晶体中一定存在离子键,也可能存在共价键
5.下列说法不正确的是 ( )
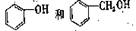 A.
A.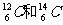 互为同位素 B.氧气和臭氧元素的同异形体
互为同位素 B.氧气和臭氧元素的同异形体
C.蔗糖和麦芽糖互为同分异构体 D. 互为同系物
27.在1 L密闭容器中,把1 mol A和1 mol B混合发生如下反应:
3A(g)+B(g) xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,通过计算完成下列问题:
xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,通过计算完成下列问题:
(1)在该平衡下,在保持压强不变时,向该容器内充入氦气,则该平衡向 (填写“正向移动”、“逆向移动”、“不移动”)
(2)x的值为 ;
(3)平衡时A的转化率为 ;
(4)如果加入0.2mol的C、 0.2molD、0.9molB和0.7molA充入到原来容器内,保持原来的条件不变,则达到平衡时B的物质的量浓度是 。
26.实验室用下图所示的装置制取溴化亚铁。其中,A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管,e是两只耐高温的瓷夹,其中共盛有56g细铁粉。实验开始时先将铁粉加热至600-700℃,然后将干燥、纯净的CO2气流通入D中,E管中的物质开始反应,不断地将d中的液溴滴入100-120℃的D中,经过几小时的连续反应后在不锈钢管一端沉积有黄绿色鳞片状溴化亚铁80g。
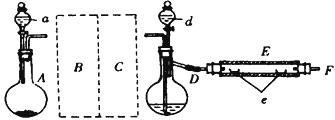
(1)若导入的CO2不干燥,会在E中发生副反应,其化学方程式为 。
(2)在A中盛有CaCO3,a中盛有6mol·L-1盐酸。为使A中产生的CO2在进入D之前既干燥又纯净,B、C处采用相同的玻璃仪器,其仪器名称为 ;
B盛有的试剂是: ;C盛有的试剂是: .
(3)实验时,D和E的橡胶塞为什么最好用铝箔包住?
(4)反应过程中要不断地通入CO2,其主要作用是: 。
(5)E中在加热时进行的反应是:2Fe+3Br2=2FeBr3,2FeBr3=2FeBr2+Br2↑。此实验中溴化亚铁的产率为 。(保留到小数点后一位)
25.有常见A、B、C三种短周期元素,它们的原子序数逐渐增大,B元素原子最外层电子数是C元素原子最外层电子数的一半。A元素原子最外层电子数比B元素原子最外层电子数多1个。甲是B元素含氧酸的钠盐。乙是C元素最高价含氧酸的酸式钠盐。丙是A元素含氧酸的钠盐(正盐)。甲、丙溶液pH>7,乙溶液pH<7,丁为气体,戊为淡黄色固体。甲、乙、丙、丁、戊、己六种物质之间相互反应关系如下:
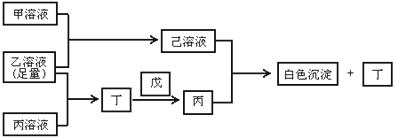
试回答:
(1)C元素原子结构示意图为: ;丁的结构式为: ;戊的电子式为: ;
(2)用有关离子方程式(或电离方程式)解释:
①乙溶液显酸性的原因是:_______________________________________;
②丙溶液呈碱性的原因是:_______________________________________;
(3)写出有关反应的离子方程式:
①乙溶液 + 丙溶液: ;
②己溶液 + 丙溶液: ;
24.根据所学知识完成下列空白:
(1)用惰性电极电解NaNO3溶液,要想恢复原来状态需要加入的物质 。
(2)用惰性电极电解CuSO4溶液的阳极反应式: 。
23.已知An+、B(n+1)+、Cn-、D(n+1)-离子具有相同的电子层结构,则A、B、C、D的原子半径由大到小的顺序是:______________,离子半径由大到小的顺序是:________________,原子序数由大到小的顺序是:_______________________。(用ABCD字母回答)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com