
26.(10分)元素X、Y、Z、W为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数占核外电子总数的3/4,W-、Z+、X+离子半径逐渐减小,化合物XW常温下为气体。请填空:
(1)X、Y、Z、W的元素符号为X ,Y ,Z ,W 。
(2)A、B均为由上述四种元素中的任意三种组成的强电解质,且两种物质中,组成元素的原子数目比均为1:1:1。A的溶液中水的电离程度比B溶液中水的电离程度小,则A的化学式为 ,电子式为 ,B的化学式为 。
13.常温下,将0.1mol·L-1的CH3COOH溶液V1mL加入到0.1mol·L-1的NaOH溶液V2mL中,下列结论中不正确的是(反应前后溶液体积无变化) ( )
A.若混合溶液pH=7,当V2=10时,混合溶液V≥20mL
B.若混合溶液呈中性,则混合溶液中:c(CH3COO-)=0.1V2/(V1+V2)mol·L-1
C.若混合溶液的pH<7,则混合溶液中离子浓度关系可能是:
c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
D.若混合溶液的pH>7,则混合溶液中离子浓度关系可能是:
c(Na+)>c(CH3COO-) > c(OH-)>c(H+)
第Ⅱ卷 (非选择题 共174分)
12.在某容积一定的密闭容器中,有下列的可逆反应:A(g)+B(g) 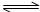 xC(g)(正反应放热)有图I所示的反应曲线,试判断对图II的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数) ( )
xC(g)(正反应放热)有图I所示的反应曲线,试判断对图II的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数) ( )
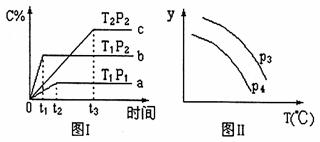
①P3>P4,y轴表示B的转化率 ②P3<P4,y轴表示B的体积分数
③P3<P4,y轴表示混合气体的密度 ④P3>P4,y轴表示混合气体的平均摩尔质量
A.①② B.②③ C.①④ D.③4
11.将含有0.400mol CuSO4和0.200moloKCl的溶液1L,用惰性电极电解一段时间后,在一个电极上析出19.2gCu,此时在另一电极上放出的气体在标准状况下的体积为 ( )
A.5.60L B.6.72L C.4.48L D.3.36
10.某有机物含有C、H、O三种元素,其球棍模型如图所示。该有机物可能发生的反应有
|
①水解 ②加聚 ③聚代 ④消去 ⑤银镜
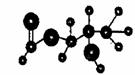
A.①③④ B.①④⑤ C.①②③④⑤ D.①③④⑤
9.制备氰氨基化钙的化学方程式如下:CaCO3+2HCN=CaCN2+CO↑+H2↑+CO2↑,关于该
反应的下列说法中正确的是 ( )
A.氢元素被氧化,碳元素被还原 B.HCN既是氧化剂又是还原剂
C.CaCN2是还原产物,H2是氧化产物 D.CO为氧化产物,H2为还原产物
8.化学用语是学习化学的重要工具,下面用来表示物质变化的化学用语中,正确的是
( )
A.氢气燃烧的热化学方程式:H2(g)+1/2O2(g)=H2O(l);△H=+285.8Kj·mol-1
B.甲烷碱性燃料电池的负极反应:CH4+10OH--8e-=CO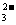 +7H2O
+7H2O
C.饱和FeCl3溶液滴入沸水中的反应:FeCl3+3H2O=Fe(OH)3↓+3HCl↑
D.铝片溶于氢氧化钠溶液:Al+2OH-=AlO +H2↑
+H2↑
7.下列物质的制备,符合工业生产实际的是 ( )
A.将氯气通入澄清石灰水中制备漂白粉
B.用离子交换膜法电解饱和食盐水制备烧碱、氢气、氯气
C.将氢气和氯气混合点燃,产物用水吸收制备盐酸
D.将SO2和O2的混合气体高压后,通过装有铁触媒的接触室,接触氧化制备SO3
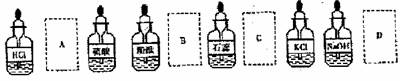
6.实验室中的药品常按物质的性质、类别不同而有规律地保管着。在做“酸的性质”实验时,实验桌上的部分药品的摆放如图所示。某同学取用KOH溶液以后应把它放回 ( )
29.(15分)某学生实验小组用10g胆矾制取CuO,并证明CuO可以催化H2O2及KClO3等的分解。
Ⅰ.请完成制备CuO的实验步骤:
(1) 称取10g胆矾,放入小烧杯中,再 ;
(2) 向小烧杯中滴加 溶液,至产生大量沉淀;
(3) (填写操作方法);
(4) 将以上混合物 ,洗涤, ,然后研细;
(5)检查(4)中洗涤是否完全的操作是 。
Ⅱ.用图示方法证明CuO能催化7% H2O2溶液的分解,并与MnO2的催化效果进行比较。
|
实验序号 |
双氧水体积 |
催化剂 |
待测数据 |
|
① |
15mL |
无 |
|
|
② |
15mL |
0.5g CuO |
|
|
③ |
15mL |
0.5g MnO2 |
|
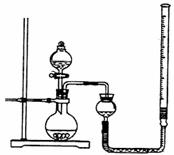
(1)从设计原理看,实验中待测数据可以是 ,也可以是 。
(2)实验时气体收集在球形漏斗中,此中气体是否纯净(不计水蒸气) ,理由是 。
(3)为探究CuO在实验②中是否起催化作用,除与①比较外,还应补充以下实验(不必写具体操作):a.证明CuO化学性质是否改变;b. 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com