
10Ł®NH3ˇ˘H2SµČĘÇĽ«ĐÔ·Ö×ÓŁ¬CO2ˇ˘BF3ˇ˘CCl4µČĘÇş¬Ľ«ĐÔĽüµÄ·ÇĽ«ĐÔ·Ö×ÓˇŁ¸ůľÝÉĎĘöʵŔýżÉÍĆłö ABnĐÍ·Ö×ÓĘÇ·ÇĽ«ĐÔ·Ö×ӵľŃéąćÂÉĘÇ
ˇˇ AŁ®·Ö×ÓÖв»ÄÜş¬ÓĐÇâÔ×Ó
ˇˇ BŁ®ÔÚABn·Ö×ÓÖĐAµÄĎŕ¶ÔÔ×ÓÖĘÁżÓ¦ĐˇÓÚBµÄĎŕ¶ÔÔ×ÓÖĘÁż
ˇˇ CŁ®ÔÚABn·Ö×ÓÖĐAÔ×ÓĂ»Óй¶Եç×Ó
ˇˇ DŁ®·Ö×ÓÖĐĂż¸öą˛ĽŰĽüµÄĽüł¤Ó¦ĎŕµČ
9Ł®ĎÂÁĐ·´Ó¦µÄŔë×Ó·˝łĚĘ˝ŐýČ·µÄĘÇ
ˇˇ AŁ®µĄÖĘÍÓëϡĎőËá·´Ó¦ŁşCu+2H++2NO3ŁŁ˝Cu2++2NOˇü+H2O
ˇˇ BŁ®ĎňFe(NO3)2ČÜŇşÖĐĽÓČëŃÎË᣺3Fe2++4H++NO3Ł Ł˝3Fe3++NOˇü+2H2O
ˇˇ CŁ®ĚĽËáÇâÄĆČÜŇşÓëÉŮÁżĘŻ»ŇË®·´Ó¦ŁşHCO3Ł+Ca2++OHŁŁ˝CaCO3ˇý+H2O
ˇˇ DŁ®ÂÁƬ¸úÇâŃő»ŻÄĆČÜŇş·´Ó¦ŁşAl+2OHŁ+2H2OŁ˝ŁŰAl(OH)4ŁÝŁ + H2ˇü
8Ł®Xˇ˘Yˇ˘ZÎŞÖ÷×ĺÔŞËŘŁ¬XÔ×ÓµÄ×îÍâ˛ăµç×ÓĹŲĽÎŞns1Ł»YÔ×ÓµÄMµç×Ó˛ăÓĐ2¸öδłÉ¶Ôµç×ÓŁ»ZÔ×ÓµÄ×îÍâ˛ăpąěµŔÉĎÖ»ÓĐŇ»¶ÔłÉ¶Ôµç×Ó,ÇŇZÔ×ӵĺËÍâµç×Ó±ČYÔ×ÓÉŮ8¸öµç×ÓŁ¬ÓÉŐâČýÖÖÔŞËŘ×éłÉµÄ»ŻşĎÎďµÄ·Ö×ÓĘ˝˛»żÉÄܵÄĘÇ
ˇˇ AŁ®XYZ4 ˇˇˇˇˇˇˇˇBŁ®X2YZ4 ˇˇˇˇˇˇˇˇˇˇCŁ®X2YZ3ˇˇˇˇˇˇˇˇ DŁ®X2Y2Z3
7Ł®ÄłÎďÖĘ·Ö×ӽṹʽΪ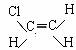 Ł¬ĎÂÁĐ˵·¨˛»ŐýČ·µÄĘÇ
Ł¬ĎÂÁĐ˵·¨˛»ŐýČ·µÄĘÇ
ˇˇ AŁ®¸Ă·Ö×ÓÖĐĽČş¬ÓĐĽ«ĐÔą˛ĽŰĽüŁ¬ÓÖş¬ÓĐ·ÇĽ«ĐÔą˛ĽŰĽü
ˇˇ BŁ®¸Ă·Ö×ÓĘÇĽ«ĐÔ·Ö×Ó
ˇˇ CŁ®¸Ă·Ö×ÓÖĐÁů¸öÔ×ÓλÓÚͬһƽĂ棬Ľü˝ÇÎŞ120ˇă
ˇˇ DŁ®¸ĂÎďÖĘÄŃČÜÓÚË®
6Ł®ĎÂÁĐ˵·¨ŐýČ·µÄĘÇ
ˇˇ AŁ®O2Ł°ëľ¶±ČFŁµÄС
ˇˇ BŁ®NaşÍCsĘôÓÚ˘ńA×ĺÔŞËŘŁ¬Csʧµç×ÓÄÜÁ¦±ČNaµÄÇż
ˇˇ CŁ®SiH4±ČCH4Îȶ¨
ˇˇ DŁ®PşÍAsĘôÓÚµÚ˘őA×ĺÔŞËŘŁ¬H3PO4 ËáĐÔ±ČH3AsO4µÄČő
5Ł®ĎÂÁĐÓйػŻŃ§ĽüÓ뾧Ěĺ˝áąąËµ·¨ŐýČ·µÄĘÇ
ˇˇ AŁ®Á˝ÖÖÔŞËŘ×éłÉµÄ·Ö×ÓÖĐËůş¬»ŻŃ§ĽüŇ»¶¨ĘÇĽ«ĐÔĽü
ˇˇ BŁ®˝đĘôľ§ĚĺµÄČ۵ăŇ»¶¨±Č·Ö×Óľ§ĚĺµÄ¸ß
ˇˇ CŁ®Äłľ§ĚĺÖĐş¬ÓĐŃôŔë×ÓŁ¬ÔňŇ»¶¨Ň˛ş¬ÓĐŇőŔë×Ó
ˇˇ DŁ®ş¬ÓĐŇőŔë×ӵĻŻşĎÎďŇ»¶¨ş¬ÓĐŃôŔë×Ó
4Ł®ÔÚĎÂĂćµÄÍâ˛ăµç×ÓąąĐÍÖĐ,µÚŇ»µçŔëÄÜ×îСµÄÔ×ÓżÉÄÜĘÇ
ˇˇ AŁ® 2s22p3ˇˇˇˇˇˇ BŁ® 3s23p5ˇˇˇˇˇˇˇˇˇˇ CŁ®3s23p4ˇˇˇˇˇˇˇˇˇˇ DŁ® 3s23p6
3Ł®ÔÚNO2±»Ë®ÎüĘյķ´Ó¦ÖĐ,·˘Éú»ąÔ·´Ó¦şÍ·˘ÉúŃő»Ż·´Ó¦µÄÎďÖĘ,ĆäÖĘÁż±ČÎŞ
ˇˇ AŁ®3:1ˇˇˇˇˇˇˇˇ BŁ®1:3ˇˇˇˇˇˇˇˇˇˇˇˇ CŁ®1:2ˇˇˇˇˇˇˇˇˇˇˇˇ DŁ®2:1
2Ł®ĎÂÁĐÎďÖʵķÖ×ÓÖĐŁ¬ĽČÓЦҼüÓÖÓЦРĽüµÄĘÇ
ˇˇ AŁ®N2ˇˇˇˇˇˇˇˇ BŁ®HClOˇˇˇˇˇˇˇˇˇˇ CŁ®CH4 ˇˇˇˇˇˇˇˇˇˇˇˇDŁ®C2H6
1Ł®ÔÚĎÂÁĐÎŢɫ͸Ă÷ČÜŇşÖĐŁ¬ÄÜ´óÁżą˛´ćµÄŔë×Ó×éĘǡˇˇˇˇˇˇˇˇˇ
ˇˇ AŁ®Cu2+ˇ˘Na+ˇ˘SO42Łˇ˘ClŁ ˇˇˇˇˇˇˇˇˇˇBŁ®K+ˇ˘Na+ˇ˘HCO3Łˇ˘NO3Ł
ˇˇ CŁ®OHŁˇ˘HCO3Łˇ˘Ca2+ˇ˘Na+ˇˇˇˇˇˇ ˇˇˇˇ DŁ®Mg2+ˇ˘Na+ˇ˘OHŁˇ˘NO3Ł
ąúĽĘѧУÓĹѡ - Á·Ď°˛áÁбí - ĘÔĚâÁбí
şţ±±Ęˇ»ĄÁŞÍřÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨Ć˝Ě¨ | ÍřÉĎÓĐş¦ĐĹϢľŮ±¨×¨Çř | µçĐĹթƾٱ¨×¨Çř | ÉćŔúĘ·ĐéÎŢÖ÷ŇĺÓĐş¦ĐĹϢľŮ±¨×¨Çř | ÉćĆóÇÖȨľŮ±¨×¨Çř
ÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨µç»°Łş027-86699610 ľŮ±¨ÓĘĎ䣺58377363@163.com