
32.(8分)取3.320g某固态芳香羧酸(A)置于4L氧气中,经点燃使其(A)完全燃烧,反应后气体体积增加了0.224L。将反应后的气体通过足量的Na2O2固体后,气体体积减少1.792L(所有气体体积均在标准状况下测定)。请回答:
(1)3.320g该羧酸(A)中碳元素的物质的量为 mol。
(2)列式计算3.320g该羧酸(A)中氢、氧两元素的物质的量。(写出计算过程)
(3)该羧酸(A)分子中C、H、O的原子个数比为 。
(4)写出符合以下各条件的相对分子质量最小的芳香羧酸(A)的结构简式;
①(A)中只含有羧基,不含其他官能团,其结构简式为(任写一种)
②(A)既能与NaHCO3反应放出CO2,又能与金属钠反应放出H2,且相同物质的量的(A)
分别与足量的NaHCO3、Na反应,放出的CO2体积和H2体积相等(同温同压下),(A)还能发生银镜反应,其结构简式为(任写一种):
31.(5分)某有机物A由碳、氢、氧三种元素组成,A蒸气的密度是相同条件氢气的15倍。15gA完全燃烧后,若将燃烧后的产物通过碱石灰,碱石灰的质量增加31g;若将燃烧后的产物通过浓硫酸,浓硫酸的质量增加9g。
(1)通过计算确定有机物A的分子式; (2)画出A的结构式。
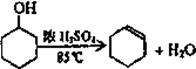
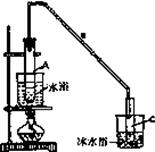
30.(10分)某化学小组采用类似制乙酸乙酯的装置(如图),以环已醇制备环已烯

已知:
|
|
密度 (g/cm3) |
溶点 (℃) |
沸点 (℃) |
溶解性 |
|
环已醇 |
0.96 |
25 |
161 |
能溶于水 |
|
环已烯 |
0.81 |
-103 |
83 |
能溶于水 |
(1)制备粗品
将12.5mL环已醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环已烯粗品。
①A中碎瓷片的作用是 ,导管B除了导气外还具有的作用是 。
②试管C置于冰水浴中的目的是 。
(2)制备精品
①环已烯粗品中含有环已醇和少量酸性杂质等。加入饱和和食盐水,振荡、静置、分层,环已烯在 层(填上或下),分液后用 (填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.NaCO3溶液
②再将环已烯按下图装置蒸馏,冷却水从 口进入。蒸馏时要加入生石灰,目的是 。
③收集产品时,控制的温度应在 左右,实验制得的环已烯精品质量低于理论产量,可能的原因是( )
a.蒸馏时从70℃开始收集产品 b.环已醇实际用量多了
c.制备粗品时环乙醇随产品一起蒸出
(3)以下区分环已烯精品的粗品的方法,合理的是 。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
29.(3分)下列方法中,不能达到实验目的是 。
A.用氯化铁溶液鉴别乙醇溶液和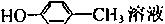
B.用蒸镏的方法分离碘的CCl4溶液
C.用酸性高锰酸钾溶液鉴别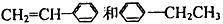
D.用KI溶液除去溴苯中含有的溴杂质
E.只用溴水一种试剂鉴别苯、甲苯、乙醇
28.(11)碱存在下,卤代烃与醇反应生成醚(R-O-R');(其中R、R'为烃基)
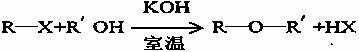 化合物A经下列四步反应可得到常用溶剂四氢呋喃,反应框图如下;
化合物A经下列四步反应可得到常用溶剂四氢呋喃,反应框图如下;
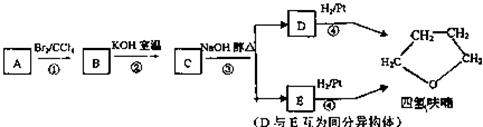
请回答下列问题:
(1)1mol A和1 molH2在一定条件下恰好反应,生成饱和一元醇Y,Y中碳元素的质量分数约为65%,则Y的分子式为 。
A分子中所含官能团的名称是 。
A的结构简式为 。
(2)第①②③步反应类型分为① ② ③
(3)化合物B具有的化学性质(填写字母代号)是 。
a.可发生氧化反应 b.强酸或强碱条件下均可发生消去反应
c.可发生酯反应 d.催化条件下可发生如聚反应
(4)写出C、D和E的结构简式:
C 、D和E 。
(5)写出化合物C与NaOH水溶液反应的化学方程式;
(6)写出四氢呋喃链状醚类的所有同分异构体的简式;
27.(9分)A、B、C、D、E、F和G都是有机化合物,它们的关系如下图所示;
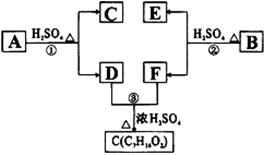
(1)化合物C的分子式是C7H8O,C遇FeCl3溶液显紫色,C苯环上的氢原子被溴原子取
代,生成的一溴代物只有两种,则C的结构简式为
(2)D为一直链化合物,其相对分子质量比化合物C的小20,它能跟NaHCO3反应放出CO2,则D分子式为 ,D具有的官能团是 。
(3)反应①的化学方程式是 ;
(4)芳香化合物B是与A具有相同官能团的A的同分异构体,通过反应②化合物B能生成E和F,F可能的结构简式为
(5)E可能的结构简式是
25.1mol某有机物分别与足量Na、NaOH、NaHCO3反应,用去的Na、NaOH、NaHCO3的物质的量分别为3mol,2mol,1mol,该有机物不能发生水解反应,推断该有机物中必须具备的官能团为 ( )
A.三个羧基 B.一个羧基、二个酚羟基
C.二个醇羟基、一个酚羟基 D.一个羟基、一个醇羟基,一个酚羟基
第Ⅱ卷(非选择题 共50分)
|
(1)丙烷脱氢可得丙烯。
已知:C3H8(g)====CH4(g)+HC≡CH(g)+H2(g)  H1=15.6kJ·mol-1
H1=15.6kJ·mol-1
CH3CH=CH2(g)====CH4(g)+HC≡CH(g)  H2=32·4kJ·mol-1
H2=32·4kJ·mol-1
则相同条件下,反应C3H8(g)====CH3CH=CH2(g)+H2(g)的H= kJ·mol-1
(2)以丙烷燃料制作新型电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应方程式为 ;放电时,CO32-移向电池的
(填“正”或“负”极)
24.下列实验能获得成功的是 ( )
A.溴乙烷中加入足量NaOH溶液,加热冷却后再加入AgNO3溶液有浅黄色沉淀生成
B.蔗糖溶液中加放稀H2SO4,加热后再加新制Cu(OH)2,加热有红色物质生成
C.将红色铜丝在酒精灯上加热后,立即插入无水乙醇中,铜丝恢复成原来的红色
D.苯酚溶液中加放少量稀溴水观察生成白色沉淀
23.某烃的衍生物A,其分子式为C6H12O2,实验表明A和NaOH溶液共热生成B和C,B和盐酸反应生有机物D,C和Cu催化加热条件下氧化为E,其中D、E都不能发生银镜反应。由此判断A可能结构有 ( )
A.2种 B.3种 C.4种 D.6种
22.将冰醋酸、甲醛、葡萄糖、甲酸甲酯依次按5:4:3:2的质量比混合,则混合物中碳元素的质量分数为
A.40% B.60% C.30% D.50%
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com