
29.(16分)有机物A(C8H8O2)为一种无色液体。从A出发可发生如下一系列反应:
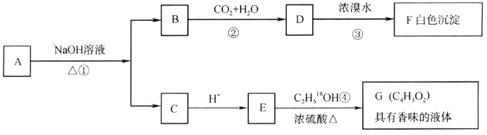
请回答:
(1)A和F的结构简式:A ,F 。
(2)反应②的离子反应方程式: 。
反应④的化学反应方程式: 。(请注明示踪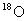 原子)
原子)
(3)A的同分异构体甚多,其中属于羧酸类的化合物,且含有苯环结构的异构体有多种。写出其结构简式 。
28.(13分)某中学有甲、乙两个探究性学习小组,他们拟用小颗粒状铝硅合金与足量稀硫酸能反应测定通常状况(约20℃,1atm)下气体摩尔体积的方法。
(1)甲组同学拟选用下图实验装置完成实验:
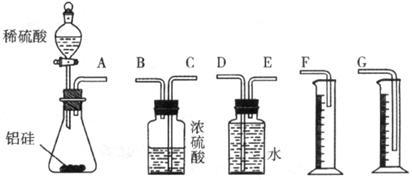
①该组同学必须选用的装置的连接顺序是A接( )( )接( )( )接( )(填接口字母,可不填满。)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸不能顺利滴入锥形瓶(导管中无固体物堵塞)。请你帮助分析原因: ___ 。
③实验结束时,该组同学应怎样测量实验中生成氢气的体积? 。
(2)乙组同学仔细分析甲组同学的实验装置后,认为有些不够完善,他们改用了如下图的装置进行实验,可减小所测氢体积的误差。
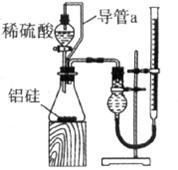
①导管a的作用是 。
②实验结束时,若用甲组同学实验装置所测氢气体积偏小,其可能的原因是(导管中无固体物堵塞) 。
③实验中准确测得4个数据:实验前铝硅合金的质量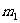 g,实验后残留固体的质量
g,实验后残留固体的质量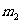 g,实验前后碱式滴定管中液面读数分别为V1mL、V2
ML。则通常状况时气体摩尔体积
g,实验前后碱式滴定管中液面读数分别为V1mL、V2
ML。则通常状况时气体摩尔体积 。
。
27.(10分)已知A-F是中学化学中常见物质,其中A、C、E、F为气体,B、D为液体,D 的消费量常作为一个国家工业发达水平的一种标志,F的浓溶液与x共热通常用于实验室制备单质C,X是一种黑色粉末,B分子中有18个电子。反应中部分生成物已略去。试回答下列问题:
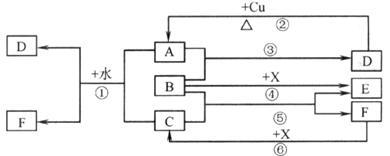
(1)根据图中信息,B、C、D、X氧化性从强到弱的顺序是 。
(2)B的电子式为: 。
(3)写出反应②的化学方程式: 。
(4)写出反应①⑥的离子方程式:
① ;
⑥ 。
26.(15分)
(1)在反应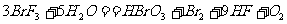 中,当有3mol水参加反应时,由
中,当有3mol水参加反应时,由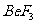 还原的
还原的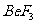 为 mol;总共转移的电子数为 mol。
为 mol;总共转移的电子数为 mol。
(2)日本青山学院大学教授秋光纯发现的化合物硼化镁在39K时超导,该化合物的晶体结构如下图所示,“○”表示Mg,处于六棱柱的顶点和面心。“●”表示B,处于六棱柱中6个三棱柱的体心,请完成下列问题:
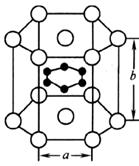
①该化合物的化学式为 ;
②以任意一个镁原子为球心、以它到最近的硼原子的距离为半径画球,则第一层球面上有 个硼原子;
③已知该化合物晶体的密度为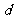 g/cm,底边边长为
g/cm,底边边长为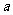 cm,高为
cm,高为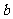 cm,则阿伏加德罗常数NA= (用含有
cm,则阿伏加德罗常数NA= (用含有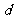 、
、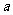 、
、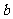 的式子表示,根号不用开出)。
的式子表示,根号不用开出)。
13.设NA为阿伏加德罗常数,下列说法正确的是
A.标准状况下的22.4L辛烷完全燃烧,生成的二氧化碳的分子数为8NA
B.在熔融状态下,l mol NaHSO4完全电离出的阳离子数目为2NA
C.1 mol S被Cu还原,转移电子数为2NA
D.在1L 2mol·L-1的硝酸镁溶液中含有的硝酸根离子数为4NA
第Ⅱ卷(非选择题 共174分)
12.下列离子方程式正确的是
A.将SO2通入次氯酸钙溶液中: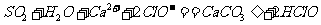
B.碳酸氢钠溶液跟过量的饱和石灰水反应: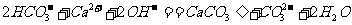
C.Ca(OH)2溶液中通入过量CO2: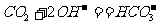
D.饱和氯化铁溶液滴加沸水中: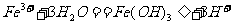
11.对下面有机物的叙述不正确的是
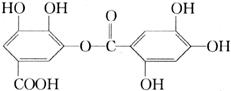
A.常温下,与Na2CO3溶液反应放出CO2
B.能发生碱性水解,1mol该有机物完全反应消耗8molNaOH
C.与稀H2SO4共热,生成两种有机物
D.该有机物的分子式为C14H10O9
10.反应A2+B2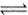 2AB在不同温度和压强改变条件下,产物AB的生成情况,如下图所示:a为500℃,b为300℃时情况,c为300℃时从时间
2AB在不同温度和压强改变条件下,产物AB的生成情况,如下图所示:a为500℃,b为300℃时情况,c为300℃时从时间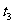 开始向容器中加压的情况,则下列叙述正确的是
开始向容器中加压的情况,则下列叙述正确的是
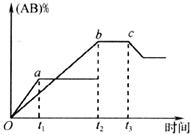
A.A2、B2、AB均为气体,正反应放热
B.AB为气体,A2、B2中最少有一种为非气体,正反应放热
C.AB为气体,A2、B2中最少有一种为非气体,正反应吸热
D.AB为固体,A2、B2中最少有一种为非气体,正反应吸热
9.某学生在实验报告中有以下实验数据
①用托盘天平称取11.7g氯化钠 ②用量筒量取5.26mL盐酸
③用广泛pH试纸测得溶液的pH是3.5
④用标准NaOH溶液滴定未知浓度盐酸用去23.10mLNaOH溶液,其中数据合理的是
A.①④ B.②③ C.①③ D.②④
8.下列说法正确的是
A.H与D,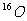 与
与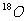 互为同位素;
互为同位素;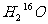 、
、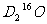 、
、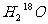 、
、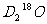 互为同素异形体;甲醇、乙二醇和丙三醇互为同系物
互为同素异形体;甲醇、乙二醇和丙三醇互为同系物
B.向某未知溶液中加入BaCl2溶液后再加入稀硝酸,检验是否含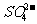
C.HI的相对分子质量大于HF,所以HI的沸点高于HF
D.由ⅠA族和ⅥA族元素形成的原子个数比为1 :1,电子总数为38的化合物,是含有共价键的离子型化合物
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com