
由90℃氯化铰的溶解度可知,100g水最多能溶71.3g 氯化铵,所以在90℃蒸发100g水将析出71.3g氯化铵。
【指导练习】将90℃饱和氯化铵溶液680g,蒸发100g水再冷却至40℃,将析出晶体多少克?已知90℃时溶解度为71.3g,40℃时溶解度为45.8g。
做练习后回答问题:这个问题我是按两步计算的:
(1)求90℃时蒸发100g水将析出多少克晶体。
3.有关溶解度的计算
溶解度计算是本讲的难点,希望同学们认真思考、积极练习,掌握解题的思路和方法。
【评价】很好。请同学们根据图1-1,找出不同温度下固体溶质的溶解度。
2.溶解度曲线
【提问】温度和压强怎样影响气体溶质的溶解度?
温度怎样影响固体溶质的溶解度?
回答:气体溶质的溶解度与温度、压强有关,温度越高,气体的溶解度越小,压强越大,气体的溶解度越大。固体的溶解度与温度有密切关系,多数固体的溶解度随温度升高,溶解度增大,少数物质,如氯化钠的溶解度则受温度影响很小。个别物质的溶解度随温度升高而降低,如氢氧化钙。
【再问】能否形象地表示出溶解度随温度改变的关系呢?
回答:可以,用溶解度曲线即可。
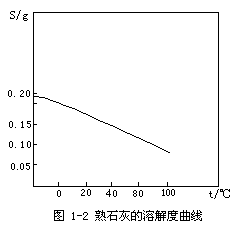
看图1-2,并练习。
1.概念
【提问】什么是溶解度?气体的溶解度是如何表示的?影响溶解度的因素有哪些?条件改变后,饱和溶液有什么变化?
思考并回答:
在一定温度下,在100g溶剂中溶解溶质达饱和,所溶解溶质的质量称为溶解度。溶解度单位是g。若溶质是气体,则溶解度是指:在一定温度和压强下,1体积溶剂溶解溶质达饱和时,所溶解的气体的体积。(单位是:L/L)
影响溶解度的因素首先是溶质和溶剂的性质。此外条件对溶解度也有影响。固体的溶解度与温度有关,而气体则和温度、压强都有关系。
由影响溶解度的条件可知,当条件改变时,溶解平衡将被打破,溶质溶解的速率和结晶的速率不再相等,饱和溶液可以转化成不饱和溶液,也可以析出晶体,在新的条件下达到新的溶解平衡。
【评价】肯定学生的回答并强调:在掌握固体的溶解度的概念时,一定要注意:(1)温度;(2)达饱和;(3)100g溶剂,这三个关键性的词语。
11. 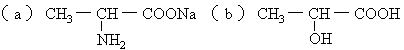

(2)5 (3)16,因为C5H12O有8种属于醇的结构,C4H8O2有2种属于羧酸的结构。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com