
12、强酸与强碱的稀溶液发生中和反应的反应热可表示如下:
H+(aq)+OH-(aq)=H2O(l);△H= - 57.3KJ/mol
向1L1mol/L的NaOHaq中加入:①稀醋酸 ②浓硫酸 ③稀硝酸
恰好完全反应时的反应热为△H1、△H2、△H3,它们的关系正确的是( )
A.△H1>△H2>△H3 B.△H2>△H3>△H1
C.△H1=△H2=△H3 D.△H1>△H3>△H2
11、含NaOH 20.0g的稀溶液与足量的稀盐酸反应,放出28.7KJ的热量,表示该反应中和热的热化学方程式正确的是( )
A.NaOH(aq)+HCl(aq)=NaCl (aq)+H2O(l);△H =+28.7KJ/mol
B.NaOH(aq)+HCl(aq)=NaCl (aq)+H2O(l);△H=-28.7KJ/mol
C.NaOH(aq)+HCl(aq)=NaCl (aq)+H2O(l);△H=+57.4KJmol
D.NaOH(aq)+HCl(aq)=NaCl (aq)+H2O(l);△H=-57.4KJ/mol
10、某强酸性溶液中可能存在NO3-、I-、Cl-、Fe3+中的一种或几种。向该溶液中加入溴水后,溴被还原,由此推断该溶液中( )
A.不含NO3-,也不含Fe3+ B.含有NO3-、I-、Cl-
C.含I-,但不能确定是否含Cl- D.含有Fe3+
9、下列各组离子能在指定环境中大量共存的是( )
A.在c(HCO3-)=0.1 mol·L-1的溶液中:NH4+、Al3+、Cl-、NO3-
B.在由水电离出的c(H+)=1×10-12 mol·L-1的溶液中:
Fe2+、ClO-、Na+、SO42-
C.在加入铝粉产生气体的溶液中:SO42-、NO3-、Na+、Fe2+
D.在使红色石蕊试纸变蓝的溶液中:SO32-、CO32-、Na+、K+
8、下列离子方程式书写正确的是 ( )
A.过量的SO2通入NaOH溶液中:SO2+2OH-=SO32-+H2O
B.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2
C.NaNO2溶液中加入酸性KMnO4溶液:
2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O
D.NaHCO3溶液中加入过量的Ba(OH)2溶液:
2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32-
7、V L Fe2(SO4)3溶液中含有a g SO42-,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量的浓度为 ( )
A
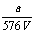 mol/L B
mol/L B 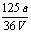 mol/L C
mol/L C  mol/L D
mol/L D 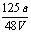 mol/L
mol/L
6、将足量的的稀盐酸加到下列固体溶液中,只能发生一种反应的是( )
A.Mg、AlCl3、 NaAlO2 B. KNO3、NaCl、CH3COONa
C. NaClO、Na2SO3、BaCl2 D. Ba(NO3)2、FeSO4、NH4HCO3
5、下列离子方程式正确的是 ( )
A. 向盐酸中滴加氨水:H+ + OH- = H2O
B. Na2CO3固体溶于水中:CO32-+2H2O H2CO3+2OH-
 C. 铜溶于稀硝酸:3Cu + 8H+ + 2NO3- = 3Cu2+
+ 2 NO ↑+ 4H2O
C. 铜溶于稀硝酸:3Cu + 8H+ + 2NO3- = 3Cu2+
+ 2 NO ↑+ 4H2O
D. 电解饱和食盐水:2Cl- +2H2O Cl2↑+ H2↑+2OH-
4、某溶液中(假定不考虑水解因素)仅含有K+、Mg2+、SO42- NO3-四种离子,其中K+与Mg2+的个数之比为4:5,则NO3-与SO42-的物质的量比一定不是
( )
A、8:3 B、3:2 C、1:3 D、2:3
3、阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是 ( )
A、2.24LCO2中含有的原子数为0.3 ×6.02×1023
B、6.8g KHSO4 溶于水,溶液中含有0.1NA 个阳离子
C、5.6g铁粉与硝酸反应失去的电子数一定为0.3 ×6.02×1023
D、4.5g SiO2晶体中含有的硅氧键数目为0.3 ×6.02×1023
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com