
3、设函数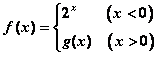 ,若
,若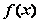 是奇函数,则
是奇函数,则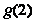 的值是( )
的值是( )
A.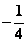 B.
B.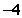 C.
C.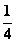 D.
D.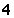
2、 设全集
设全集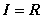 ,
,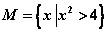 ,
,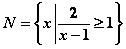 ,如图,则图中阴影部分所表示的集合为( )
,如图,则图中阴影部分所表示的集合为( )
A.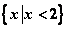 B.
B.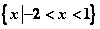
C.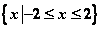 D.
D.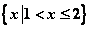
1、设集合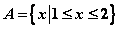 ,
,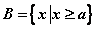 ,若
,若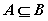 ,则
,则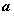 的范围是( )
的范围是( )
A. 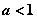 B.
B.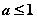 C.
C.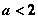 D.
D.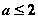
28. (8分) 将2.5g碳酸钠、碳酸氢钠和氢氧化钠固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如下图所示:
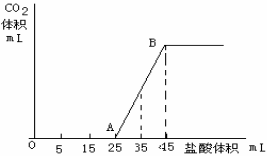 (1)写出OA段所发生反应的
(1)写出OA段所发生反应的
离子方程式
(2)当加入35mL盐酸时,产生
二氧化碳的体积为 mL(标准状况)
(3)计算原混合物中Na2CO3的质量分数。
27. (8分)A、B、C、D、E、F六种物质在一定条件下有如图所示的相互转化关系,所有反应物和生成物已给出
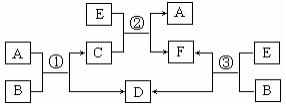
(1)若反应①、②、③均为溶液中的置换反应,且通常状况下A为液态非金属单质,B的焰色反应为黄色,则根据反应①、②、③比较相关物质的氧化性由强到弱的顺序为 (用字母表示);反应②的离子方程式为 。
(2)若B是一种淡黄色固体,绿色植物的光合作用和呼吸作用可实现自然界中D、E的循环,则反应①的离子方程式为 。在反应③中若生成1molD,则转移的电子数目为
26. (12分)为了研究氯水能否和碳酸钙发生化学反应,某学生设计如下实验:
实验一:向盛有饱和氯水的锥形瓶中加入大理石,并充分振荡,观察到氯水的黄绿色褪去并同时产生少量气体。
实验二:取上述实验一后锥形瓶中清液,进行如下实验:
(1)该清液滴在有色布条上有极强的漂白作用。
(2)该清液中滴加碳酸钠溶液产生白色沉淀。
(3)该清液中滴加稀盐酸可产生大量气体。
(4)该清液加热后变浑浊并产生大量气体。
实验三:该学生设想用下列装置收集实验二中产生的气体作进一步检验。
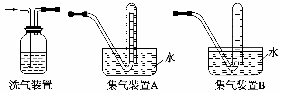
回答下列问题:
(1)在实验二中,清液滴在有色布条上有极强的漂白作用说明该清液中含有 (写化学式);清液中滴加碳酸钠溶液产生白色沉淀说明该清液中含有 离子;清液加热后产生浑浊的原因是因为生成了 (用化学式表示)。
(2)实验三中,洗气装置内的洗涤液一般用 溶液。
(3)在反应物的量相同情况下,该学生尝试用集气装置A和集气装置B分别和洗气装置相连来收集气体。选用集气装置 (选填“A”或“B”)可收集到更多的气体。经试验,该学生最终选用集气装置B进行下一步实验。其选择装置B的原因是
(4)该学生通过上述实验,写出了氯水和碳酸钙反应的化学方程式为
25. (6分)下面a-e是中学化学实验中常见的几种定量仪器:
(a)量筒 (b)容量瓶 (c)托盘天平 (d)温度计 (e)滴定管
(1)其中标示出仪器使用温度的是 (填写编号)。
(2)配制一定物质的量浓度的溶液时,由于错误操作, 使得到的数据比正确数据偏小的是 (填写编号)。
A.用量筒量取一定量液体时, 俯视液面读数。
B.没有用蒸馏水洗烧杯2-3次,并将洗液移入容量瓶中。
C、容量瓶刚用蒸馏水洗净,没有烘干。
D、使用容量瓶配制溶液时, 俯视液面定容。
(3)称取10.5g固体样品(1g以下使用游码)时, 将样品放在了天平的右盘, 则所称样品的实际质量为 g。
24. (6分)一瓶澄清的溶液,其中可能含有NH4+、K+、Na+、Mg2+、Ba2+、Al3+、Cl-、I-、NO3-、
CO32-、SO42-离子,取该溶液进行以下实验:
(1)取pH试纸检验,溶液呈酸性。
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4层呈紫色。
(3)另取部分溶液逐渐加入少量NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,溶液均无沉淀产生。
(4)取上述部分碱液加碳酸钠溶液,有白色沉淀产生。
(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝
根据上述实验事实确定:
①该溶液中肯定存在的离子是___ ___; ②肯定不存在的离子是____ _;
③还不能确定是否存在的离子是__________________________________。
23.(6分)在盛有淀粉KI溶液(已酸化)的试管中,滴加少量的次氯酸钠溶液,会立即看到溶液变蓝色,相应的离子方程式为 ;
在盛有淀粉和碘形成的蓝色溶液中,滴加亚硫酸钠溶液,又发现蓝色逐渐消失,相应的离子方程式为 ,
对比以上两组实验结果,可得出ClO-、I2、SO42-的氧化性由强到弱的顺序为 。
22.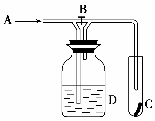 如图是一种试验某气体化学性质的实验装置,图中B为活塞。如先打开B,在A处通入干燥氯气,C中红布条颜色无变化;当关闭B时,C中红布条颜色褪去。则D瓶中盛有的溶液是 ( )
如图是一种试验某气体化学性质的实验装置,图中B为活塞。如先打开B,在A处通入干燥氯气,C中红布条颜色无变化;当关闭B时,C中红布条颜色褪去。则D瓶中盛有的溶液是 ( )
A.浓硫酸 B.浓NaOH溶液 C.H2O D.饱和NaCl溶液
第Ⅱ卷(非选择题 共46分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com