
7.为了检验某化合物中是否含有NH4+、SO42-、Fe2+和结晶水,设计了下列操作步骤:
①取少量晶体加热,发现试管口处有液体,且该液体能使无水硫酸铜变蓝;
②另取少量晶体溶于水中,加入KSCN溶液,再滴加少量的氯水,有红色出现;
③取少量溶液于试管,加入盐酸,没有反应现象,再加入BaC12溶液,有白色沉淀生成; ④取少量溶液于试管中,加入浓NaOH溶液,微热有使湿润的红色石蕊试纸变蓝的气
体
产生,同时也有白色沉淀产生,该沉淀很快变成灰绿色沉淀。
下列说法不正确的是 ( )
A.②中的现象说明有Fe2+
B.通过上述实验可确定该化合物的化学式为(NH4)2Fe(SO4)2·6H2O
C.为了检测SO2-4,可以将③中的试剂换为HNO3酸化的Ba(NO3)2
D.④中的沉淀长时间放置会变红褐色沉淀
6.有一瓶无色溶液,可能含有K+、Al3+、Mg2+、NH4+、Cl-、SO42-、HCO3-、MnO4-离子中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生下列推断正确的是 ( )
A.肯定有Al3+、Mg2+、NH4+、Cl- B.肯定有Al3+、Mg2+、HCO3-
C.肯定有K+、HCO3-、MnO4- D.肯定有Al3+、Mg2+、SO42-
5.下列实验能证明SO2存在的是 ( )
①能使澄清石灰水变浑浊 ②能使湿润的蓝色石蕊试纸变红 ③能使品红溶液褪色 ④通入足量的NaOH溶液中,再加BaCl2溶液有白色沉淀生成,该沉淀溶于稀盐酸 ⑤通入溴水中能使溴水褪色,再滴加HNO3酸化的Ba(NO3)2溶液有白色沉淀生成
A.都不能证明 B.都能证明 C.只有⑤能证明 D.③④⑤能证明
4.某溶液中可能存在Br-、CO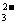 、SO
、SO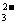 、Al3+、I-、Mg2+、Na+等7种离子中的几种现取该溶液进行实验,得到如下实验现象:①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。据此可以推断,该溶液中肯定不存在的离子是( )
、Al3+、I-、Mg2+、Na+等7种离子中的几种现取该溶液进行实验,得到如下实验现象:①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。据此可以推断,该溶液中肯定不存在的离子是( )
A.Al3+、Mg2+、I-、SO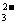 B.Mg2+、Na+、CO
B.Mg2+、Na+、CO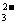 、I-
、I-
C.Al3+、Na+、SO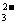 、I- D.Al3+、CO
、I- D.Al3+、CO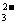 、Br-、SO
、Br-、SO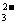
3.不用其它试剂,就能将下列溶液一一鉴别开来的是 ( ) A.NaOH、NaHCO3、NaHSO4、AlCl3 B.NOH、NH4NO3、HCl、KNO3 C.Na2SO4、Ca(NO3)2、BaCl2、Na2CO3 D.CuSO4、KMnO4、FeCl3、溴水
2.为了区别5瓶无色溶液:HCl、AlCl3、Ba(NO3)2、NaCl、Na2CO3,甲、乙、丙、丁4位
学生都没有酒精灯,其中1位学生没有另用任何试剂。他们中操作步骤一定最少的是
A.甲另用了酚酞试液 B.乙另用了NaOH溶液
C.丙另用了石蕊试液 D.丁不用任何试剂
pH在3.1-4.1时的甲基橙溶液等。
专题训练
1.有NaCl、FeCl2、FeCl3、MgCl2、AlCl3五种溶液,用一种试剂就可把它们鉴别开来,这种试剂是 ( )
A.盐酸 B.烧碱溶液 C.氨水 D.KSCN溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com