
5.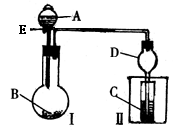 某课外活动小组学生模拟呼吸面具中的原理(过氧化钠与潮湿二氧化碳反应),设计用下图所示的仪器来制取氧气并测量氧气的体积。
某课外活动小组学生模拟呼吸面具中的原理(过氧化钠与潮湿二氧化碳反应),设计用下图所示的仪器来制取氧气并测量氧气的体积。
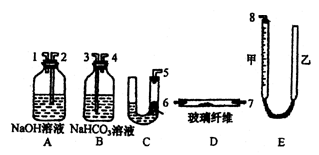 上图中量气装置E是由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水。甲管有刻度(0-50mL),供量气用;乙管可上下移动,以调节液面高低。
实验室可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水
试回答:(1)上述装置的连接顺序是(填各接口的编号):___________。
(2)装置C中放入的反应物是__________和__________。
(3)装置A的作用是__________,装置B的作用是__________。
(4)为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读取反应前后甲管中液面的读数,求其差值的过程中,应注意____________和____________(填写字母编号)。
a.视线与凹液面最低数相平 b.等待片刻,待乙管中液面不再上升时,立刻读数
c.读数时应上下移动乙管,使甲、乙两管液面相平d.读数时不一定使甲、乙管液面相平
上图中量气装置E是由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水。甲管有刻度(0-50mL),供量气用;乙管可上下移动,以调节液面高低。
实验室可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水
试回答:(1)上述装置的连接顺序是(填各接口的编号):___________。
(2)装置C中放入的反应物是__________和__________。
(3)装置A的作用是__________,装置B的作用是__________。
(4)为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读取反应前后甲管中液面的读数,求其差值的过程中,应注意____________和____________(填写字母编号)。
a.视线与凹液面最低数相平 b.等待片刻,待乙管中液面不再上升时,立刻读数
c.读数时应上下移动乙管,使甲、乙两管液面相平d.读数时不一定使甲、乙管液面相平
4.下列各组物质中,制备装置、收集装置均相同,且都可用浓H2SO4干燥的是( ) A.SO2和H2S B.CH4和NH3 C.CO2和H2 D.CH4和O2
1. 某试管内装有约占其容积1/10的溶液,则溶液的体积是
A.约1mL B.约3mL C.约2ml D.无法判断
2.拟在烧杯中于加热条件下配制某溶液50mL,应选择的烧杯是
A.400mL烧杯 B.250mL烧杯
C.100mL烧杯 D. 50mL烧杯
3.实验室保存下列试剂采取的措施不正确的是( )
A.KI保存在棕色试剂瓶中 B.波尔多液盛放在铁制容器中
C.氢氟酸保存在塑料瓶中 D.溴水盛放在带胶塞的棕色瓶中
某试管内装有约占其容积1/10的溶液,则溶液的体积是
A.约1mL B.约3mL C.约2ml D.无法判断
2.拟在烧杯中于加热条件下配制某溶液50mL,应选择的烧杯是
A.400mL烧杯 B.250mL烧杯
C.100mL烧杯 D. 50mL烧杯
3.实验室保存下列试剂采取的措施不正确的是( )
A.KI保存在棕色试剂瓶中 B.波尔多液盛放在铁制容器中
C.氢氟酸保存在塑料瓶中 D.溴水盛放在带胶塞的棕色瓶中
6.有以下四组物质:①FeCl2、Al(NO3)3、MgSO4、NH4NO3四种溶液
②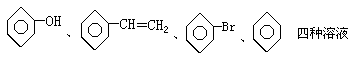 ③MnO2、FeS、CuO、C四种黑色固体
④NaCl、AlCl3、Ba(OH)2、HCl四种溶液。其中只用一种试剂(允许加热)就能将组内物质区别开的是( )
A.只有①③ B.只有①②③ C.只有①③④ D.全部
③MnO2、FeS、CuO、C四种黑色固体
④NaCl、AlCl3、Ba(OH)2、HCl四种溶液。其中只用一种试剂(允许加热)就能将组内物质区别开的是( )
A.只有①③ B.只有①②③ C.只有①③④ D.全部
课外作业
5.将淀粉溶液和淀粉酶的混合物放入玻璃纸袋扎好袋口,浸入流动的温水中,经相当一段时后,取袋内液体分别与碘水、新制Cu(OH)2悬浊液(加热)、浓硝酸(微热)作用,其现象依次是
|
试剂 |
A |
B |
C |
D |
|
碘水 |
显蓝色 |
显蓝色 |
无明显现象 |
无明显现象 |
|
新制Cu(OH)2(加热) |
无红色沉淀 |
红色沉淀 |
无红色沉淀 |
红色沉淀 |
|
浓硝酸(微热) |
显黄色 |
无明显现象 |
显黄色 |
无明显现象 |
4.在化学实验室进行下列实验操作时,其操作或记录的数据正确的是( ) A.用托盘天平称取8.84g食盐 B.用250mL的容量瓶配制所需的220mL、0.1mol/L的NaOH溶液 C.用量筒量取12.12mL的盐酸 D.用0.12mol/L盐酸滴定未知浓度的NaOH溶液,消耗盐酸21.40mL
3.下列各实验现象能用同一原理解释的是( ) A.苯酚、乙烯都能使溴水褪色 B.稀硫酸中加入铜粉不反应,再加硝酸钠或硫酸铁后,铜粉溶解 C.葡萄糖和福尔马林与新制氢氧化铜悬浊液共热,都产生红色沉淀 D.将SO2通入氯化钡溶液至饱和,再加入足量硝酸或苛性钠溶液,都产生白色沉淀
2.下列实验操作中,仪器需插入液面下的有①制备Fe(OH)2,用胶头滴管将NaOH溶液滴入FeSO4溶液中;②制备氢气,简易装置中长颈漏斗的下端管口;③分馏石油时,测量温度所用的温度计;④用乙醇制乙烯时所用的温度计;⑤用水吸收氨气时的导气管;⑥向试管中的BaCl2溶液中滴加稀硫酸 A.③⑤⑥ B.③⑤ C.①②④ D.①②③④⑤⑥
1.下列有关实验操作的叙述中,不正确的是( )
 A.少量的白磷贮存在水中,切割时在水下进行
B.制取硝基苯时,使用的温度计的水银球应浸没于反应混合液中
C.不慎将浓硫酸沾到皮肤上,应迅速大量用水冲洗,最后涂上稀小苏打溶液
D.不能使用裂化汽油从溴水中萃取溴
A.少量的白磷贮存在水中,切割时在水下进行
B.制取硝基苯时,使用的温度计的水银球应浸没于反应混合液中
C.不慎将浓硫酸沾到皮肤上,应迅速大量用水冲洗,最后涂上稀小苏打溶液
D.不能使用裂化汽油从溴水中萃取溴
2.(05年江苏20)硫酸亚铁(FeSO4•7H2O)是一种重要的食品和饲料添加剂。实验室通过如下实验由废铁屑制备FeSO4•7H2O晶体:
① 将5%Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na2CO3溶液,然后将废铁屑用水洗2-3遍;
② 向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50-80℃之间至铁屑耗尽;
③ 趁热过滤,将滤液转入到密闭容器中,静置、冷却结晶;
④ 待结晶完毕后,滤出晶体,用少量冰水洗涤2-3次,再用滤纸吸干晶体;
⑤ 将制得的FeSO4•7H2O晶体放在一个小广口瓶中,密闭保存。回答下列问题:
(1)实验步骤①的目的是 ,加热的作用是 。
(2)实验步骤②明显不合理,理由是 。(3)实验步骤④中用少量冰水洗涤晶体,其目的是 ;
。
(4) 经查阅资料后发现,硫酸亚铁在不同温度下结晶可分别得到FeSO4•7H2O、FeSO4•4H2O、FeSO4•H2O。硫酸亚铁在不同温度下的溶解度和该温度下析出晶体的组成如下表所示(仅在56.7℃、64℃时可同时析出两种晶体)。
硫酸亚铁的溶解度和析出晶体的组成
|
温度/℃ |
0 |
10 |
30 |
50 |
56.7 |
60 |
64 |
70 |
80 |
90 |
||
|
溶解度/g |
14.0 |
17.0 |
25.0 |
33.0 |
35.2 |
35.3 |
35.6 |
33.0 |
30.5 |
27.0 |
||
|
析出晶体 |
FeSO4•7H2O |
FeSO4•4H2O |
FeSO4•H2O |
|||||||||
请根据表中数据作出硫酸亚铁的溶解度曲线。
若需要从硫酸亚铁溶液中结晶出FeSO4•4H2O,应控制的结晶温度范围为 。
思维方法: 。
展望高考:
[巩固练习]
课堂反馈
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com