
29.(28分)回答下列Ⅰ、Ⅱ题
 Ⅰ.(10分)下丘脑是机体调节内分泌活动的枢纽,与体内的许多生理活动密切相关,下丘脑与垂体之间既有神经联系又有血液联系,右图中1、2、3为神经细胞。请根据图提供的信息,分析并回答问题。
Ⅰ.(10分)下丘脑是机体调节内分泌活动的枢纽,与体内的许多生理活动密切相关,下丘脑与垂体之间既有神经联系又有血液联系,右图中1、2、3为神经细胞。请根据图提供的信息,分析并回答问题。
(1)科学家发现,切断C处的联系时垂体的分泌功能未受到影响,说明 ▲ .
(2)当人体受到寒冷刺激时,在大脑皮层相关部位的影响下,使细胞1产生兴奋,传递给细胞2,使A处 ▲ 含量增加。这说明体温调节是通过机体的 ▲ 和 ▲ 两种调节方式完成的;也说明机体中既能传导兴奋,又能分泌激素的细胞位于 ▲ (下丘脑、垂体)。
Ⅱ.(18分)酵母菌在氧气充足条件下不能进行酒精发酵,有同学认为是氧气自身抑制了酵母菌厌氧呼吸,也有同学认为是需氧呼吸产生的某产物X抑制了酵母菌厌氧呼吸。请设计实验探究酵母菌在氧气充足条件下不能进行厌氧呼吸的原因。
供选的实验试剂和用品:酵母菌细胞(试剂1)、酵母菌破碎后经离心处理得到的只含有酵母菌细胞溶胶的上清液(试剂2)和只含有酵母菌细胞器的沉淀物(试剂3)、X溶液、蒸馏水、橡皮管夹若干、其他常用器材和试剂。
(1)先给本设计作出假说 ▲ 。
(2)完成下列实验步骤:

①取锥形瓶等连接成如上图所示的装置四套,依次编号为甲、乙、丙、丁。其中每套装置的a锥形瓶加入质量分数为10%的NaOH溶液10mL,c锥形瓶加入质量分数5%的葡萄糖溶液10ml,b与d锥形瓶各加入等量的澄清石灰水。
②首先完成表内空格的填空(在C锥形瓶中添加试剂、溶液和气体的处理),然后按表格完成实验操作。
|
实验操作 |
甲 |
乙 |
丙 |
丁 |
|
添加试剂(供选:试剂1、2、3) |
10mL的试剂2 |
10mL的试剂2 |
▲ |
10mL的试剂2 |
|
添加溶液(供选:X溶液、蒸馏水) |
2mL蒸馏水 |
2mL X溶液 |
▲
|
2mL X溶液 |
|
通气状况(供选:氧气、氮气) |
持续通入足量的氮气 |
▲
|
▲
|
持续通入足量的氧气 |
(注:甲、乙、丙、丁四套装置均先持续通入氮气5min,去除锥形瓶中的氧气,后按表格操作)
③将四套装置放在温度适宜(25-35℃)的相同条件下培养相同一段时间(8-10h)。
④观察澄清石灰水是否变浑浊,判断是否进行厌氧呼吸。
(3)预期实验结果并得出相应结论:
① ▲ ;
② ▲ ;
③ ▲ ;
④ ▲ ;
⑤甲、乙、丙三套变浑浊,丁套不变浑浊,则酵母菌厌氧呼吸受X与氧气共同抑制。
28.(14分)已知J是一种药物,其合成路线可以设计如下:
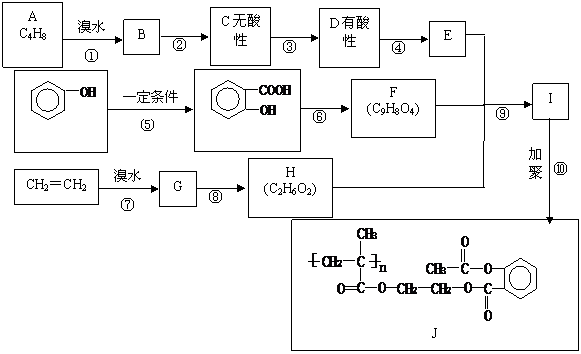
(1)A与H2发生还原反应后所得产物的名称为 ▲ 。
(2)写出反应类型:反应④ ▲ ,反应⑥ ▲ 。
(3)写出反应②的化学方程式: ▲ 。
(4)写出满足下列条件的F的一种同分异构体的结构简式 ▲
①苯的衍生物,且苯环上的一取代产物只有两种;②与Na2CO3溶液反应放出气体;
③水解后的产物才能与FeCl3 溶液发生显色反应。
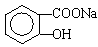 (5)上述反应⑤的原子经济性为100%,请以苯和氯气为原料,设计合理的方案合成水杨酸钠(
)(用合成路线流程图表示,并注明必要的反应条件,无机试剂任意选用)。合成路线流程图示例如下:
(5)上述反应⑤的原子经济性为100%,请以苯和氯气为原料,设计合理的方案合成水杨酸钠(
)(用合成路线流程图表示,并注明必要的反应条件,无机试剂任意选用)。合成路线流程图示例如下:
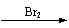 CH3CH2OH
CH3CH2OH 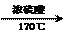 H2C=CH2
BrH2C-CH2Br
H2C=CH2
BrH2C-CH2Br
27.(16分)硫酸铜是一种应用极其广泛的化工原料。铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图所示)。

(1)写出烧瓶中发生反应的化学方程式为: ▲ 。
(2)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:以空气为氧化剂法
方案1:以空气为氧化剂。将铜粉在仪器B中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应。
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加FeSO4或Fe2(SO4)3,即发生反应。反应完全后向其中加物质甲调节pH 3~4,产生Fe(OH)3沉淀,过滤、浓缩、结晶,滤渣作催化剂循环使用。已知:
|
沉淀物 |
Fe(OH)3 |
Cu(OH)2 |
Fe(OH)2 |
|
开始沉淀pH |
2.7 |
4.8 |
7.6 |
|
完全沉淀pH |
3.7 |
6.4 |
9.6 |
请回答下列问题:
①方案1中的B仪器名称是 ▲ 。
②方案2中甲物质是 ▲ ,最后所得晶体中可能含有 ▲ (填字母序号)
A、CaO B、NaOH C、CuCO3 D、FeSO4 E、Fe2(SO4)3 F、FeSO4·7H2O
第二组:过氧化氢为氧化剂法
将3.2g铜丝放到45 mL 1.5mol·L-1的稀硫酸中,控温在50℃。加入18mL 10%的H2O2,反应0.5h后,升温到60℃,持续反应1 h后,过滤、蒸发浓缩、减压抽滤等,用少量95%的酒精淋洗后晾干,得CuSO4·5H2O 10.5g。
请回答下列问题:
③加热时温度不宜过高的原因是 ▲ ,写出组装减压抽滤装置的注意点
▲ 。(至少二点)
④本实验CuSO4·5H2O的产率为 ▲ 。
⑤上述两种氧化法中,更符合绿色化学理念的是 ▲ (填“第一组”或“第二组”),理由是 ▲ 。
26.(15分)(1)已知:在常温下,浓度均为0.1mol·L-1的下列六种溶液的pH:
|
溶质 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
C6H5ONa |
|
pH |
8.8 |
9.7 |
11.6 |
10.3 |
11.1 |
11.3 |
复分解反应存在这样一个规律:一种较强酸(或碱性较强的物质)可以自发地反应生成较弱酸(或碱性较弱的物质)。依照该规律,请你判断下列反应不能成立的是
▲ (填编号)。
A.CH3COOH+ Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO
D.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
(2)根据前述信息判断,浓度均为0.05mol·L-1的下列六种物质的溶液中,pH最小的是
▲ (填编号);将各溶液分别稀释100倍,pH变化最小的是 ▲ (填编号)。
①C6H5OH ②CH3COOH ③HCN ④HClO ⑤H2SO4 ⑥HClO4
(3)根据前述信息,写出将过量的氯气通入到少量的碳酸钠溶液中反应的离子方程式:
▲ 。
(4)已知CuSO4 + H2S = CuS ↓+ H2SO4 反应成立,是否违反了上述复分解反应规律?你的判断是 ▲ (填“是”或“否”),原因是 ▲ 。(提示:室温下氢硫酸(H2S)K1=1×10-7,K2=1×10-13;CuS的Ksp=6.3×10-36)
(5)标准状况下,向1L含NaOH、Ca(OH)2各0.1 mol的溶液中不断通入CO2至过量,请画出产生的沉淀的物质的量(mol)随CO2通入体积(L)的变化趋势图。

25.(13分)某溶液中的溶质由下列中的几种离子构成:Na+、Fe3+、Cu2+、Ba2+、AlO2-、CO32-、SO32-、SO42-。取该溶液进行有关实验,实验步骤及结果如下:
①向溶液中加入过量稀盐酸,得到气体甲和溶液甲;
②向溶液甲中加入过量NH4HCO3溶液,得到白色沉淀乙、气体乙和溶液乙;
③向溶液乙中加入过量Ba(OH) 2溶液,得到白色沉淀丙、气体丙和溶液丙。
④检验气体甲、气体乙、气体丙,都只含有一种成份,而且各不相同。
请回答下列问题:
(1)只根据实验①能得出的结论是 ▲ 。
(2)沉淀丙中一定含有 ▲ ,可能含有 ▲ 。
(3)该溶液中肯定存在的离子有 ▲ 。
(4)气体乙分子的结构式为 ▲ 。
(5)向溶液甲中加入NH4HCO3溶液至过量,该过程中可能发生反应的离子方程式为
▲ ; ▲ ; ▲ ;(根据需要,可不填完,也可补充)
24.(22分)有一个带正电的小球,质量为m、电量为q,静止在固定的绝缘支架上.现设法给小球一个瞬时的初速度υ0使小求水平飞出,飞出时小球的电量没有改变.同一竖直面内,有一个竖直固定放置的圆环(圆环平面保持水平),环的直径略大于小球直径,如图所示.要使小球能准确进入圆环,可在空间分布匀强电场或匀强磁场(匀强电场和匀强磁场可单独存在,也可同时存在),请设计两种分布方式,并求出:
(1)相应的电场强度E或磁感应强度B的大小和方向;
(2)相应的小球到圆环的时间t .
 (若加匀强电场,则匀强电场限制在竖直面内;若加匀强磁场,则匀强磁场限制在垂直纸面情况.已知υ0>
(若加匀强电场,则匀强电场限制在竖直面内;若加匀强磁场,则匀强磁场限制在垂直纸面情况.已知υ0>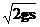 ,小球受重力不能忽略)
,小球受重力不能忽略)
23.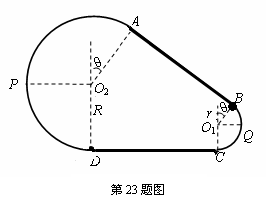 (18分)如图所示为放置在竖直平面内游戏滑轨的模拟装置,滑轨由四部分粗细均匀的金属杆组成,其中倾斜直轨AB与水平直轨CD长均为L=3m,圆弧形轨道APD和BQC均光滑,BQC的半径为r=1m,APD的半径为R=2m,AB、CD与两圆弧形轨道相切,O2A、O1B与竖直方向的夹角均为q=37°.现有一质量为m=1kg的小球穿在滑轨上,以初动能Ek0从B点开始沿BA向上运动,小球与两段直轨道间的动摩擦因数均为μ=
(18分)如图所示为放置在竖直平面内游戏滑轨的模拟装置,滑轨由四部分粗细均匀的金属杆组成,其中倾斜直轨AB与水平直轨CD长均为L=3m,圆弧形轨道APD和BQC均光滑,BQC的半径为r=1m,APD的半径为R=2m,AB、CD与两圆弧形轨道相切,O2A、O1B与竖直方向的夹角均为q=37°.现有一质量为m=1kg的小球穿在滑轨上,以初动能Ek0从B点开始沿BA向上运动,小球与两段直轨道间的动摩擦因数均为μ=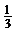 ,设小球经过轨道连接处均无能量损失.求:(g=10m/s2,sin37°=0.6,cos37°=0.8)
,设小球经过轨道连接处均无能量损失.求:(g=10m/s2,sin37°=0.6,cos37°=0.8)
(1)要使小球完成一周运动回到B点,求初动能EK0至少多大;
(2)若小球以第一问Ek0数值从B出发,求小球第二次到达D点时的动能及小球在CD段上运动的总路程.
22.(16分)国庆60周年阅兵中,质量为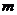 的歼10飞机受阅后返回某机场,降落在跑道上减速过程简化为两个匀减速直线运动.飞机以速度
的歼10飞机受阅后返回某机场,降落在跑道上减速过程简化为两个匀减速直线运动.飞机以速度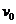 着陆后立即打开减速阻力伞,加速度大小为
着陆后立即打开减速阻力伞,加速度大小为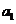 ,运动时间为
,运动时间为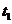 ;随后在无阻力伞情况下匀减速直至停下.在平直跑道上减速滑行总路程为
;随后在无阻力伞情况下匀减速直至停下.在平直跑道上减速滑行总路程为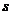 .求:第二个减速阶段飞机运动的加速度大小和时间.
.求:第二个减速阶段飞机运动的加速度大小和时间.
19.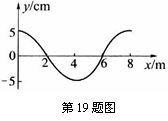 如图所示为一列沿x轴正方向传播的简谐波在某一时刻的波形图,其波源位于坐标原点.波源处质点从平衡位置开始振动经过时间3s通过的路程为15cm.则
如图所示为一列沿x轴正方向传播的简谐波在某一时刻的波形图,其波源位于坐标原点.波源处质点从平衡位置开始振动经过时间3s通过的路程为15cm.则
A.波的周期为4s
B.波速为20m/s
C.x=2m处的质点速度沿x轴的正方向
|
|
 20.如图所示,有两条细束平行单色光a、b射向空气中横截面为矩
20.如图所示,有两条细束平行单色光a、b射向空气中横截面为矩
|
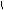
|
|

 只有一束光射出,则下列说法中正确的是
只有一束光射出,则下列说法中正确的是
|
|
B.在玻璃中单色光a的传播速率大于单色光b的传播速率
C.若光束a恰好能使某未知金属发生光电效应,则b也能
D.减小光束与玻璃砖下表面的夹角θ,上表面会有两束平行单色光射出
第Ⅱ卷(非选择题 共10题 共180分)
21Ⅰ.(10分)
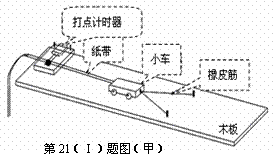 “探究功与物体速度变化的关系”的实验如图(甲)所示,当小车在一条橡皮筋作用下弹出时,橡皮筋对小车做的功记为W. 当用2条、3条……完全相同的橡皮筋并在一起进行第2次、第3次……实验时,使每次实验中橡皮筋伸长的长度都保持一致.每次实验中小车获得的速度由打点计时器所打的纸带测出.
“探究功与物体速度变化的关系”的实验如图(甲)所示,当小车在一条橡皮筋作用下弹出时,橡皮筋对小车做的功记为W. 当用2条、3条……完全相同的橡皮筋并在一起进行第2次、第3次……实验时,使每次实验中橡皮筋伸长的长度都保持一致.每次实验中小车获得的速度由打点计时器所打的纸带测出.
(1)(4分)除了图中已有的实验器材外,还需要导线、开关、 ▲ (填测量工具)和
▲ 电源(填“交流”或“直流”).
(2)(3分)若木板水平放置,小车在两条橡皮筋作用下运动,当小车速度最大时,关于橡皮筋所处的状态与小车所在的位置,下列说法正确的是 ▲ .
A.橡皮筋处于原长状态 B.橡皮筋仍处于伸长状态
C.小车在两个铁钉的连线处 D.小车已过两个铁钉的连线
(3)(3分)在正确操作情况下,打在纸带上的点并不都是均匀的,如图(乙)所示.为了测量小车获得的速度,应选用纸带的 ▲ 部分进行测量(根据下面所示的纸带回答,并用字母表示).


Ⅱ.(12分)
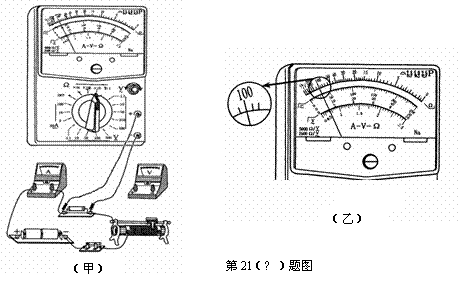
(1)(4分)A同学准备用伏安法测量一只未知阻值的电阻,部分接线完成后,B同学找来多用电表粗测其电阻,如图(甲)所示,请找出图示操作中的一个错误: ▲ .
(2) (4分)A同学帮助B纠错后,选择了欧姆档×10倍率,测量的结果如图(乙)所示,请你读出其阻值大小为 ▲ .为了使多用电表测量的结果更准确,该同学应将选择开关换到 ▲ 挡.
(3) (4分)若再用“伏安法”测量该电阻,其中电压表内阻约为5kΩ,电流表内阻约为5Ω,变阻器阻值为50Ω.图中部分连线已经连接好,为了尽可能准确地测量电阻,请你在答题卷上完成其余的连线.
18.已知某行星绕太阳做匀速圆周运动的半径为r,公转周期为T,万有引力常量为G,下列说法正确的是
A.可求出行星的质量
B.可求出太阳的质量
C.可求出行星的绕行速度
D.据公式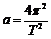 ,行星的向心加速度与半径r成正比
,行星的向心加速度与半径r成正比
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com