
28、(14分)(1)天平(1分);250mL的容量瓶(1分);
(2)不需要(1分),紫色不褪色(1分)。 (3)2Na2SO3+O2→2Na2SO4(2分)
(4)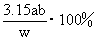 (2分);
(2分);
(5)盐酸提供H+,Ba(NO3)2提供NO3- 形成稀HNO3,将一部分SO32-氧化成SO42-,遇Ba2+结合生成BaSO4沉淀,沉淀质量偏大,导致含量偏高(3分)。
(6)称取样品m1g,加入过量盐酸,测定放出SO2的体积或质量;或其他合理答案(3分)
27、(15分)(每空3分)

26、(15分)
(1)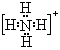 ;水合氢离子;第3周期、ⅢA族。
;水合氢离子;第3周期、ⅢA族。
(2)Al3++3NH3∙H2O =Al(OH)3↓+3NH4+ Al(OH)3+OH― = AlO2―+2H2O
(3)①NH4Al(SO4)2 = NH4++Al3++2SO42― ② a、c、b、e、d。
③150ml;46.6g;
31.(20分)Ⅰ.(12分)右图是遗传病系谱图,控制正常与白化病相对性状的基因用A、a表示。控制正常和红绿色盲的基因用基因B、b表示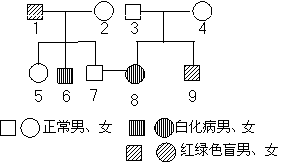 ;请回答:
;请回答:
(1)7号和8号婚配,生一个患白化病男孩的概率是 。所生男孩只患一种病的概率是 。
(2)5号产生aXb配子的概率是 。
(3)若8号患白化病的同时也患多指,但3号手指正常,7号表现型正常(多指为常染色体显性遗传病);则7号和8号婚配后,生一个多指又白化女孩的概率是 。
Ⅱ.(8分)玉米籽粒的有色与白色是一对相对性状,籽粒的饱满与皱缩是另一对相对性状。控制相对性状的基因在细胞核内的染色体上。用纯种有色饱满籽粒的玉米与白色皱缩籽粒的玉米杂交,F1全部表现为有色饱满。请设计一个试验方案,判断这两对性状的遗传是否符合基因的自由组合定律(试验条件满足实验要求)。要求写出方案并对结果作出推断。
30.(22分)
做植物生理实验时,经常用叶片作实验材料,请回答有关问题:
(1)某同学欲测定植物叶片叶绿体的光合作用速率,作如图所示实验。在叶柄基部作环剥处理(仅限制叶片有机物的输入和输出),于不同时间分别在同一叶片上陆续取下面积为1cm2的叶圆片烘干后称其重量,M处的实验条件是将整个实验装置遮光3小时(不考虑取叶圆片后对叶生理活动的影响和温度微小变化对叶生理活动的影响)。测得叶片的叶绿体光合作用速率= 。

(2)可用叶片作实验材料,探究光照的强、弱,CO2的有、无,较高温度与低温对光合速率的影响。
部分实验原理:抽去叶内细胞间隙的空气,充以水分,使叶片沉于水中。若O2在细胞间积累,能使原来下沉的叶片上浮,根据上浮时间长短,即能比较光合作用的强弱。
材料和用具:
棉花植株;测量光强度的照度计;温度计;钻孔器;注射器;恒温水浴;40W日光灯;小烧杯;冷开水;冰块;玻璃管等。
实验步骤:
第1步:用直径1厘米的钻孔器,避开叶脉,打下小圆片60片,放于大注射器中注入水,用注射器抽去气体,当叶圆片全部下沉后连同水倒于小烧杯中,放在黑暗中备用。
第2步:取6只小烧杯,各加含10片叶圆片的相应溶液,作如下表处理,请完成表格。
①
|
杯号 |
光 |
温度 |
CO2 |
|
1 |
强 |
较高 |
|
|
2 |
强 |
较高 |
有 |
|
3 |
强 |
|
有 |
|
4 |
弱 |
较高 |
无 |
|
5 |
弱 |
较高 |
|
|
6 |
弱 |
低 |
有 |
②只运用上述提供的材料和用具,为了得到不同的光强,应如何操作?
;
只运用上述提供的材料和用具,为了得到含有较多CO2和不含CO2的溶液,应如何操作?
。
③预期叶圆片全部上浮所需的平均时间最短的是 号烧杯。通过比较 烧杯的结果,可以说明适当提高温度能提高光合作用速率。比较2号和5号烧杯的结果,可以说明 ;
④分析叶圆片上浮的原因: .
29.(16分)
已知:CH2=CH2+HOCl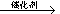 HOCH2CH2Cl
HOCH2CH2Cl
HCHO+CH3COOR(H)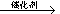 H
H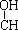 -CH2
-CH2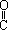 -OR(H)
-OR(H)
杨梅酯是制作冰制食品、糖果等的香料,可用A、E两种烃为原料,经如下路线合成
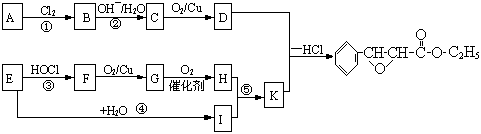
试回答下列问题:
(1)写出结构简式:D ,B ,I 。
(2)上述属于取代反应的有 (选填序号)
(3)分别写出反应F→G,⑤的化学方程式: , 。
(4)有机物甲与杨梅酯互为同分异构,且已知:①结构中除了苯环,无其它环状结构。②1mol甲与足量的NaHCO3溶液反应放出22.4LCO2,与足量的Na反应则放出22.4LH2,与足量的NaOH溶液反应则生成1mol 水。(气体体积均在标准状况下测定)。
则:①1mol甲在氧气中完全燃烧生成CO2和水,共消耗氧气的物质的量为 mol。
②甲中官能团的名称: 。③甲的结构简式(写出一种即可) 。
28、(14分)
为了测定实验室长期存放的Na2SO3固体的纯度,准确称取W g固体样品,配成250 mL溶液。设计了以下三种实验方案:
方案I:取25.00 mL上述溶液,加入足量的盐酸,再加入足量的BaCl2溶液,过滤、洗涤和干燥沉淀,称得沉淀的质量为m1 g
方案Ⅱ:取25.00 mL上述溶液,加入足量的盐酸,再加入足量的的Ba(NO3)2溶液,过滤、洗涤和干燥沉淀,称重,其质量为m2 g
方案Ⅲ:取25.00 mL上述溶液,用a mol/L 的酸性KMnO4溶液进行滴定。(SO32-+MnO4-+H+→SO42-+Mn2++H2O)(未配平),消耗KMnO4溶液b mL。
(1)配制250 mL Na2SO3溶液时,必须用到的实验仪器有:烧杯、玻棒、滴管、药匙和 、 。
(2)在方案Ⅲ中滴定时是否需要选择指示剂? (填“需要”或“不需要”)。滴定终点的颜色变化是 。
(3)写出Na2SO3固体氧化变质的化学方程式 。
(4)用方案Ⅲ的实验数据,计算Na2SO3的纯度为 。
(5)实验中发现,方案Ⅱ测定的Na2SO3纯度比方案I和方案Ⅲ的结果都要低得多。试分析产生上述现象的原因 。
(6)请再设计一个测定Na2SO3固体的纯度的实验方案。 。
27、(15分)
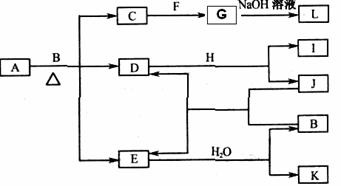 由两种元素组成的化合物A存在如右图所示的转化关系(部分产物及反应条件已略去)。其中E为红棕色气体、D为无色气体,F、H为常见金属单质,J为固态非金属单质。L露置于空气中时,由白色最终转化为红褐色,B与F反应时可生成C,也可生成G。
由两种元素组成的化合物A存在如右图所示的转化关系(部分产物及反应条件已略去)。其中E为红棕色气体、D为无色气体,F、H为常见金属单质,J为固态非金属单质。L露置于空气中时,由白色最终转化为红褐色,B与F反应时可生成C,也可生成G。
试回答下列问题:
(1)写出下列物质的名称:G_______ ____,K_______ ______。
(2)已知A中两种元素原子成最简整数比,且其中一种元素的质量分数为1/15,则A的化学式为_______ ___________。
(3)写出D与H反应的化学方程式
(4)写出L与B的稀溶液反应的离子方程式 。
26.(15分)
由短周期元素组成的A、B、C、D、E、F六种微粒,其中只有C、D是分子,其余四种是离子,且每个微粒中都含有10个电子。已知A、E是由非金属元素组成的阳离子,六种微粒间有下列关系:
①A、B两种离子在加热条件下可生成C、D两种分子;
②通常状况下C的聚集状态为气态,且可使湿润的红色石蕊试纸变蓝;
③1mol B离子与1mol E离子作用可生成2mol D分子;
④向含F离子的溶液中加入C的溶液,可生成白色沉淀W,C溶液过量沉淀也不消失,但再加入含大量B离子或大量E离子的溶液,沉淀W都会溶解。
(1)微粒A的电子式是 ;微粒E的名称是 。构成微粒F的元素在元素周期表中的位置是 。
(2)写出下列反应的离子方程式:F+过量C溶液 ;W+含大量B离子的溶液 。
(3)六种微粒中的两种可与硫酸根形成一种复盐,向该盐的浓溶液中逐滴加入浓苛性钠溶液,产生的现象有:a.溶液中出现白色沉淀 b.有刺激性气味气体放出 c.沉淀逐渐增多 d.沉淀完全消失 e.沉淀逐渐减少
①该复盐在溶液中的电离方程式是 。
②上述各实验现象由先到后出现的正确顺序是(填写序号) 。
③在100 mL浓度为1mol•Lˉ1的该复盐溶液中,加入 mL 1mol•Lˉ1的氢氧化钡溶液,能使产生的沉淀物质的量最多。当加入过量的1mol•Lˉ1的氢氧化钡溶液后,产生的沉淀质量是 g。
25、(20分)
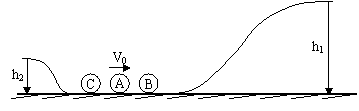
如图所示,体积相同的A、B、C三个小球位于水平面上,mB=mC=mA/2=m。在B、C的两侧分别是高为h1=0.8m、h2=0.2m的平台,平面与平台下沿斜坡间自然相接。B、C两球静止,A以速度V0向右运动。已知A、B的碰撞无能损,A、C的碰撞会粘在一起,球在斜坡上运动时不会脱离,不计一切摩擦, g=10m/s2。
(1)要使B球刚好能被A球撞上平台,则A的初速度至少应为多大?
(2)要使A球能分别将B、C撞上平台(球上了平台后不再返回),则V0满足什么条件?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com