
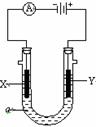
19Θ°(14Ζ÷)ΒγΫβ‘≠άμ‘ΎΜ·―ßΙΛ“Β÷–”–ΙψΖΚ”Π”ΟΓΘ”“ΆΦ±μ Ψ“ΜΗωΒγΫβ≥ΊΘ§ΉΑ”–ΒγΫβ“ΚaΘΜ XΓΔY «ΝΫΩιΒγΦΪΑεΘ§Ά®ΙΐΒΦœΏ”κ÷±ΝςΒγ‘¥œύΝ§ΓΘ«κΜΊ¥π“‘œ¬Έ ΧβΘΚ
(1)»τXΓΔYΕΦ «Εη–‘ΒγΦΪΘ§a «±ΞΚΆNaCl»ή“ΚΘ§ Β―ιΩΣ Φ ±Θ§Ά§ ±‘ΎΝΫ±ΏΗςΒΈ»κΦΗΒΈΖ”ΧΣ ‘“ΚΘ§‘ρ
ΔΌ ΒγΫβ≥Ί÷–XΦΪ…œΒΡΒγΦΪΖ¥”Π ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ‘ΎXΦΪΗΫΫϋΙέ≤λΒΫΒΡœ÷œσ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΔΎ YΒγΦΪ…œΒΡΒγΦΪΖ¥”Π ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ Θ§
Φλ―ιΗΟΒγΦΪΖ¥”Π≤ζΈοΒΡΖΫΖ® «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(2)»γ“Σ”ΟΒγΫβΖΫΖ®ΨΪΝΕ¥÷Ά≠Θ§ΒγΫβ“Κa―Γ”ΟCuSO4»ή“ΚΘ§‘ρ
ΔΌ XΒγΦΪΒΡ≤ΡΝœ «ΓΓΓΓΓΓΓΓΓΓΓΓ Θ§ΒγΦΪΖ¥”Π Ϋ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΔΎ YΒγΦΪΒΡ≤ΡΝœ «ΓΓΓΓΓΓΓΓΓΓΓΓ Θ§ΒγΦΪΖ¥”Π Ϋ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(ΥΒΟςΘΚ‘”÷ ΖΔ…ζΒΡΒγΦΪΖ¥”Π≤Μ±Ί–¥≥ω)
18.(4Ζ÷)”Ο±ξΉΦΒΡNaOHΒΈΕ®Έ¥÷Σ≈®Ε»ΒΡ―ΈΥαΘ§―Γ”ΟΖ”ΧΣΈΣ÷Η ΨΦΝΘ§‘λ≥…≤βΕ®ΫαΙϊΤΪΗΏΒΡ‘≠“ρΩ…Ρή «ΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΘ
ΓΓΓΓ A. ≈δ÷Τ±ξΉΦ»ή“ΚΒΡ«β―θΜ·ΡΤ÷–Μλ”–Na2CO3‘”÷
ΓΓΓΓ B. ΒΈΕ®÷’ΒψΕΝ ΐ ±Θ§Η© ”ΒΈΕ®ΙήΒΡΩΧΕ»Θ§ΤδΥϋ≤ΌΉςΨυ’ΐ»Ζ
ΓΓΓΓ C. ΔΉΑΈ¥÷Σ“ΚΒΡΉΕ–ΈΤΩ”Ο’τΝσΥ°œ¥ΙΐΘ§Έ¥”Ο¥ΐ≤β“Κ»σœ¥
D. ΒΈΕ®ΒΫ÷’ΒψΕΝ ΐ ±ΖΔœ÷ΒΈΕ®ΙήΦβΉλ¥Π–ϋΙ““ΜΒΈ»ή“Κ
 E. Έ¥”Ο±ξΉΦ“Κ»σœ¥Φν ΫΒΈΕ®Ιή
E. Έ¥”Ο±ξΉΦ“Κ»σœ¥Φν ΫΒΈΕ®Ιή
17.(8Ζ÷)”–ΝΫ÷ΜΟή±’ΒΡ»ίΤςAΚΆBΘ§AΡή±Θ≥÷Κψ―ΙΘ§BΡή±Θ≥÷Κψ»ίΓΘΤπ Φ ±œρ»ίΜΐœύΒ»ΒΡΝΫ»ίΤς÷–Ά®»κΧεΜΐ±»ΈΣ2ΘΚlΒΡΒ»ΝΩΒΡS02ΚΆ02Θ§ Ι÷°ΖΔ…ζΖ¥”ΠΘΚ 2S02 +02ΓΓΓΓΓΓ 2S03Θ§≤Δ¥οΒΫΤΫΚβΓΘ‘ρ(Χν<ΓΔ=ΓΔ>ΘΜΉσΓΔ”“ΘΜ‘ω¥σΓΔΦθ–ΓΓΔ≤Μ±δ)ΓΓΓΓ
ΓΓ (1)¥οΒΫΤΫΚβΥυ–ηΒΡ ±ΦδΘΚtAΓΓ tBΘ§S02ΒΡΉΣΜ·¬ ΘΚaA ΓΓΓΓΓΓΓΓaBΓΘΓΓΓΓ
(2)Τπ Φ ±ΝΫ»ίΤς÷–ΒΡΖ¥”ΠΥΌ¬ ΘΚvAΘΏΘΏΘΏΘΏΘΏΘΏΘΏvBΘ§Ζ¥”ΠΙΐ≥Χ÷–ΒΡΖ¥”ΠΥΌ¬ ΘΚvAΘΏΘΏΘΏΘΏΘΏΘΏvB
ΓΓ ΓΓ(3)¥οΒΫΤΫΚβ ±Θ§œρΝΫ»ίΤς÷–Ζ÷±πΆ®»κΒ»ΝΩΒΡκ≤ΤχΓΘA»ίΤς÷–ΒΡΜ·―ßΤΫΚβœρΓΓ Ζ¥”ΠΖΫœρ“ΤΕ·Θ§B»ίΤς÷–ΒΡΜ·―ßΖ¥”ΠΥΌ¬ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓ (4)¥οΒΫΤΫΚβΚσΘ§œρΝΫ»ίΤς÷–Ζ÷±πΆ®»κΒ»ΝΩΒΡ‘≠Ζ¥”ΠΤχΧεΘ§‘Ό¥Έ¥οΒΫΤΫΚβ ±Θ§A»ίΤς÷–ΒΡS02ΒΡΑΌΖ÷Κ§ΝΩΓΓΓΓ Θ§B»ίΤς÷–S02ΒΡΑΌΖ÷Κ§ΝΩ ΓΓΓΓΓΓΓΘΓΓ
16Θ°(6Ζ÷)”…«βΤχΚΆ―θΤχΖ¥”Π…ζ≥…1molΥ°’τΤχΖ≈»»241.8kJ–¥≥ωΗΟΖ¥”ΠΒΡ»»Μ·―ßΖ¥”ΠΖΫ≥Χ ΫΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ»τ1gΥ°’τΤχΉΣΜ·ΈΣ“ΚΧ§Υ°Ζ≈»»2.444kJΘ§‘ρΖ¥”ΠH2(g)+1/2O2(g)=H2O(g)ΒΡΓςH=ΓΓΓΓ kJΓΛmol-1ΓΘ«βΤχΒΡ»Φ…’»»ΈΣΓΓΓΓΓΓΓΓΓΓΓΓ kJΓΛmol-1ΓΘ
15Θ°(6Ζ÷)œ¬Ν–10÷÷Έο÷ ÷–ΘΚΔΌNaOH»ή“Κ ΔΎH2SO4 ΔέΝρΥαΆ≠ΨßΧε ΔήCu ΔίCH3COOHΓΓ ΔόNaOHΙΧΧε ΔΏ’αΧ« Δύ ·Μ“Υ° ΔαΥ°“χ ΔβΑ±Υ°
ΡήΒΦΒγΒΡ”–ΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ τ”Ύ«ΩΒγΫβ÷ ΒΡ”–ΓΓΓΓΓΓΓΓ ΘΜ τ”Ύ»θΒγΫβ÷ ΒΡ”–ΓΓΓΓΓΓΓΓ ΓΘ
14Θ°‘ΎΈ¬Ε»ΓΔ»ίΜΐœύΆ§ΒΡ3ΗωΟή±’»ίΤς÷–Θ§Α¥≤ΜΆ§ΖΫ ΫΆΕ»κΖ¥”ΠΈοΘ§±Θ≥÷ΚψΈ¬ΓΔΚψ»ίΘ§≤βΒΟΖ¥”Π¥οΒΫΤΫΚβ ±ΒΡ”–ΙΊ ΐΨί»γœ¬(“―÷Σ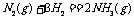 ®SH=-92.4kJΓΛmol-1)
®SH=-92.4kJΓΛmol-1)
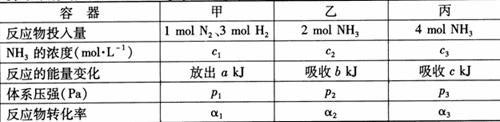
œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
A. 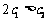 ΓΓB.
ΓΓB. 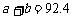 ΓΓC.
ΓΓC. 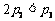 ΓΓΓΓD.
ΓΓΓΓD. 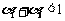
ΒΎIIΨμ
13. ≥ΘΈ¬œ¬Θ§”Ο 0.1000 molΓΛL-1 NaOH»ή“ΚΒΈΕ® 20.00ml 0.10000 molΓΛL-1 CH3COOH»ή“ΚΒΈΕ®«ζœΏ»γ”“ΆΦΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
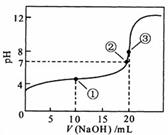 A. ΒψΔΌΥυ Ψ»ή“Κ÷–ΘΚ
A. ΒψΔΌΥυ Ψ»ή“Κ÷–ΘΚ
c(CH3COO-)+ c(OH-)= c(CH3COOH)+ c(H+)
B. ΒψΔΎΥυ Ψ»ή“Κ÷–ΘΚ
c(Na+)= c(CH3COOH)+ c(CH3COO-)
C. ΒψΔέΥυ Ψ»ή“Κ÷–ΘΚ
c(Na+)> c(OH-)>(CH3COO-)> c(H+)
D. ΒΈΕ®Ιΐ≥Χ÷–Ω…Ρή≥ωœ÷ΘΚ
c(CH3COOH)> c(CH3COO-) > c(H+)> c(Na+)> c(OH-)
12.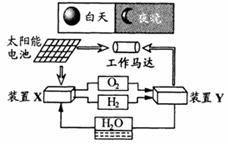 ”“ΆΦ «“Μ÷÷ΚΫΧλΤςΡήΝΩ¥Δ¥φœΒΆ≥‘≠άμ Ψ“βΆΦΓΘ
”“ΆΦ «“Μ÷÷ΚΫΧλΤςΡήΝΩ¥Δ¥φœΒΆ≥‘≠άμ Ψ“βΆΦΓΘ
ΓΓ œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
ΓΓ A. ΗΟœΒΆ≥÷–÷Μ¥φ‘Ύ3÷÷–Έ ΫΒΡΡήΝΩΉΣΜ·
ΓΓ B. ΉΑ÷ΟY÷–ΗΚΦΪΒΡΒγΦΪΖ¥”Π ΫΈΣΘΚ
O2+2H2O+4e-=4OH-
ΓΓ C. ΉΑ÷ΟXΡή Βœ÷»ΦΝœΒγ≥ΊΒΡ»ΦΝœΚΆ―θΜ·ΦΝ‘Ό…ζ
ΓΓ D. ΉΑ÷ΟXΓΔY–Έ≥…ΒΡΉ”œΒΆ≥Ρή Βœ÷Έο÷ ΒΡΝψ≈≈Ζ≈Θ§
≤ΔΡή Βœ÷Μ·―ßΡή”κΒγΡήΦδΒΡΆξ»ΪΉΣΜ·
11.”ΟΥ°œΓ Ά0.1mol/LΑ±Υ° ±Θ§»ή“Κ÷–ΥφΉ≈Υ°ΝΩΒΡ‘ωΦ”ΕχΦθ–ΓΒΡ «
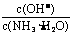
A.ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
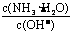
BΘ°ΓΓ
C.c(H+)ΚΆc(OH-)ΒΡ≥ΥΜΐ
ΓΓΓΓ D.OH-ΒΡΈο÷ ΒΡΝΩ
10. œ¬Ν– Β―ι≤ΌΉς”κ‘ΛΤΎ Β―ιΡΩΒΡΜρΥυΒΟ Β―ιΫα¬έ“Μ÷¬ΒΡ «
|
―Γœν |
Β―ι≤ΌΉς |
Β―ιΡΩΒΡΜρΫα¬έ |
|
A |
Ρ≥ΦΊ―Έ»ή”Ύ―ΈΥαΘ§≤ζ…ζΡή Ι≥Έ«ε ·Μ“Υ°±δΜκΉ«ΒΡΈό…ΪΈόΈΕΤχΧε |
ΥΒΟςΗΟΦΊ―Έ «K2CO3 |
|
B |
œρΚ§”–…ΌΝΩFeCl3ΒΡMgCl2»ή“Κ÷–Φ”»κΉψΝΩMg(OH)2ΖέΡ©Θ§ΫΝΑη“ΜΕΈ ±ΦδΚσΙΐ¬Υ |
≥ΐ»ΞMgCl2»ή“Κ÷–…ΌΝΩFeCl3 |
|
C |
≥ΘΈ¬œ¬Θ§œρ±ΞΚΆNa2CO3»ή“Κ÷–Φ”…ΌΝΩBaSO4ΖέΡ©Θ§Ιΐ¬ΥΘ§œρœ¥ΨΜΒΡ≥ΝΒμ÷–Φ”œΓ―ΈΥαΘ§”–Τχ≈ί≤ζ…ζ |
ΥΒΟς≥ΘΈ¬œ¬ Ksp(BaCO3)<Ksp(BaSO4) |
|
D |
C2H5OH”κ≈®ΝρΥα170ΓφΙ≤»»Θ§÷ΤΒΟΒΡΤχΧεΆ®»ΥΥα–‘KMnO4»ή“Κ |
Φλ―ι÷ΤΒΟΤχΧε «ΖώΈΣ““œ© |
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com