
20.(09年山东理综·28)(14分)运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
(1)合成氨反应N2(g)+3H2(g) 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”、“向右”或“不”);使用催化剂 反应的△H(填“增大”、“减小”或“不改变”)。
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”、“向右”或“不”);使用催化剂 反应的△H(填“增大”、“减小”或“不改变”)。
(2)已知:O2(g) = O2+(g)+e-
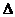 H1=1175.7
kJ·mol-1
H1=1175.7
kJ·mol-1
PtF6(g)+e-=PtF6-(g)
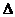 H2=-771.1
kJ·mol-1
H2=-771.1
kJ·mol-1
O2PtF6(S)=O2+(g)+PtF6-(g)
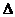 H3=482.2
kJ·mol-1
H3=482.2
kJ·mol-1
则反应O2(g)+PtF6(g) = O2+PtF6-(s)的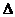 H=_____________
kJ·mol-1。
H=_____________
kJ·mol-1。
(3)在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成 沉淀(填化学式),生成该沉淀的离子方程式为 。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20。
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应时溶液中c(NH4*)=c(Cl-)。则溶液显 性(填“酸”、“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb= 。
答案:(1)向左 不改变
(2)-77.6
(3)Cu(OH)2 Cu2++2NH3·H2O = Cu(OH)2↓ +2NH4+
(4)中 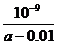 mol·L-1
mol·L-1
19.

 (09年上海化学·25)铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
(09年上海化学·25)铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
 (1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:Fe2O3(s)+3CO(g)
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)
 ①该反应的平衡常数表达式为:K=
。
①该反应的平衡常数表达式为:K=
。
 ②该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单
②该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单
 质铁11.2g。则10min内CO的平均反应速率为
。
质铁11.2g。则10min内CO的平均反应速率为
。
 (2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
 ①
②
。
①
②
。
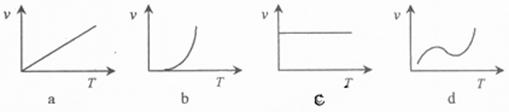
 (3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)
(3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v) 和温度(T)的关系示意图中与铝热反应最接近的是
。
和温度(T)的关系示意图中与铝热反应最接近的是
。

 (4)写出氢氧化铝在水中发生酸式电离的电离方程式:
,
(4)写出氢氧化铝在水中发生酸式电离的电离方程式:
,
 欲使上述体系中Al3+浓度增加,可加入的物质是
。
欲使上述体系中Al3+浓度增加,可加入的物质是
。
答案:(本题共8分)
 (1)
(1)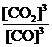

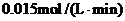
 (2)①CO或(CO2)的生成速率与消耗速率相等;②CO(或CO2)的质量不再改变(合理即给分)
(2)①CO或(CO2)的生成速率与消耗速率相等;②CO(或CO2)的质量不再改变(合理即给分)
 (3)b
(3)b
 (4)Al(OH)3
(4)Al(OH)3 H++AlO2-+H2O 盐酸(合理即给分)
H++AlO2-+H2O 盐酸(合理即给分)
1.(1)<;(2)88×10-4 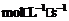 ;
;
(3)5000;(4)C、D;
(5)①280;1.20×10-3;5.80×10-3;1.20×10-3;5.80×10-3;
②如图:
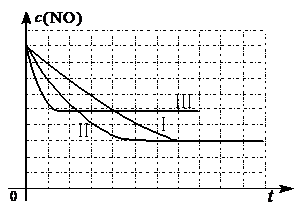
18.(09年浙江理综·27)[15分]超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO 2CO2+N2。
2CO2+N2。
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
|
时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
|
c(NO)(mol/L) |
1.00×10-3 |
4.50×10-4 |
2.50×10-4 |
1.50×10-4 |
1.00×10-4 |
1.00×10-4 |
|
c(CO)(mol/L) |
3.60×10-3 |
3.05×10-3 |
2.85×10-3 |
2.75×10-3 |
2.70×10-3 |
2.70×10-3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H 0(填写“>”、“<”、“=”)。
(2)前2s内的平均反应速率v(N2)= 。
(3)在该温度下,反应的平衡常数K= 。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是 。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
|
实验 编号 |
T(℃) |
NO初始浓度 (mol/L) |
CO初始浓度 (mol/L) |
催化剂的比表面积(m2/g) |
|
Ⅰ |
280 |
1.20×10-3 |
5.80×10-3 |
82 |
|
Ⅱ |
|
|
|
124 |
|
Ⅲ |
350 |
|
|
124 |
①请在上表空格中填入剩余的实验条件数据。
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号。
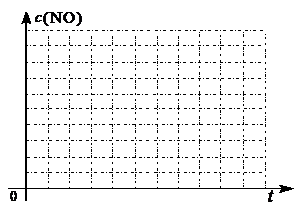
答案:[14分]
17.(09年重庆理综·13)各可逆反应达平衡后,改变反应条件,其变化趋势正确的是
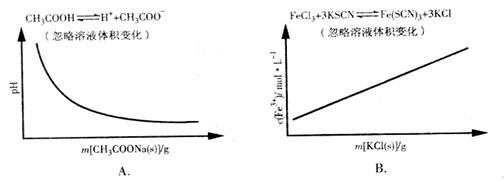
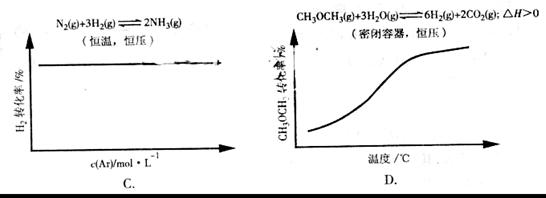
答案:D
15.(09年四川理综·13)在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g) nY(g) △H=QkJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气
nY(g) △H=QkJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气
体体积的关系如下表所示:
 气体体积 气体体积c(Y)/mol·L-1 温度℃ |
1 |
2 |
3 |
|
100 |
1.00 |
0.75 |
0.53 |
|
200 |
1.20 |
0.09 |
0.63 |
|
300 |
1.30 |
1.00 |
0.70 |
下列说法正确的是
A.m>n
B.Q<0
C.温度不变,压强增大,Y的质量分数减少
D.体积不变,温度升高,平衡向逆反应方向移动
答案:C
16 .(09年天津理综·5)人体血液内的血红蛋白(Hb)易与O2结合生成HbO2,因此具有输氧能力,CO吸入肺中发生反应:CO+HbO2
.(09年天津理综·5)人体血液内的血红蛋白(Hb)易与O2结合生成HbO2,因此具有输氧能力,CO吸入肺中发生反应:CO+HbO2 O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是
O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是
 A.CO与HbO2反应的平衡常数K=
A.CO与HbO2反应的平衡常数K=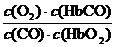
 B.人体吸入的CO越多,与血红蛋白结合的O2越少
B.人体吸入的CO越多,与血红蛋白结合的O2越少
 C.当吸入的CO与O2浓度之比大于或等于0.02时,人的智力才会受损
C.当吸入的CO与O2浓度之比大于或等于0.02时,人的智力才会受损
 D.把CO中毒的病人放入高压氧仓中解毒,其原理是使上述平衡向左移动
D.把CO中毒的病人放入高压氧仓中解毒,其原理是使上述平衡向左移动
 答案:C
答案:C
12.(09年山东理综·14)2SO2(g)+O2(g)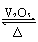 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
A.催化剂V2O5不改变该反应的逆反应速率
B.增大反应体系的压强、反应速度一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,SO3(g)的浓度分别是c1,c2,则时间间隔t1-t2内,SO3(g)生成的平均速率为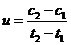

答案:D
 13
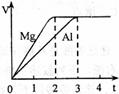
13 .(09年上海化学·15)镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生
.(09年上海化学·15)镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生 气体的体积(V)与时间(t)关系如右图。反应中镁和铝的
气体的体积(V)与时间(t)关系如右图。反应中镁和铝的
 A.物质的量之比为3︰2 B.质量之比为3︰2
A.物质的量之比为3︰2 B.质量之比为3︰2
 C.摩尔质量之比为2︰3 D.反应速率之比为2︰3
C.摩尔质量之比为2︰3 D.反应速率之比为2︰3
答案:A
14 .(09年上海化学·21)下列坐标图所表示的量的关系错误的是
.(09年上海化学·21)下列坐标图所表示的量的关系错误的是

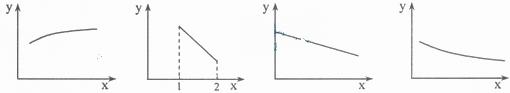
 烷烃分子中碳原子数x与 NOx溶于水完全转化 氯化钠溶液中加水的量x 酒精水溶液中质量
烷烃分子中碳原子数x与 NOx溶于水完全转化 氯化钠溶液中加水的量x 酒精水溶液中质量
 碳的质量分数y的关系 为硝酸,x与消耗氧气 与溶质的质y的关系 分数x与酒精水溶液
碳的质量分数y的关系 为硝酸,x与消耗氧气 与溶质的质y的关系 分数x与酒精水溶液
 的量y的关系
密度y的关系
的量y的关系
密度y的关系
 A. B. C. D.
A. B. C. D.
答案:C
11.(09年全国理综卷I·13)下图表示反应X(g) 4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化曲线:
4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化曲线:
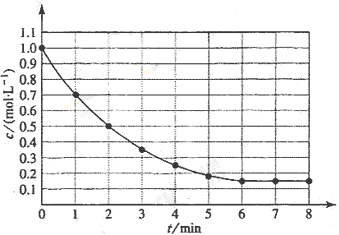
下列有关该反应的描述正确的是
A.第6min后,反应就终止了
B.X的平均转化率为85%
C.若升高温度,X的平均转化率将大于85%
D.若降低温度,v正和v逆将以同样倍数减小
答案:B
10.(09年宁夏理综·13)在一定温度下,反应H2(g)+X2(g) HX(g)的平衡常数为10。若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于
HX(g)的平衡常数为10。若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于
A.5% B.17% C.25% D.33%
答案:B
9.(09年宁夏理综·10)硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是
|
实验 |
反应温度/℃ |
Na2S2O3溶液 |
稀H2SO4 |
H2O |
||
|
V/mL |
c/mol·L-1 |
V/mL |
c/mol·L-1 |
V/mL |
||
|
A |
25 |
5 |
0.1 |
10 |
0.1 |
5 |
|
B |
25 |
5 |
0.2 |
5 |
0.2 |
10 |
|
C |
35 |
5 |
0.1 |
10 |
0.1 |
5 |
|
D |
35 |
5 |
0.2 |
5 |
0.2 |
10 |
答案:D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com