
8、下列物质中所有原子不全是稳定结构的是( )
A、HCl B、CH3CHO C、BeCl2 D、NaCl
7、下列分子中所有原子都满足最外层为8电子结构的是( )
A、BF3 B、H2S C、SiCl4 D、PCl5
6、32S与33S互为同位素,下列说法正确的是( )
A、32S与33S原子的最外层电子数均为2 B、32S与33S具有相同的质子数
C、32S与33S具有不同的电子数 D、32S与33S具有相同的中子数
5、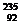 U是重要的核工业原料,在自然界的丰度很低。
U是重要的核工业原料,在自然界的丰度很低。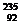 U的浓缩一直为国际社会关注。下列有关
U的浓缩一直为国际社会关注。下列有关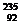 U说法正确的是(
)
U说法正确的是(
)
A、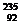 U原子核中含有92个中子 B、
U原子核中含有92个中子 B、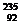 U原子核外有153个电子
U原子核外有153个电子
C、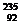 U与
U与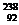 U互为同位素 D、
U互为同位素 D、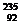 U与
U与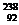 U互为同素异形体
U互为同素异形体
4、13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,KurtW ü thrich等人为此获得2002年诺贝尔化学奖。下面有关13C、15N叙述正确的是( )
A、13C与15N有相同的中子数 B、13C与C60互为同素异形体
C、15N与14N互为同位素 D、15N的核外电子数与中子数相同
3、据报道,月球上有大量3He存在, 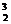 He可以作为核聚变材料。下列关于
He可以作为核聚变材料。下列关于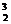 He的叙述正确的是( )
He的叙述正确的是( )
A、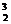 He和
He和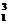 H互为同位素 B、比4He少一个质子
H互为同位素 B、比4He少一个质子
C、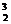 He原子核外电子数为2 D、
He原子核外电子数为2 D、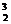 He原子核内有2个质子和3个中子
He原子核内有2个质子和3个中子
2、据报道,某些建筑材料会产生放射性同位素氡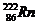 ,从而对人体产生伤害,该同位
,从而对人体产生伤害,该同位
素原子的中子数和质子数之差是( ) A、136 B、50 C、86 D、222
1、分析发现,某陨石中含有半衰期极短的镁的一种放射性同位素28Mg,该同位素的原子核内的中子数是( )A、12 B、14 C、16 D、18
12、盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe203(s)+3CO(g)=2Fe(s)+3C02(g) △H=-24.8kJ/mol
Fe203(s)+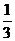 CO(g)==
CO(g)== 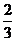 Fe3O4(s)+
Fe3O4(s)+ 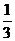 C02(g)
△H=-15.73kJ/mol
C02(g)
△H=-15.73kJ/mol
Fe304(s)+CO(g)==3FeO(s)+C02(g) △H=+640.4kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:
_________________
11、(1)1g碳与适量水蒸气反应生成一氧化碳和氢气,需吸收10.94KJ热量,此反应的热化学方程式为__________________________________________。
(2)奥运会圣火燃料中成份之一是丙烷,标准状况下4.48L丙烷完全燃烧生成二氧化碳和液态水时放出150.1 kJ的热量,则丙烷燃烧的热化学方程式中为____________________。
(3)家用液化气中的主要成分之一是丁烷,当10 kg丁烷完全燃烧并生成二氧化碳和液态水时,放出热量为5×105kJ,试写出丁烷燃烧反应的热化学方程式 。已知1 mol液态水汽化时需要吸收44 kJ的热量,则1 mol丁烷完全燃烧并生成气态水时放出的热量为 kJ。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com