
12.(7分)下表中的数据是破坏1mol 物质中的化学键所消耗的能量(kJ):
|
物质 |
Cl2 |
Br2 |
I2 |
H2 |
HF |
HCl |
HBr |
HI |
|
能量 (kJ) |
243 |
193 |
151 |
436 |
565 |
432 |
366 |
298 |
根据上述数据回答(1)-(5)题。
(1)下列单质本身具有的能量最低的是:
A.H2 B.Cl2 C. Br2 D. I2
(2)下列氢化物中最稳定的是:
A.HCl B.HBr C.HI D..HF
(3)X2 + H2=2HX (X代表Cl、Br、I)的反应是吸热反应还是放热反应?
答:_________________________________________________。
(4)相同条件下,X2(X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是_____________________。
(5)若无上表中的数据,你能正确回答出问题(4)吗?
答:___________________ 你的根据是___________________________________.
11.(8分)A、B、C三种常见的短周期元素可以形成AB2、C2B、AB3、C2B2、B2等物质。已知B离子和C离子有相同的电子层结构,A离子比B离子多一个电子层,请回答:
(1)A元素的名称是 ,B元素的符号是 ,C离子的电子式是 。
(2)用电子式表示C2B的形成过程 。
(3)AB3常温下为 态,AB3的水化物在低温下跟C2B2反应生成一种稳定性较差的过氧化物,该反应的化学方程式是 。
(4)AB3的水化物溶液跟C2A溶液反应的离子方程式是 ,此反应物之一跟AB2反应的化学方程式是 。
10.(6分)溴化碘(IBr)的化学性质类似于卤素化合物,试回答下列问题:
(1)溴化碘的电子式是 ,它是由 键形成的 化合物。
(2)溴化碘与水反应的化学方程式为 。
9.(6分)指出下列物质中化学键的类型:
①H2O2 ②Na2O2 ③CO2
④HClO ⑤Ca(OH)2 ⑥HBr
8.( 08·海南卷)白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P akJ·mol-1、P-O bkJ·mol-1、P=O ckJ·mol-1、O=O dkJ·mol-1。
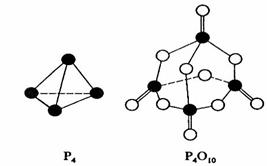
根据图示的分子结构和有关数据估算该反应的△H,其中正确的是 ( )
A.(6a+5d-4c-12b)kJ·mol-1 B.(4c+12b-6a-5d)kJ·mol-1
C.(4c+12b-4a-5d)kJ·mol-1 D.(4a+5d-4c-12b)kJ·mol-1
7.(09·广东卷)下列说法正确的是 ( )
A.MgSO4晶体中只存在离子键
B.含Ca2+、Mg2+的水都是硬水
C.雾是气溶胶,在阳光下可观察到丁达尔效应
D.玻璃是氧化物,成分可表示为Na2O▪CaO▪6SiO2
6.下列关于化学键的叙述正确的是 ( )
A.化学键既存在于相邻原子之间,又存在与相邻分子之间
B.两个原子之间的相互作用叫化学键
C.化学键通常指的是相邻的两个或多个原子之间的强相互作用
D.阴阳离子之间有强烈的吸引作用而没有排斥作用,所以离子键的核间距相当小
5.下列说法正确的是 ( )
①化学键存在于原子之间,也存在于分子之间 ②两种非金属原子不能形成离子键 ③金属元素和非金属元素相化合时,一定形成离子键 ④不同种元素组成的多原子分子里的化学键一定是极性键 ⑤离子键和极性键只存在于化合物中 ⑥非金属元素之间不可能组成离子化合物 ⑦离子化合物中一定含有非金属元素 ( )
A.①②④⑥ B.②⑤⑦ C.②④⑤⑥ D.②⑤⑥⑦
4.( 08·全国卷)对于IVA族元素,下列叙述中不正确的是 ( )
A.SiO2和CO2中,Si和O,C和O之间都是共价键
B.C、Si和Ge的最外层电子数都是4,次外层电子数都是8
C.CO2和SiO2都是酸性氧化物,在一定条件下都能和氧化钙反应
D.该族元素的主要化合价是+4和+2
3.( 08·上海卷)已知:H2(g)+F2(g)→2HF(g)+270kJ,下列说法正确的是 ( )
A.2L氟化氢气体分解成1L氢气与1L氟气吸收270kJ热量
B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出热量小于270 kJ
C.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量
D.1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270热量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com