
5.温度为0℃,压强为505kPa时,CO2气体的气体摩尔体积是22.4L·mol-1
4.标准状况下,一定量的任何气体的体积都约是22.4L
3.1mol任何物质的体积在标准状况下都约是22.4L
2.1molH2O在标准状况下的体积是22.4L
1.1molH2的体积是22.4L
2.气体摩尔体积:单位物质的量的气体所占的体积
符号Vm ,表达式:Vm=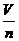 ,单位:
(L·mol-1)(
,单位:
(L·mol-1)(
在标准状况下,1mol任何气体的体积都约是 。即标准状况下Vm=
(练习)判断下列说法是否正确?为什么?
1.决定物质体积的因素: 、 、
当微粒数一定时(1mol),决定体积大小的因素是 和 。
2.摩尔质量与相对原子质量、相对分子质量的关系:1mol任何原子的质量,以g为单位在数值上等于该原子的相对原子质量;1mol任何分子的质量以g为单位,在数值上等于该分子的相对分子质量。
(练习)
①O的相对原子质量为 ,1molO的质量为 ,M(O)=
②H2的相对分子质量为 ,1molH2的质量为 ,M(H2)=
③H2O的相对分子质量为 ,1molH2O的质量为 ,M(H2O)= (
(小结)摩尔质量:M=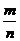 (g·mol-1)((
(g·mol-1)((
(例1)483gNa2SO4·10H2O中含Na+和SO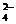 的物质的量各是多少?所含水分子的数目是多少?
的物质的量各是多少?所含水分子的数目是多少?
解:
(总结)
N n m
有了物质的量、M和NA 反应方程式中的量的关系就可以用物质的量表示
如: H2 (g) + Cl2(g) = 2HCl (g)
微粒数比 1 ∶ 1 ∶ 2
质量比 2 ∶ 71 ∶ 73
物质的量比1 ∶ 1 ∶ 2
物质的量在化学方程式中的意义
1.摩尔质量:单位物质的量的物质所具有的质量,符号M,单位g·mol-1
4.阿伏加德罗常数是有单位的(mol-1)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com