
5ЃЎЁАетЪЧвЛИіЛЎЪБДњЕФЭЛЦЦКЭзюКЇШЫЬ§ЮХЕФЩчЛсНсЙЙЃЌУЛгаЗтЙњЗтОєЃЌУЛгаЙЋКюВЎзгФаЁЃЁЁгШЦфЪЧШхМвбЇепИќЪЧДѓЛѓВЛНтЃЌЖјЧвВЛОУОЭДѓЦ№ПжЛХЃЌетМђжБОЭЪЧДђЫщЫћУЧЕФЗЙЭыСЫЁБЁЃетИіЪБДњЪЧжИ ЁЁ AЃЎДКЧяеНЙњЁЁЁЁЁЁЁЁ ЁЁ BЃЎЧиДњЁЁЁЁЁЁ ЁЁЁЁЁЁCЃЎККДњЁЁЁЁЁЁЁЁЁЁ ЁЁDЃЎЬЦЫЮЪБЦк 6ЃЎИљОнЁЖКгЖЋЯШЩњМЏОэЕкШ§ЁЄЗтНЈТлЁЗХаЖЯЃЌетЦЊЮФеТЕФжїЬтПЩФмЪЧТлЪі
AЃЎЗтНЈжЦЖШЁЁЁЁЁЁЁЁ BЃЎзкЗЈжЦЖШЁЁЁЁЁЁ CЃЎПЄЯижЦЖШЁЁЁЁЁЁ DЃЎЗжЗтжЦЖШ
4ЃЎЙигкжаЙњаеЪЯЕФЦ№дДЃЌЬЦШЫСјЗМЫЕЃКЁАЪЯгкЙњЃЌдђЦыТГЧиЮтЃЛЪЯгккжЃЌдђЮФЮфГЩаћЁЁЪЯгкЪТЃЌдђЮзввНГЬеЁЃЁБгЩДЫРрЭЦЃЌЭѕЁЂКюЁЂЙЋЫяЕШаеЪЯгІдДзд
AЃЎзхКХЁЁЁЁЁЁ BЃЎвиУћЁЁЁЁЁЁЁЁ CЃЎОєКХЁЁЁЁЁЁЁЁЁЁ DЃЎЙйУћ
3ЃЎДКЧяГѕЦкЃЌГўЙњО§жїЪзЯШГЦЭѕЁЃЫцКѓЮтдНЕШЙњЙњО§вВЯрМЬГЦЭѕЁЃЩЯЪіЯжЯѓБОжЪЩЯЗДгГСЫ
AЃЎО§жїзЈжЦЕФЖЏвЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎНФЯОМУГЌЙ§ББЗНЁЁ
CЃЎЗжЗтжЦЕФЖЏвЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎжмЭѕжСз№ЕиЮЛЕФЖЏвЁ
2ЃЎЮвЙњЙХДњЮФЯзжаОГЃЛсГіЯжЁААйЪРВЛЧЈжЎзкЁБЃЌетжИЕФЪЧ
AЃЎДѓзкжаЕФГЄзгЁЁЁЁ BЃЎДѓзкжаЕФЪќзгЁЁ CЃЎаЁзкжаЕФГЄзгЁЁЁЁ DЃЎаЁзкжаЕФЪќзг
1ЃЎОнЁЖЪЗМЧЁЄвѓБОМЭЁЗдиЃКЁАзджаЖЁвдРДЃЌЗЯЕеЖјИќСЂжюЕмзгЃЌЕмзгЛђељЯрДњСЂЁБЃЌДгЖјГіЯжЁАБШОХЪРТвЁБЁАжюКюФЊГЏЁБЕФОжУцЁЃетЪЧвђЮЊ
AЃЎУЛгазёбзкЗЈжЦддђЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎЗжЗтжЦдтЕНЦЦЛЕ
CЃЎРёБРРжЛЕЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЫ№КІСЫжюКюЙњЕФРћвц
23ЃЎ(7Зж)ЪЕбщЪвРяГЃгУХЈбЮЫсгыЖўбѕЛЏУЬЗДгІРДжЦШЁЩйСПЕФТШЦјЃЌЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК
MnO2+4HCI(ХЈ) 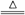 MnCl2+C12Ёќ+2H2O
MnCl2+C12Ёќ+2H2O
ШЁвЛЖЈСПЕФХЈбЮЫсЪЙЦфгыЖўбѕЛЏУЬЗЂЩњЗДгІЃЌВњЩњЕФТШЦјдкБъзМзДПіЯТЕФЬхЛ§ЮЊ22.4LЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
(1)ИУЗДгІЕФРызгЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)ЗДгІжаБЛбѕЛЏЕФHClЕФЮяжЪЕФСПЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)ЪЕбщЪвБИгУЕФХЈбЮЫсжЪСПЗжЪ§ЮЊ36ЃЎ5%ЃЌУмЖШЮЊ1ЃЎ19gЁЄcm-3,ЁЁ ЮЊЪЙгУЗНБуЃЌЧыМЦЫуГіИУХЈбЮЫсЕФЮяжЪЕФСПХЈЖШ:ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
22ЃЎ(12Зж)AЁЂBЁЂCЁЂDЪЧЫФжжЖЬжмЦкдЊЫиЃЌЫќУЧЕФдзгађЪ§вРДЮдіДѓЃЌЦфжаAЁЂCМАBЁЂDЗжБ№ЪЧЭЌвЛжїзхдЊЫиЃЌBЁЂDСНдЊЫиЕФдзгКЫжажЪзгЪ§жЎКЭЪЧAЁЂCСНдЊЫидзгКЫжажЪзгЪ§жЎКЭЕФСНБЖЃЌгжжЊЫФжждЊЫиЕФЕЅжЪжагаСНжжЦјЬхЁЂСНжжЙЬЬхЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
(1)BЁЂDдкжмЦкБэжаЭЌДІдк_____зхЃЌBЕФдзгНсЙЙЪОвтЭМЪЧ_______ЃЌЯТСаПЩвдбщжЄBгыDСНдЊЫидзгЕУЕчзгФмСІЧПШѕЕФЪЕбщЪТЪЕЪЧ__________(ЬюаДБрКХ)ЃЛ
AЃЎБШНЯетСНжждЊЫиЕФЦјЬЌЧтЛЏЮяЕФЗаЕу
BЃЎБШНЯетСНжждЊЫиЕФдзгЕФЕчзгВуЪ§
CЃЎБШНЯетСНжждЊЫиЕФЦјЬЌЧтЛЏЮяЕФЮШЖЈад
DЃЎБШНЯетСНжждЊЫиЕФЕЅжЪгыЧтЛЏКЯЕФФбвз
(2)аДГіСНжжОљКЌAЁЂBЁЂCЁЂDЫФжждЊЫиЕФЛЏКЯЮяЯрЛЅМфЗЂЩњЗДгІЃЌЧвЩњГЩЦјЬхЕФРызгЗНГЬЪН______________________________________________ЃК
(3)AЁЂBЁЂDМфПЩаЮГЩМзЁЂввСНжжЮЂСЃЃЌЫќУЧОљЮЊИКвЛМлЫЋдзгвѕРызгЃЌЧвМзга18ИіЕчзгЃЌввгаl0ИіЕчзгЃЌдђМзгыввЗДгІЕФРызгЗНГЬЪНЮЊ________________ЃЛ
(4)DдЊЫиЕФЦјЬЌЧтЛЏЮяКЭЦфЕЭМлбѕЛЏЮяФмЗДгІЩњГЩDЕФЕЅжЪЃЎИУЗДгІжабѕЛЏВњЮягыЛЙдВњЮяЕФЮяжЪЕФСПжЎБШЮЊ_________________ЁЃ
21ЃЎ(6Зж)Ш§ЗњЛЏЕЊ(NF3)ЪЧвЛжжЮоЩЋЁЂЮоЮЖЕФЦјЬхЃЌЫќЪЧЮЂЕчзгЙЄвЕММЪѕДДаТБиВЛПЩЩйЕФЙиМќдСЯжЎвЛЃЌПЩгЩАБЦјКЭЗњЦјЗДгІЕУЕНЃК4NH3+3F2 = NF3+3NH4FЁЃдђЃК
(1)ЩЯЪіЗДгІжаЃЌбѕЛЏМСгыЛЙдМСЕФЮяжЪЕФСПжЎБШЮЊ_________ЃЛШєЗДгІжага0.5 mol NH3 БЛбѕЛЏЃЌзЊвЦЕчзгЕФЪ§ФПЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)дкГБЪЊЕФПеЦјжаЃЌNF3 ФмгыЫЎеєЦјЗЂЩњбѕЛЏЛЙдЗДгІЃЌЦфЗДгІЕФВњЮягаЃКHFЁЂNOКЭHNO3 ЃЌдђдкNF3ЁЂF2 ЁЂNOШ§жжЦјЬхжаЃЌбѕЛЏадгЩШѕЕНЧПЕФЫГађЮЊ ЁЁЁЁЁЁЁЁЁЃ
20ЃЎ(7Зж)НёгавЛЛьКЯЮяЕФЫЎШмвКЃЌжЛПЩФмКЌгавдЯТРызгжаЕФШєИЩжжЃКK+ЁЂH+ЁЂ I-ЁЂMg2+ЁЂBa2+ЁЂSO42-ЁЂCO32-ЁЂNO3-ЃЌЯжШЁЖўЗнИї100 mLШмвКНјааШчЯТЪЕбщЃК
ЂйЕквЛЗнМгзуСПNaHCO3 ШмвКЃЌМгШШКѓЃЌЪеМЏЕНЦјЬх0.05 mol
ЂкЕкЖўЗнМгзуСПBaCl2 ШмвКЃЌГфЗжЗДгІКѓЙ§ТЫИЩдяЃЌЕУГСЕэ4.66 gЁЃ
ИљОнЩЯЪіЪЕбщЛиД№
(1)ШмвКжавЛЖЈВЛДцдкЕФРызгЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
(2)ШмвКжаЮоЗЈШЗЖЈЪЧЗёДцдкЕФбєРызгЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
(3)ШмвКжавЛЖЈДцдкЕФвѕРызгЪЧЁЁЁЁЁЁ ЃЌЦфЮяжЪЕФСПХЈЖШЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
19ЃЎ(8Зж)ЪЕбщЪвгћХфжЦ100mLХЈЖШЮЊ0.5 molЁЄL-1ЕФNaOHШмвКЃЌгавдЯТВйзїВНжшЃК
ЁЁ ЂйАбГЦСПКУЕФNaOHЙЬЬхЗХдкаЁЩеБжаМгЪЪСПЕФеєСѓЫЎШмНтЃЌВЂРфШДжСЪвЮТЁЃ
ЁЁ ЂкНЋШмНтРфШДКѓЕФШмвКаЁаФЕизЊвЦШЫШнСПЦПжаЁЃ
ЁЁ ЂлМЬајЯђШнСПЦПжаМгеєСѓЫЎжСОрПЬЖШЯпlcm~2cmДІЃЌИФгУНКЭЗЕЮЙмаЁаФЕЮМгеєСѓЫЎжСШмвКАМвКУцзюЕЭЕугыПЬЖШЯпЯрЧаЁЃ
ЁЁ ЂмНЋШнСПЦПЦПШћШћНєЃЌГфЗжвЁдШЁЃ
ЁЁ ЂнгУЩйСПеєСѓЫЎЯДЕгЩеБКЭВЃСЇАє2~3ДЮЃЌУПДЮЕФЯДЕгвКЖМаЁаФзЊвЦШЫШнСПЦПЃЌВЂЧсЧсвЁдШЁЃ
ЁЁ ЧыЛиД№ЯТСаЮЪЬтЃК
ЁЁ (1)ашвЊГЦШЁNaOHЙЬЬхЕФжЪСПЮЊЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ(2)ХфжЦNaOHШмвКЪБЃЌе§ШЗЕФВйзїЫГађЮЊ(ЬюаДађКХ)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)дкећИіХфжЦЙ§ГЬжаЃЌашвЊгУЕНЕФвЧЦїЃЌГ§СЫЩеБЁЂВЃСЇАєЁЂНКЭЗЕЮЙмЭтЃЌЛЙБиаыгУЕНЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЃ
(4)ЯТСаВйзїФмЪЙЫљХфШмвКХЈЖШЦЋИпЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ AЃЎЖЈШнЪБИЉЪгШнСПЦПЕФПЬЖШЯп
ЁЁ BЃЎЯђШнСПЦПжазЊвЦШмвКЪБЃЌгаШмвКШїТфдкШнСПЦПЭт
ЁЁ CЃЎЯђШнСПЦПжаЕЮМгеєСѓЫЎЪБЃЌВЛЩїГЌЙ§СЫПЬЖШЯп
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com