
4、 一般的共价键和配位键 --根据原子提供轨道和电子的方式
配位键是一种特殊的共价键,一方提供孤电子对(如NH3、H2O 、CO、NO2-、CN-、Cl-等),一方有空轨道(如H+、BF3、Cu2+、Ag+等),孤电子对进入空轨道,从而形成配位键。
3、 极性键和非极性键 --根据共用电子对是否偏向
2、 σ键与π键 --根据原子轨道的重叠方式不同
|
键类型 |
σ键 |
π键 |
|
原子轨道重叠方式 |
沿键轴方向相对重叠,即头碰头 |
沿键轴方向平行重叠,即肩并肩 |
|
原子轨道重叠部位 |
两原子核之间,在键轴处 |
键轴上方和下方,键轴处为零 |
|
原子轨道重叠程度 |
大 |
小 |
|
键的强度 |
较大 |
较小 |
|
化学活泼性 |
不活泼 (如乙烷) |
活泼 (如乙烯) |
1、 共价键的本质及特征
(1) 概念:原子间通过共用电子对形成的化学键叫共价键。
(2) 本质:共用电子对与成键的两个原子核之间的电性作用力。
(3) 特征:既有饱和性又有方向性。
2、关于假说:
假说的定义:是以已有事实材料和科学理论为依据,面对未知事实或规律所提出的一种推测性说明。假说提出后需得到实践的证实,才能成为科学理论。
1、关于模型:
①模型的定义:是以客观事实为依据建立起来的,是对事物及其变化的简化模拟。
②模型的分类:一般可分为物体模型和思维模型两大类。
例如,在研究有机化合物的结构时经常用到的球棍模型就是一种物体模型,而在研究原子结构的过程中所建立起的各种模型则属于思维模型。
在实验中,经常是同时使用其中的几种方法(以氯气为例)。
第一步:观察认识氯气的物理性质

第二步:预测氯气的性质。氯气是活泼非金属,则可与金属、非金属反应
第三步:通过实验论证氯气的化学性质

探究氯气的特性--氯气与水反应

第四步:对实验现象进行分析、综合、推论,概括出物质的通性及特性
氯气是呈黄绿色、有刺激性气味的气体,氯气可溶于水形成浅黄绿色的氯水
氯气的化学性质:
2Fe+3Cl2 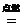 2FeCl3 Cu+Cl2
2FeCl3 Cu+Cl2
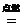 CuCl2
CuCl2
Cl2 +H2 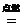 2HCl
Cl2+H2O=HCl+HClO
2HCl
Cl2+H2O=HCl+HClO
根据氯气能与水反应生成盐酸和次氯酸的事实,推论氯气是能与碱溶液反应
氯气 + 碱溶液 → 金属氯化物 + 次氯酸盐 + 水
Cl2+2NaOH=NaCl+NaClO+H2O(应用于实验室制氯气时尾气的吸收和工业制取漂白剂)
2Cl2+2Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2H2O(应用于工业制取漂白粉)
总之,研究物质性质的基本程序应该是:
观察物理性质 → 预测化学性质 → 验证或探究预测的性质 →分析现象并解释 → 分类、比较、归纳、概括同类物质的性质 → 性质的延伸和应用
1、基本程序
首先,要观察物质的外观性质(包括物质的存在状态、颜色气味等);
4、比较法
运用比较的方法,可以找出物质的组成、结构或性质间的异同,认识物质间的内在联系,对物质的组成、结构或性质等进行归纳和概括
应用分类法和比较法研究物质的性质的实例:比较金属钠与金属铁性质
|
性质 |
相同点 |
不同点 |
|
物理性质 |
不透明、银白色,易导电、导热,具有延展性 |
金属钠与铁相比,密度小,硬度小,熔点、沸点低 |
|
化学性质 |
①都能与非金属反应②都能与盐酸或稀硫酸反应产生H2③都能与盐反应 |
反应时需要的条件不同;反应的剧烈程度不同;通常条件下,钠与水剧烈反应,而铁不反应 |
上面是研究物质的性质时常用的四种方法,当然还有其他的一些方法;在研究物质的某方面性质时,可能只用到一种或两种方法,但在研究物质的整体性质时却常常是观察、实验、分类、比较等方法综合应用。在初中化学的学习中,常使用研究物质的性质的方法归类
|
物质的性质 |
研究方法 |
|
|
1.研究物质的物理性质 |
氧气、氢气、铁、盐酸等物质的颜色、状态 |
观察法 |
|
2.探究物质的化学性质 |
氧气的助燃性 |
观察和实验法 |
|
氢气的可燃性、还原性 |
观察和实验法 |
|
|
二氧化碳的化学性质(灭火性、与碱反应) |
观察和实验法 |
|
|
盐酸的化学性质 |
观察和实验法 |
|
|
3.归纳同类物质的共性 |
金属的通性 |
分类、比较法 |
|
酸的通性 |
分类、比较法 |
基本程序
3、分类法
到目前为止,人类已发现以及人工合成的各种物质已达三千多万种,根据物质的组成、结构等因素,我们可以分门别类地对物质及其变化进行研究,可以总结出各类物质的通性和特性;反之,知道某物质的类别,我们就可根据这类物质的通性推知该物质的一般性质。
对物质进行分类的依据有很多,如组成、结构、某种性质、用途等,以何种因素作为分类的依据,关键是看研究的出发点和目的。
例1:下列物质:金属铁、金属锌、木炭、CuO、CaCO3、H2SO4、NaOH、Ba(OH)2、NaCl、CuSO4 有人根据不同的依据进行了分类如下,请在适当的位置指出他分类的依据
|
分 类 依 据 |
分 类 |
|
① |
类别一:金属铁、金属锌、木炭 类别二:CuO、CaCO3、H2SO4、NaOH、Ba(OH)2、NaCl、CuSO4 |
|
② |
类别一:金属铁、金属锌、 类别二:木炭 类别三:CuO 类别四:H2SO4 类别五:NaOH、Ba(OH)2 类别六:CaCO3、NaCl、CuSO4 |
|
③ |
类别一:金属铁、金属锌、木炭、CuO、CaCO3 类别二:H2SO4、NaOH、Ba(OH)2、NaCl、CuSO4 |
解析:第一种情况分类的依据是物质的元素组成,将题给物质分成了单质和化合物;第二种情况分类的依据是物质的组成和性质,将题给物质分成了金属、非金属、氧化物、酸、碱、盐;第三种情况分类的依据是水溶性,将题给物质分成了溶与不溶两类。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com