
27、为测试一铁片中铁元素的含量,某课外活动小组提出下面两种方案并进行了实验(以下数据为多次平行实验测定结果的平均值):
方案一:将a g铁片完全溶解于过量稀硫酸中,测得生成氢气的体积为580mL(标准状况);
方案二:将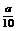 g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.02000mol·L-1的KMnO4溶液滴定,达到终点时消耗了25.00mL KMnO4溶液。请回答下列问题:
g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.02000mol·L-1的KMnO4溶液滴定,达到终点时消耗了25.00mL KMnO4溶液。请回答下列问题:
⑴配平下面的化学方程式(将有关的化学计量数填入答题卡的横线上):
KMnO4+ FeSO4+ H2SO4= Fe2(SO4)3+ MnSO4+ K2SO4+ H2O
⑵在滴定实验中不能选择 式滴定管,理由是 ;
⑶根据方案一和方案二测定的结果计算,铁片中铁的质量分数依次为 和
;(铁的相对原子质量以55.9计)
⑷若排除实验仪器和操作的影响因素,试对上述两种方案测定结果的准确性做出判断和分析。
①方案一 (填“准确”“不准确”“不一定准确”),理由是 ;
②方案二 (填“准确”“不准确”“不一定准确”),理由是 。
26、氮化铝(AlN,Al和N的相对原子质量分别为27和14)广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN可通过反应Al2O3+N2+3C 2AlN+3CO合成。下列叙述正确的是(
)
2AlN+3CO合成。下列叙述正确的是(
)
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中,每生成1molAlN需转移3mol电子
C.AlN中氮元素的化合价为+3
D.AlN的摩尔质量为41g
25、下列做法中用到物质氧化性的是( )
A.明矾净化水 B.纯碱除去油污
C.臭氧消毒餐具 D.食醋清洗水垢
24、 已知在热的碱性溶液中,NaClO发生如下反应:3NaClO→2NaCl+NaClO3。在相同条件下NaClO2也能发生类似的反应,其最终产物是(
)
已知在热的碱性溶液中,NaClO发生如下反应:3NaClO→2NaCl+NaClO3。在相同条件下NaClO2也能发生类似的反应,其最终产物是(
)
A.NaCl、NaClO B.NaCl、NaClO3 C.NaClO、NaClO3 D.NaClO3、NaClO4
23、锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水。当生成1 mol硝酸锌时,被还原的硝酸的物质的量为( )
A.2mol B.1 mol C.0.5mol D.0.25mol
22、(NH4)2SO4在高温下分解,产物是SO2、H2O、N2和NH3。在该反应的化学方程式中,化学计量数由小到大的产物分子依次是( )
A.SO2、H2O、N2、NH3 B.N2、SO2、H2O、NH3
C.N2、SO2、NH3、H2O D.H2O、NH3、SO2、N2
21.Cl2 和NH3 能发生下列反应:3Cl2+8NH3=6NH4Cl+N2 。
⑴该反应中氧化剂是 ,还原剂是 。被氧化的
NH3 占参加反应的NH3的 ;氧化剂与作还原剂物质的分子个
数比为 ⑵若有6.8g NH3 参加了反应,则被氧化的NH3
为 g,生成氧化产物 g。
C.能力训练
20.在一定条件下,RO3n- 与I- 发生反应的离子方程式为:
RO3n- +6I- + 6H+ = R- +3I2 + 3H2O ,推断RO3n-中n的数值为
,R元素的化合价为 ,R是周期表中 族元素。
19.有如下微粒①Mg2+、②N2、③Cu2+、④Cl2、⑤Fe2+、⑥S2-、
⑦Fe3+、⑧Al,其中只有氧化性的微粒是 ;只有还原性的
微粒是 ;既有氧化性又有还原性的微粒是 。
18.将KCl和CrCl3两种固体混合物共熔制得化合物X,X由K、Cl、Cr元素组成。将1.892gX中Cr元素全部氧化成Cr2O72-, Cr2O72-可过量的KI中氧化出2.667g I2,反应离子方程式是:
Cr2O72-+6I-+14H+=2Cr3++3 I2+7H2O,如果取溶有1.892g X的溶液,加入过量的AgNO3,可得4.52g AgCl沉淀,则表示X组成
的化学式为 ( )
A K3Cr2Cl7 B K3Cr2Cl5 C K3Cr2Cl9 D K2CrCl4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com