
25.(8分)
(1)2009年9月至今,我国各个地区也接连暴发甲H1N1流感(或称H1N1型猪流感)疫情,防控专家表示,含氯消毒剂和过氧化物消毒可防甲型H1N1流感。二氧化氯 是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与Na2SO3反应制得。请写出反应的离子方程式:
。
是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与Na2SO3反应制得。请写出反应的离子方程式:
。
(2)漂白剂亚氯酸钠(NaClO2)在常温黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平)。当1molHClO2发生分解反应时,转移的电子个 数是
。
数是
。
(3)有Fe2+、NO-3、Fe3+、NH+4、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,则该反应中还原剂与氧化剂的物质的量之比为 。
(4)完成下列方程式:
3Fe+1NO-2+ OH-→3FeO2-2+1H2O 。
24.(1)在某容积不变的密闭容器中,有可逆反应:
 Ma(g)+Nb(g) pC(g)+qD(g)+Q(Q>0)
Ma(g)+Nb(g) pC(g)+qD(g)+Q(Q>0)
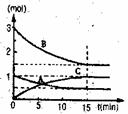
如图某反应过程中各物质的量n(mol)随时间t(min)的
变化曲线图。达到化学平衡:
①该反应的平衡常数表达式为 ;
②若充入A,K值 (填一定增大、一定减小、或可能增大也可能减小、不变)。正反应速率 (填增大、减小、不变)
③若体积为10升的密闭容器中,500°C、有催化剂存在的条件下,根据图示回答下列问题;在0~15min内的平均反应速率:v(B)= 。

 (2)对于某可逆反应:A(g)+B(g) 2C(g)+Q(Q>0)。若该反应的正反应速率与时间关系如下图所示。在其它条件不变的情况下,请填空:
(2)对于某可逆反应:A(g)+B(g) 2C(g)+Q(Q>0)。若该反应的正反应速率与时间关系如下图所示。在其它条件不变的情况下,请填空:
①写出t2时改变的条件可能是 (用文字表达)
②写出t4时改变的条件可能是 (用编号表
示,多选扣分)
A.增大压强 B.减小压强
C.使用催化 剂 D.升高温度
剂 D.升高温度
E.增大A的浓度
23.现有A、B、C、D四种短周期元素(零族除外),请根据信息回答下列问题。
|
元素 |
A |
B |
C |
D |
|
性质或结构信息 |
元素非金属性较强,其最高价氧化物对应的水化物为强酸,但其单质稳定,常作保护气。 |
原子核外电子占了4个轨道 |
原子半径仅比氢原子大,其氢化物溶于水形成弱酸 |
其原子核外有13种运动状态的电子 |
(1)A元素原子单质电子式为: ,B元素在元素周期有中的位置是 。
(2)写出C元素单质与水反应的化学方程式 ;
A、C两元素的氢化物的稳定性强弱是 > (用化学式表示)
(3)D元素最高价氧化物对应的水化物呈 (填:酸性、碱性或非极性),能说明这一结论的电离方程式为 。
 (4)B元素最简单的氢化物分子为
分子(填:极性或非极性)。8g该氢化物在空气中完全燃烧生成液态水时,放出445.15kJ热量,该反应的热化学方程式为
(4)B元素最简单的氢化物分子为
分子(填:极性或非极性)。8g该氢化物在空气中完全燃烧生成液态水时,放出445.15kJ热量,该反应的热化学方程式为
22.某稀硫酸和硝酸的混合溶液200mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉的质量增加的变化如下图所示。下列分析或结果正确的是 ( )
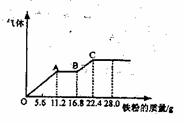 A.混合酸中NO-3物质的理为0.2mol
A.混合酸中NO-3物质的理为0.2mol
B.OA段产生的是NO,AB段的反应为:
Fe+2Fe3+→3Fe2+,BC段产生氢气
C.第二份溶液中最终溶质为FeSO4
D.H2SO4浓度为5mol·L-1
第二卷(共84分)
21.①pH=3的CH3COOH溶液;②Ph=3的HCl溶液;③Ph=11的氨水;④pH=11的NaOH溶液。相同条件下,有关上述溶液的比较中,正确的是 ( )
A.将②、③溶液混合后,pH=7,消耗溶液的 体积:②>③
体积:②>③
B.水电离产生的c(H+):①=②=③=④
C.等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量;②最大
D.向溶液中加入100mL水后,溶液的pH:③>④>①>②
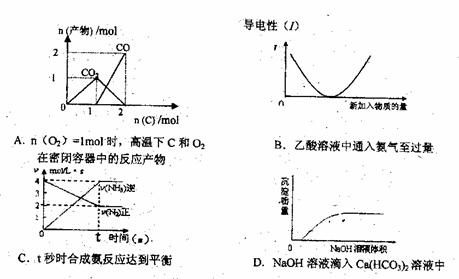
20.化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是 ( )
19.某反应体系中的物质有NaOH、Au2O3,Na2S4O6,Au2O,H2O,Na2S2O3。Au2O3为反应物,则下列有关说法正确的是 ( )
A.该反应体系中有三种元素的价态发生了变化
B.Au2O在反应中作还原剂
C.Na2S4S6发生还原反应
D.1molAu2O3发生反应,转移电子4moL
18.下列离子方程式正确的是 ( )
A.硫酸铝溶液中加过量氨水:Al3++4OH-→AlO2-+2H2O
B.向苯酚钠溶液中通入少量的二氧化碳:CO2+H2O+C6H5O-→C6H5OH+HCO-3
C.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至刚好沉淀完全:
Ba2++2OH-+NH+4+H++SO2-4→BaSO4↓+NH3·H2O+H2O
D.过量铁粉与一定量稀硝酸反应:Fe+4H++NO-3→Fe3++NO↑+2H2O
16.某溶液中仅含有Na+、H+、OH-、CH3COO-四种离子,下列说法错误的是 ( )
A.若溶液中部分离子间满足:c(CH3COO-)=c(Na+)则该溶液一定呈中性
B.若溶液中溶质仅为CH3COONa,则离子间一定满足:
C(Na+)>c(CH3COO-)>c(OH-)>c(H+)
C.溶液中四种离子之间可能满足:c(Na+)>c(OH-)>c(CH3DCOO-)>c(H+)
D.若溶液中的溶质是CH3COONa和CH3COOH,则溶液中离子间一定满足:
C(CH3COO-)>c(Na+)>c(H+)>c(OH-)
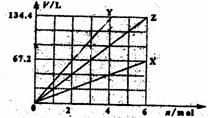 17.右图表示金属X、Y以及它们的合金Z分别与足量盐酸反
17.右图表示金属X、Y以及它们的合金Z分别与足量盐酸反
应时产生氢气的情况,其中横坐标表示消耗金属的物质的
量,纵坐标表示产物氢气的体积(标准状况)。下列对有关
Z 的组成的判断,正确的是 ( )
A.n(Na):n(Fe)=2:1
B.n(Mg):n(K)=1:2
C.n(Na):n(Al)=1:3
D.n(K):n(Al)=1:1
15.用NA表示阿伏加德罗数的值。下列叙述正确的是 ( )
A.25°C时,Ph=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA
B.标准状况下,2.24LCl2与过量烯的NaOH溶液反应,转移的电子总数为0.2NA
C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
D.标准状况下,22.4L乙醇中含有的氧原子数为1.0NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com